
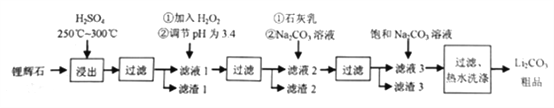
【題目】工業上以鋰輝石為原料生產碳酸鋰的部分工業流程如下:
已知:①鋰輝石的主要成分為Li2O·Al2O3·4SiO2,其中含少量FeO、MgO等。
②Li2O·Al2O3·4SiO2+H2SO4![]() Li2SO4+Al2O3·4SiO2·H2O
Li2SO4+Al2O3·4SiO2·H2O
③某些物質的溶解度(S)如下表所示。
T℃ | 20 | 40 | 60 | 80 |
S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
④Fe3+完全沉淀時pH為3.4
(1)為提高原料浸出速率,除升高溫度外還可采取的措施是__________(任寫一條)。
(2)在濾液1中加入H2O2的目的是__________(用離子方程式表示);調節pH最佳試劑是__________(填序號 )。
A.CuO B.CuCO3 C.MgO D.NH3·H2O
(3)從濾渣中分離出Al2O3的流程如下圖所示,請寫出生成沉淀的離子方程式__________。
![]()
(4)向濾液2中加入Na2CO3溶液的作用是__________。
(5)“過濾、熱水洗滌”步驟中,“熱水洗滌”的原因是__________;證明沉淀已洗凈的操作是__________。
【答案】適當增大硫酸濃度、減小原料顆粒直徑、攪拌等(合理答案均可給分) 2Fe2++H2O2+2H+ =2Fe3++2H2O C Al3++3NH3·H2O=Al(OH)3↓+3NH4+ 使Ca2+完全轉化為沉淀(或除去Ca2+) 碳酸鋰在熱水中溶解度較小,熱水洗滌可減少產品損失 取最后一次洗滌液,加入鹽酸酸化,滴加Ba2+溶液,若無沉淀產生,說明已洗凈
【解析】
鋰輝石(Li2OAl2O34SiO2,含少量少量FeO、MgO等)經過加入硫酸酸化得到可溶性的硫酸鋰、硫酸鋁、硫酸亞鐵、硫酸鎂和不溶的二氧化硅,經過過濾,得到濾渣1二氧化硅,濾液1加入過氧化氫氧化亞鐵離子為鐵離子,調節溶液PH=3.4,Fe3+完全沉淀,過濾得到濾渣2為氫氧化鐵,濾液2加入石灰乳和碳酸鈉溶液,以增加Ca2+、OH-的濃度,使Mg(OH)2、CaCO3更利于析出,過濾得到濾液Mg(OH)2和CaCO3,以便形成濾渣3,濾液中加入飽和碳酸鈉溶液沉淀鋰離子生成Li2CO3的沉淀,過濾熱水洗滌Li2CO3的溶解度隨溫度升高而減小,可減少Li2CO3的損失,得到最終產物碳酸鋰。
(1)為提高原料浸出速率,除升高溫度外還可采取的措施是:適當增大硫酸濃度、減小原料顆粒直徑、攪拌等,故答案為:適當增大硫酸濃度、減小原料顆粒直徑、攪拌等;
(2)在濾液1中加入H2O2的目的是氧化亞鐵離子調節溶液pH沉淀鐵離子,反應的離子方程式為:2Fe2++H2O2+2H+=2Fe3++2H2O,調節pH最佳試劑是不能引入新的雜質,AB會引入銅離子,D會引入銨根離子,所以調節pH最佳試劑是C氧化鎂,故答案為:2Fe2++H2O2+2H+=2Fe3++2H2O;C;
(3)從濾渣中分離出Al2O3的流程如下所示,其中生成沉淀的反應是鋁鹽和過量氨水生成,反應的離子方程式Al3++3NH3H2O=Al(OH)3↓+3NH4+,故答案為:Al3++3NH3H2O=Al(OH)3↓+3NH4+;
(4)向濾液2中加入Na2CO3溶液的作用是使Ca2+完全轉化為沉淀(或除去Ca2+),故答案為:使Ca2+完全轉化為沉淀(或除去Ca2+);
(5)圖表數據可知碳酸鋰溶解度隨溫度升高減小,“過濾、熱水洗滌”步驟中,“熱水洗滌”的原因是碳酸鋰在熱水中溶解度較小,熱水洗滌可減少產品損失,證明沉淀已洗凈的操作是:取最后一次洗滌液,加入鹽酸酸化,滴加Ba2+溶液,若無沉淀產生,說明已洗凈,故答案為:碳酸鋰在熱水中溶解度較小,熱水洗滌可減少產品損失;取最后一次洗滌液,加入鹽酸酸化,滴加Ba2+溶液,若無沉淀產生,說明已洗凈。


科目:高中化學 來源: 題型:
【題目】鎂的化合物在化工生產和藥物合成上有重要用途。某興趣小組以一種工業廢渣(主要成分為MgCO3、MgSiO3和少量Fe的氧化物)為原料制備MgCO3·3H2O。實驗過程如下:

(1)濾渣的成分為________(填化學式),過濾裝置在使用一段時間后需用NaOH溶液清洗,用化學方程式表示其清洗原理:____________________________。
(2)加入H2O2的目的是________________________,一段時間后,溶液中有氣泡出現并放熱,則產生氣泡的原因是_______________________________。
(3)萃取分液中要用到分液漏斗,分液漏斗在使用前須洗干凈并________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按如圖裝置進行實驗,下列描述正確的是(N裝置中兩個電極均為石墨棒)

A. C1上發生還原反應
B. Cu電極與C2電極上的電極反應相同
C. M 裝置中SO42-移向Cu電極
D. 工作一段時間后裝置M 中溶液pH變小,裝置N中溶液pH變大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用NaHCO3溶液處理NaAlO2溶液(由Al2O3過量NaOH溶液反應制得),測得溶液pH和Al(OH)3生成的量隨加入NaHCO3溶液體積的變化情況如圖所示。下列說法正確的是( )
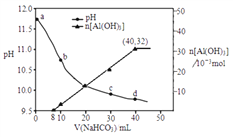
A. Al(OH)3的生成是因為NaHCO3促進了NaAlO2的水解
B. b點和c點溶液所含微粒種類不同
C. NaHCO3溶液的物質的量濃度為1.0mol·L-1
D. d點時:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】應用電化學原理,回答下列問題:
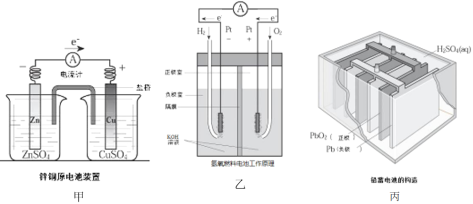
(1)上述三個裝置中,負極反應物化學性質上的共同特點是_________。
(2)甲中電流計指針偏移時,鹽橋(裝有含瓊膠的KCl飽和溶液)中離子移動的方向是________。
(3)乙中正極反應式為________;若將H2換成CH4,則負極反應式為_______。
(4)丙中鉛蓄電池放電一段時間后,進行充電時,要將外接電源的負極與鉛蓄電池______極相連接。
(5)應用原電池反應可以探究氧化還原反應進行的方向和程度。按下圖連接裝置并加入藥品(鹽橋中的物質不參與反應),進行實驗:

ⅰ.K閉合時,指針偏移。放置一段時間后,指針偏移減小。
ⅱ.隨后向U型管左側逐漸加入濃Fe2(SO4)3溶液,發現電壓表指針的變化依次為:偏移減小→回到零點→逆向偏移。
① 實驗ⅰ中銀作______極。
② 綜合實驗ⅰ、ⅱ的現象,得出Ag+和Fe2+反應的離子方程式是______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設計一個簡單的一次性完成實驗的裝置圖,驗證醋酸溶液、二氧化碳水溶液、苯酚溶液的酸性強弱順序是CH3COOH>H2CO3>C6H5OH。
(1)利用如圖所示的儀器可以組裝實驗裝置,則儀器的連接順序是____接D、E接_____、______接_____。
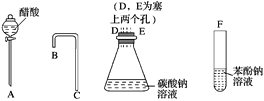
(2)有關反應的化學方程式為________________________________________________。
(3)有的同學認為此裝置不能驗證H2CO3和C6H5OH的酸性強弱,你認為________(填“有”或“沒有”)道理。怎樣改進實驗才能驗證H2CO3和C6H5OH的酸性強弱?
________________________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮、磷及其化合物在工農業生產中都有重要作用。
(1)基態磷原子價電子排布的軌道表示式為___________。
(2)元素B、N、O的第一電離能由大到小的順序為___________。
(3)食品添加劑NaNO2中NO2-中心原子的雜化類型是_____,與NO2-互為等電子體的分子的化學式為___________。(寫1種)。
(4)N2H4是火箭的燃料,與氧氣的相對分子質量相同,它在常溫常壓下是液態,而氧氣是氣態,造成這種差異的主要原因是____________。
(5)磷化硼是一種耐磨涂料,它可用作金屬的表面保護層。磷化硼可由三溴化硼和三溴化磷于高溫下在氫氣中反應合成。
①三溴化磷分子的空間構型是_________,三溴化硼鍵角是___________。
②磷化硼晶體晶胞如圖所示:其中實心球為磷原子,在一個晶胞中磷原子空間堆積方式為________,磷原子的配位數為___________,該結構中有一個配位鍵,提供空軌道的原子是___________。己知晶胞邊長apm,阿伏加德羅常數為NA。則磷化硼晶體的密度為___________g/cm3。

③磷化硼晶胞沿著體對角線方向的投影(圖中虛線圓圈表示P原子的投影),用實線圓圈畫出B原子的投影位置(注意原子體積的相對大小)。______
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(I)無水MgBr2可用作催化劑實驗室采用鎂屑與液溴為原料制備無水MgBr2,裝置如圖1。

主要步驟如下:
步驟1 三頸瓶中裝入10g鎂屑和150mL無水乙醚;裝置B中加入15mL液溴。
步驟2緩慢通入干燥的氮氣,直至溴完全導入三頸瓶中。
步驟3反應完畢后恢復至室溫,過濾除去鎂,濾液轉移至另一干燥的燒瓶中,冷卻至0℃,析出晶體,再過濾得三乙醚合溴化鎂粗品。
步驟4常溫下用苯溶解粗品,冷卻至0℃,析出晶體,過濾,洗滌得三乙醚合溴化鎂,加熱至160℃分解得無水MgBr2產品。
已知:①Mg和Br2反應劇烈放熱;MgBr2具有強吸水性。
②MgBr2+3C2H5OC2H5![]() MgBr2·3C2H5OC2H5
MgBr2·3C2H5OC2H5
請回答:
(1)儀器A的名稱是____________。實驗中不能用干燥空氣代替干燥N2,原因是___________。
(2)如將裝置B改為裝置C(圖2),可能會導致的后果是_______________________。
(3)有關步驟4的說法,正確的是___________。
A.可用95%的乙醇代替苯溶解粗品 B.洗滌晶體可選用0℃的苯
C.加熱至160℃的主要目的是除去苯 D.該步驟的目的是除去乙醚和可能殘留的溴
(4)為測定產品的純度,可用EDTA(簡寫為Y)標準溶液滴定,反應的離子方程式:Mg2++Y4-=MgY2-
①滴定前潤洗滴定管的操作方法是____________________________。
②測定前,先稱取0.2500g無水MgBr2產品,溶解后,用0.0500mol·L-1的EDTA標準溶液滴定至終點,消耗EDTA標準溶液26.50mL,則測得無水MgBr2產品的純度是________________________(以質量分數表示)。
(II)化合物Mg5Al3(OH)19(H2O)4可作環保型阻燃材料,受熱時按如下化學方程式分解:
2Mg5Al3(OH)19(H2O)4=27H2O+10MgO+3Al2O3
(1)寫出該化合物作阻燃劑的兩條依據__________________、_____________________;
(2)用離子方程式表示除去固體產物中Al2O3的原理________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com