
【題目】已知1mol某有機物M含碳原子 n mol,在恰好完全燃燒時消耗氧氣1.5n mol。請把符合條件的物質類別填入空格。
供選擇的物質類別有:烷烴、烯烴、炔烴、二烯烴、環烷烴、芳香烴、飽和一元醇、飽和一元醛、醚、酮。
(1)有機物M可能是(填物質的類別)_____________、_____________、_____________、_____________(你認為有幾種填幾種,但多填少填要扣分)。
(2)若 4.4克M與足量的金屬鈉反應可收集到560 ml氫氣(標準狀況),則有機物M一定是(填物質的類別)____________,且M的摩爾質量為___________________。
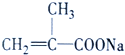
(3)具有支鏈的化合物A的分子式為C4H6O2,A可以使溴的四氯化碳溶液褪色。1molA和1mol NaHCO3能完全反應,則A的結構簡式是________________________。
(4)化合物B含有C、H、O三種元素,相對分子質量為60,其中碳的質量分數為60%,氫的質量分數為13.33%。B在Cu的催化作用下被氧氣氧化成C,C能發生銀鏡反應,則C發生銀鏡反應的化學方程式為__________________________。
(5)D在NaOH水溶液中加熱反應,可生成A的鈉鹽和B,相應反應的化學方程式是_____________
【答案】 烯烴 環烷烴 飽和一元醇 醚 飽和一元醇 88g/mol ![]() CH3CH2CHO+2[Ag(NH3)2]OH
CH3CH2CHO+2[Ag(NH3)2]OH![]() CH3CH2COONH4+2Ag+3NH3+H2O
CH3CH2COONH4+2Ag+3NH3+H2O ![]() +NaOH
+NaOH![]()
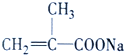 +CH3CH2CH2OH
+CH3CH2CH2OH
【解析】試題分析:(1)根據有機物燃燒通式![]() ,分析不同有機物燃燒耗氧量;(2)醇能與鈉反應放出氫氣;(3)1molA和1mol NaHCO3能完全反應,說明A分子中含有1個羧基;A可以使溴的四氯化碳溶液褪色,說明A中含有碳碳雙鍵;(4)B含有C、H、O三種元素,相對分子質量為60,其中碳的質量分數為60%,氫的質量分數為13.33%,則B中碳原子數是
,分析不同有機物燃燒耗氧量;(2)醇能與鈉反應放出氫氣;(3)1molA和1mol NaHCO3能完全反應,說明A分子中含有1個羧基;A可以使溴的四氯化碳溶液褪色,說明A中含有碳碳雙鍵;(4)B含有C、H、O三種元素,相對分子質量為60,其中碳的質量分數為60%,氫的質量分數為13.33%,則B中碳原子數是![]() 、氫原子數是
、氫原子數是![]() 、氧原子數
、氧原子數![]() ,所以B的分子式是C3H8O,B在Cu的催化作用下被氧氣氧化成C,C能發生銀鏡反應,B是CH3CH2CH2OH;(5)D在NaOH水溶液中加熱反應,可生成
,所以B的分子式是C3H8O,B在Cu的催化作用下被氧氣氧化成C,C能發生銀鏡反應,B是CH3CH2CH2OH;(5)D在NaOH水溶液中加熱反應,可生成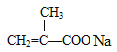 和CH3CH2CH2OH,所以D是酯,D是
和CH3CH2CH2OH,所以D是酯,D是![]() ;
;
解析:(1) 根據![]() ,烷烴通式是
,烷烴通式是![]() ,1mol烷烴恰好完全燃燒時消耗氧氣(1.5n+0.5) mol;烯烴的通式是
,1mol烷烴恰好完全燃燒時消耗氧氣(1.5n+0.5) mol;烯烴的通式是![]() ,1mol烯烴恰好完全燃燒時消耗氧氣1.5n mol;炔烴的通式是
,1mol烯烴恰好完全燃燒時消耗氧氣1.5n mol;炔烴的通式是![]() ,1mol炔烴恰好完全燃燒時消耗氧氣(1.5n-0.5)mol;、二烯烴的通式是
,1mol炔烴恰好完全燃燒時消耗氧氣(1.5n-0.5)mol;、二烯烴的通式是![]() ,1mol二烯烴恰好完全燃燒時消耗氧氣(1.5n-0.5)mol;環烷烴的通式是
,1mol二烯烴恰好完全燃燒時消耗氧氣(1.5n-0.5)mol;環烷烴的通式是![]() ,1mol環烷烴恰好完全燃燒時消耗氧氣1.5nmol;芳香烴中苯的同系物的通式是
,1mol環烷烴恰好完全燃燒時消耗氧氣1.5nmol;芳香烴中苯的同系物的通式是![]() ,1mol苯的同系物恰好完全燃燒時消耗氧氣(1.5n-1.5)mol;飽和一元醇的通式是
,1mol苯的同系物恰好完全燃燒時消耗氧氣(1.5n-1.5)mol;飽和一元醇的通式是![]() ,1mol飽和一元醇恰好完全燃燒時消耗氧氣1.5nmol;飽和一元醛的通式是
,1mol飽和一元醇恰好完全燃燒時消耗氧氣1.5nmol;飽和一元醛的通式是![]() ,1mol飽和一元醛恰好完全燃燒時消耗氧氣(1.5n-0.5)mol;醚的通式是
,1mol飽和一元醛恰好完全燃燒時消耗氧氣(1.5n-0.5)mol;醚的通式是![]() ,1mol醚恰好完全燃燒時消耗氧氣1.5nmol;酮的通式是
,1mol醚恰好完全燃燒時消耗氧氣1.5nmol;酮的通式是![]() ,1mol酮恰好完全燃燒時消耗氧氣(1.5n-0.5)mol;所以有機物M可能是烯烴、環烷烴、飽和一元醇、醚;(2)醇能與鈉反應放出氫氣,若 4.4克M與足量的金屬鈉反應可收集到560 ml氫氣(標準狀況),則有機物M一定是飽和一元醇;設M的結構簡式是
,1mol酮恰好完全燃燒時消耗氧氣(1.5n-0.5)mol;所以有機物M可能是烯烴、環烷烴、飽和一元醇、醚;(2)醇能與鈉反應放出氫氣,若 4.4克M與足量的金屬鈉反應可收集到560 ml氫氣(標準狀況),則有機物M一定是飽和一元醇;設M的結構簡式是![]() ;
;
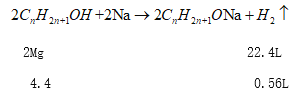
M=88,所以M的摩爾質量為88g/mol;
(3)1molA和1mol NaHCO3能完全反應,說明A分子中含有1個羧基;A可以使溴的四氯化碳溶液褪色,說明A中含有碳碳雙鍵;A具有支鏈,A的分子式為C4H6O2,則A的結構簡式是![]() ;(4)B含有C、H、O三種元素,相對分子質量為60,其中碳的質量分數為60%,氫的質量分數為13.33%,則B中碳原子數是
;(4)B含有C、H、O三種元素,相對分子質量為60,其中碳的質量分數為60%,氫的質量分數為13.33%,則B中碳原子數是![]() 、氫原子數是
、氫原子數是![]() 、氧原子數
、氧原子數![]() ,所以B的分子式是C3H8O,B在Cu的催化作用下被氧氣氧化成C,C能發生銀鏡反應,B是CH3CH2CH2OH,B氧化為C,C是CH3CH2CHO;CH3CH2CHO發生銀鏡反應的化學方程式為CH3CH2CHO+2[Ag(NH3)2]OH
,所以B的分子式是C3H8O,B在Cu的催化作用下被氧氣氧化成C,C能發生銀鏡反應,B是CH3CH2CH2OH,B氧化為C,C是CH3CH2CHO;CH3CH2CHO發生銀鏡反應的化學方程式為CH3CH2CHO+2[Ag(NH3)2]OH![]() CH3CH2COONH4+2Ag+3NH3+H2O;(5)D在NaOH水溶液中加熱反應,可生成
CH3CH2COONH4+2Ag+3NH3+H2O;(5)D在NaOH水溶液中加熱反應,可生成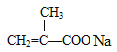 和CH3CH2CH2OH,所以D是
和CH3CH2CH2OH,所以D是![]() ;
;![]() 在氫氧化鈉的水溶液中發生水解的方程式是
在氫氧化鈉的水溶液中發生水解的方程式是![]() +NaOH
+NaOH![]()
 +CH3CH2CH2OH。
+CH3CH2CH2OH。


 舉一反三單元同步過關卷系列答案
舉一反三單元同步過關卷系列答案科目:高中化學 來源: 題型:
【題目】下面三個圖是某研究小組利用過氧化氫酶探究H2O2分解條件而獲得的實驗結果.請回答下列有關問題:

(1)圖1、2、3所代表的實驗中,實驗自變量依次為 , , .
(2)根據圖1可以得出的實驗結論是 _.
(3)圖2曲線bc段產生的最可能原因是 .
(4)若進行圖2所代表的實驗時增加過氧化氫酶的含量,請在圖2中,利用虛線繪出曲線的變化
(5)能否以H2O2為材料來探究溫度對H2O2酶活性的影響? 為什么 .
(6)酶的作用原理 ,酶的本質 . .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:2N2O5(g)![]() 4NO2(g) + O2(g) ΔH=+Q kJmol-1 (Q>0),某溫度下,向2L的密閉容器中通入N2O5,部分實驗數據見下表:
4NO2(g) + O2(g) ΔH=+Q kJmol-1 (Q>0),某溫度下,向2L的密閉容器中通入N2O5,部分實驗數據見下表:
時間/s | 0 | 500 | 1000 | 1500 |
n(N2O5)/mol | 10.0 | 7.0 | 5.0 | 5.0 |
下列說法正確的是
A. 在500s內,O2分解速率為3×10-3 molL-1s-1
B. 在1000s時,反應恰好達到平衡
C. 在1000s內,反應吸收的熱量為2.5Q kJ
D. 在1500s時,N2O5的正反應速率等于NO2的逆反應速率
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】茶是我國的傳統飲品,茶葉中含有的茶多酚可以替代食品添加劑中對人體有害的合成抗氧化劑,用于多種食品保鮮等,如圖所示是茶多酚中含量最高的一種兒茶素A的結構簡式,關于這種兒茶素A的有關敘述正確的是( )
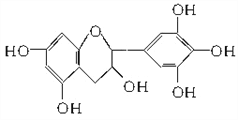
①分子式為C15H14O7 ②1 mol兒茶素A在一定條件下最多能與7 mol H2加成 ③等質量的兒茶素A分別與足量的金屬鈉和氫氧化鈉反應消耗金屬鈉和氫氧化鈉的物質的量之比為1∶1 ④1 mol兒茶素A與足量的濃溴水反應,最多消耗4 molBr2
A. ①② B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸銨是一種常見的化肥,某工廠用石膏、NH3、H2O、CO2制備硫酸銨的工藝流程如下:
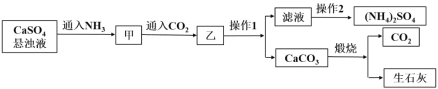
下列說法不正確的是
A. 操作1為過濾,操作2為蒸餾
B. 濾液中的主要陽離子可通過向少量濾液中加NaOH溶液,加熱,并用濕潤的紅色石蕊試紙來檢驗
C. 甲到乙反應的離子方程式為CaSO4+2NH3+CO2+H2O==CaCO3↓+2NH4++ SO42-
D. 工藝流程中產生的CO2可循環利用
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有部分短周期元素的性質或原子結構如下表:
元素符號 | 元素性質或原子結構 |
T | M層上的電子數是原子核外電子層數的2倍 |
X | 最外層電子數是次外層電子數的2倍 |
Y | 常溫下單質為雙原子分子,其氫化物水溶液呈堿性 |
Z | 元素最高正價是+7價 |
下列敘述中不正確的是( )
A.14X可用與測定文物年代
B.Z的非金屬性比T強
C.Y和T位于同一主族
D.X元素形成的化合物種類很多
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮元素在地球上含量豐富,其中氨氣在工農業生產生活中有著重要的作用。
(1)大氣中氮以_________(填微粒符號)形式存在。固氮是氮循環的重要環節,工業固氮制NH3反應溫度選擇500℃左右的原因是________________________________。
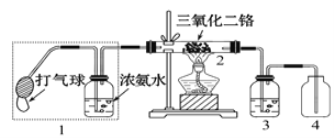
(2)某興趣小組用如圖裝置探究氨的催化氧化,加熱玻璃管2一段時間后,擠壓1中打氣球鼓入空氣,觀察到2中物質呈紅熱狀態;停止加熱后仍能保持紅熱,該反應是_________反應(填“吸熱”或“放熱”)。
(3)上圖中若取消3,在4中僅觀察到大量白煙,該白煙的化學式可能為______________。
(4)實驗室還可用濃氨水與氫氧化鈉固體混合,制得氨氣。請用平衡移動及其他相關的理論解釋該方法能制備氨氣的原因:_____________________________________________。
(5)按下圖裝置進行氨氣的性質實驗(旋塞1和旋塞2實驗前關閉),G、H是兩個等體積的容器。先打開旋塞1,一段時間后,關閉旋塞1,再打開旋塞2,H瓶中現象依次是:________________________。
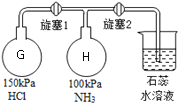
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列現象或事實可用同一原理解釋的是( )
A.不能用pH試紙測定濃硫酸和新制氯水的pH
B.濃硫酸和濃鹽酸長期暴露在空氣中濃度降低
C.SO2和FeSO4溶液使酸性高錳酸鉀的紫色褪去
D.氫氧化鈉固體易潮解和鋁制容器可用盛裝濃硫酸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應中生成物總能量高于反應物總能量的是
A. 鐵與鹽酸反應 B. 乙醇燃燒
C. 鋁粉與氧化鐵粉末反應 D. Ba(OH)2·8H2O 與NH4Cl 反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com