
分析 ①加入AgNO3溶液有沉淀產生,說明溶液中可能存在Cl-、CO32-、SO42-;
②4.66g為硫酸鋇沉淀,其物質的量為0.02mol,8.6g為硫酸鋇和碳酸鋇,據此可以計算出碳酸鋇的物質的量;
再根據電荷守恒,得出一定存在鈉離子,據此進行判斷.
解答 解:①與AgNO3溶液有沉淀產生的離子有Cl-、CO32-、SO42-;
②不溶于硝酸的4.66g沉淀為硫酸鋇,硫酸鋇的物質的量是:$\frac{4.66g}{233g/mol}$=0.02mol;8.6g沉淀是硫酸鋇和碳酸鋇,碳酸鋇質量為:8.6g-4.66g=3.94g,碳酸鋇物質的量為:$\frac{3.94g}{197g/mol}$=0.02mol,所以原溶液中一定存在:CO32-、SO42-,因而一定沒不含Ba2+和Mg2+,由溶液電中性原則可知,一定存在Na+,
c(CO32-)=c(SO42-)=$\frac{0.02mol}{0.1L}$=0.2mol/L,再根據電荷守恒,正電荷為:n(+)=n(Na+)=0.08mol;
(1)根據以上分析可知:原溶液中一定存在的離子有Na+、CO32-、SO42-,一定沒有的離子Mg2+、Ba2+,可能存在Cl-,碳酸鋇與硝酸反應生成硝酸鋇、二氧化碳氣體和水,離子反應方程式為:BaCO3+2H+═Ba2++H2O+CO2↑,故答案為:Na+、CO32-、SO42-;Mg2+、Ba2+;Cl-;BaCO3+2H+═Ba2++H2O+CO2↑;
(2)n(Na+)=2n(CO32-)+2n(SO42-)=0.02×2+0.02×2=0.08mol,若存在氯離子,那么鈉離子>0.08mol,故答案為:≥0.08.
點評 本題考查離子的檢驗,采用定性實驗和定量計算分析相結合的模式,增大了解題難度,同時涉及離子共存、離子反應等都是解題需注意的信息,尤其是K+的確定易出現失誤.


科目:高中化學 來源: 題型:選擇題
| A. | C2H6和C4H10一定是同系物 | |
| B. | C2H4和C4H8一定是同系物 | |
| C. | C3H6不只表示一種物質 | |
| D. | 烯烴中各同系物中碳的質量分數相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 負極反應Al-3e-Al3+ | B. | 燃料氣體是氧氣 | ||
| C. | 正極反應為2CO2+O2+4e-2CO32- | D. | 該電池不能用烴類物質作燃料 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
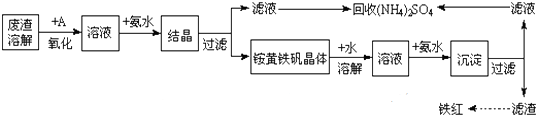
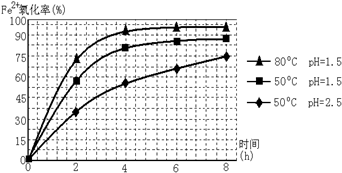
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將CH3CH2Br與NaOH溶液共熱,冷卻,取上層溶液加AgNO3溶液,觀察是否產生淡黃色沉淀,檢驗CH3CH2Br與NaOH溶液是否發生反應 | |
| B. | 在實驗室,將乙醇和濃硫酸的混合物共熱發生反應,生成能使酸性KMnO4溶液褪色的氣體,此氣體一定是乙烯 | |
| C. | 室溫下向苯和少量苯酚的混合液中加入適量燒堿溶液,振蕩、靜置后分液,可除去其中的苯酚 | |
| D. | 將硝酸銀溶液和少量乙醛于試管中充分混合后,把試管放在熱水浴中加熱,在試管內壁上有光亮的銀鏡出現 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋅錳干電池工作一段時間后碳棒變細 | |
| B. | 氫氧燃料電池可將熱能直接轉變為電能 | |
| C. | 太陽能電池的主要材料是高純度的二氧化硅 | |
| D. | 氫氧燃料電池工作時氫氣在負極被氧化 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 開始沉淀時 | 3.4 | 6.3 | 1.5 |
| 完全沉淀時 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3CH2OH$→_{170℃}^{濃硫酸}$CH2═CH2↑+H2O | |
| B. | CH3CHBrCH3+NaOH$→_{△}^{乙醇}$CH3CH═CH2↑+NaBr+H2O | |
| C. | 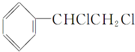 +2NaOH$→_{△}^{乙醇}$ +2NaOH$→_{△}^{乙醇}$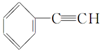 +2NaCl+2H2O +2NaCl+2H2O | |
| D. | 2CH3OH$→_{△}^{濃硫酸}$CH3-O-CH3+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 不同的原子 | B. | 同一元素的不同原子或離子 | ||
| C. | 不同元素的離子 | D. | 不同的元素 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com