
【題目】(1)下列敘述正確的有________。
A.蠶絲、棉花和羊毛的主要成分都是纖維素
B.我們平時吃的豆腐中主要含有蛋白質
C.“病毒感冒”的元兇是一種油脂
D.生物實驗室一般用質量分數為40%甲醛水溶液保存生物標本
(2)如果發現有人誤服重金屬鹽而出現了輕微中毒癥狀,需要馬上對病人進行搶救。
①你認為下列物質可以利用的有________。
A.碳酸鋇 B.豆漿 C.碘酒 D.熟雞蛋 E.酒精 F.生牛奶
②當你用所選物質對病人進行搶救以后,下一步的做法是________。
A.建議病人盡快去醫院治療
B.將病人安置于通風處呼吸新鮮的空氣
C.建議病人臥床休息
(3)血液中有一種含銅的呈藍色的蛋白質分子,其相對分子質量約為151000。已知該蛋白質分子中銅的質量分數為0.34%,平均每個該蛋白質分子中銅原子的個數為________。
【答案】BD BF A 8
【解析】
(1)棉花的主要成分是纖維素,蠶絲、羊毛、豆腐的主要成分是蛋白質,故A錯誤,B正確;病毒是蛋白質,C錯誤;40%甲醛水溶液可使蛋白質變性,可用于保存生物標本,D正確;故答案為:BD;
(2)①豆漿和生牛奶中含有較多的未變性的蛋白質,可以與重金屬鹽作用,從而降低其對人體的傷害,熟雞蛋中的蛋白質已經變性,不能與重金屬鹽作用,故答案為:BF;
②重金屬鹽中毒者服用生牛奶等雖然能降低重金屬鹽對人體的傷害,但不能完全消除,病人去醫院進行更有效的治療才是最佳選擇,故答案為:A;
(3) ![]() ,已知該蛋白質分子中銅的質量分數為0.34%,則Cu原子的個數為
,已知該蛋白質分子中銅的質量分數為0.34%,則Cu原子的個數為![]() ,故答案為:8。
,故答案為:8。


 小學學習好幫手系列答案
小學學習好幫手系列答案 小學同步三練核心密卷系列答案
小學同步三練核心密卷系列答案科目:高中化學 來源: 題型:
【題目】氯原子對O3的分解有催化作用:
O3+Cl=ClO+O2 ΔH1
ClO+O=Cl+O2 ΔH2
該反應的能量變化如圖所示,下列敘述中正確的是( )
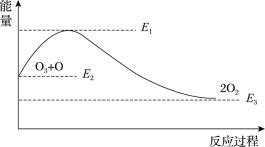
A.反應O3+O=2O2的ΔH=E1-E2
B.反應O3+O=2O2的ΔH=E2-E3
C.反應O3+O=2O2是吸熱反應
D.反應O3+O=2O2的ΔH=ΔH1+ΔH2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有單質A、B、C及化合物D、E、F、G、H,它們之間能發生如圖反應(圖中有些反應的產物和反應的條件沒有全部標出)。
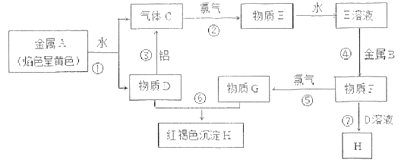
請根據以上信息回答下列問題:
(1)反應③是D物質的水溶液與金屬鋁反應,金屬鋁被氧化___(寫化學式);
(2)步驟⑦中剛生成的白色沉淀顏色會迅速發生變化,最終生成紅褐色沉淀H,請寫出由白色沉淀變成H的化學方程式:___;
(3)檢驗G中所含的金屬離子時,在G溶液中加入硫氰化鉀溶液,離子方程式為:___;
(4)工業上將氯氣通入D溶液中制取消毒液,反應的化學方程式為___,1mol氯氣發生反應,轉移電子___mol;消毒液中的有效成分是___(填名稱);
(5)將0.1molA的碳酸鹽溶液和0.15molE溶液混合,有如下兩種方式:
A.將含A的碳酸鹽溶液逐滴加入到E溶液中;
B.將E溶液逐滴加入到含A的碳酸鹽溶液中;
理論上產生氣體比較多的是___(填序號),多___mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,向20mL0.05mol·L-1的某稀酸H2B溶液中滴入0.1mol·L-1氨水,溶液中由水電離出氫離子濃度隨滴入氨水體積變化如圖。下列分析正確的是( )

A. NaHB溶液可能為酸性,也可能為堿性
B. A、B、C三點溶液的pH是逐漸減小,D、E、F三點溶液的pH是逐漸增大
C. E溶液中離子濃度大小關系:c(NH4+)>c(B2-)>c(OH-)>c(H+)
D. F點溶液c(NH4+)=2c(B2-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】辛烷(C8H18)是汽油的重要成分,其與O2反應的能量變化如圖所示。下列判斷正確的是
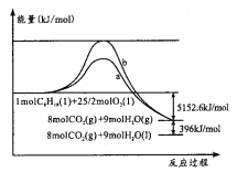
A. 曲線b代表加入催化劑時的能量變化
B. 反應物的總能量小于生成物的總能量
C. 表示辛烷燃燒熱的熱化學方程式:C8H18(l)+25/2O2(g)=8CO2(g)+9H2O(g) ΔH=-5152.6kJ/mol
D. 反應a、b的活化能不同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】配合物Fe(CO)5的熔點一20℃,沸點103℃。可用于制備純鐵。Fe(CO)5的結構如圖所示。

(1)基態Fe原子的價電子排布式是_____________________;Fe(CO)5晶體類型屬于__________晶體。
(2)CO分子中C、O原子都滿足8電子穩定結構,CO分子的結構式是________,寫出與CO互為等電子體的分子的電子式:___________________。
(3)C、O、Fe的第一電離能由大到小的順序為_______________________。
(4)關于Fe(CO)5,下列說法正確的是______。
A. Fe(CO)5是非極性分子,CO是極性分子 B. Fe(CO)5中Fe原子以sp3雜化方式與CO成鍵
C.1molFe(CO)5含有10mol配位鍵 D.Fe(CO)5==Fe+5CO反應中沒有新化學鍵生成
(5)鐵的三種晶體的晶胞均為立方晶胞,三種晶體的晶胞如下圖所示。

①上述三種晶體的晶胞中屬于面心晶胞的是______(填“a”“δ””或“γ”)-Fe。
②a-Fe晶胞中鐵原子的配位數為_______________。
③γ-Fe晶胞的邊長為apm,則γ-Fe單質的密度為____g/cm3(NA表示阿伏伽德羅常數的值,列出計算式即可)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氟碳鈰礦(主要成分為CeFCO3)是提取稀土化合物、冶煉鈰的重要礦物原料,以氟碳鈰礦為原料提取鈰的工藝流程如圖所示。
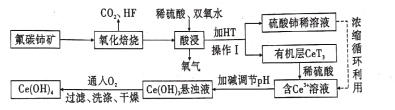
回答下列問題:
(l)CeFCO3中Ce的化合價為____ 。
(2)氧化培燒時不能使用陶瓷容器,原因是________.。
(3)氧化焙燒后的產物之一為CeO2.則酸浸時發生反應的離子方程式為____。
(4)HT是一種難溶于水的有機溶劑,則操作I的名稱為 _____。
(5)為了提高酸浸率,可以適當提高反應溫度,但溫度偏高浸出率反而會減小,其原因是____。
(6)有機物HT能將Ce3+從水溶液中萃取出來,該過程可表示為Ce3+(水層)+3HT(有機層) ![]() CeT3(有機層)+3H+(水層)。向CeT3(有機層)中加入稀硫酸能獲得較純的含Ce3+的水溶液,從平衡角度解釋其原因________。
CeT3(有機層)+3H+(水層)。向CeT3(有機層)中加入稀硫酸能獲得較純的含Ce3+的水溶液,從平衡角度解釋其原因________。
(7)寫出向Ce(OH)3懸濁液中通入氧氣得到產品Ce(OH)4的化學方程式:__________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碳酸亞乙酯是一種重要的添加劑,其結構簡式為![]() 。用環氧乙烷合成碳酸亞乙酯的反應為:
。用環氧乙烷合成碳酸亞乙酯的反應為: 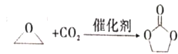 下列說法錯誤的是
下列說法錯誤的是
A.碳酸亞乙酯中的所有原子處于同一平面內B.碳酸亞乙酯的二氯代物只有兩種
C.上述反應屬于加成反應D.1 mol碳酸亞乙酯最多可消耗2 mol NaOH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于化學反應的描述中正確的是
A.需要加熱才能發生的反應一定是吸熱反應
B.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.3kJ/mol,則含40.0gNaOH的稀溶液與醋酸完全中和,放出57.3kJ的熱量
C.CO(g)的燃燒熱是283.0kJ/mol,則表示CO(g)的燃燒熱的熱方程式為2CO(g)+O2(g)=2CO2(g) △H=-283.0kJ/mol
D.已知2C(s)+2O2(g)=2CO2(g) △H=akJ/mol,2C(s)+O2(g)=2CO(g) △H=bkJ/mol,則b>a
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com