
【題目】元素R、X、T、Z、Q在元素周期表中的相對位置如下表所示,其中R單質在暗處與H2劇烈化合并發生爆炸。則下列判斷正確的是( )
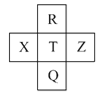
A.非金屬性:Z<T<X
B.R與Q的電子數相差26
C.氣態氫化物穩定性:R<T<Q
D.最高價氧化物的水化物的酸性:R>Q
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】有機物W用作調香劑、高分子材料合成的中間體等,制備W的一種合成路線如下。
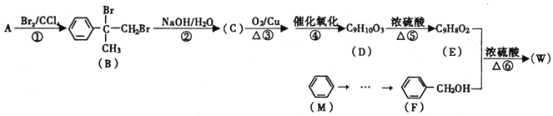
請回答下列問題:
(1)F的化學名稱是________,⑤的反應類型是________。
(2)E中含有的官能團是________(寫名稱),D聚合生成高分子化合物的結構簡式為________。
(3)將反應③得到的產物與O2在催化劑、加熱的條件下反應可得D,寫出反應④的化學方程式________。
(4)④、⑤兩步能否顛倒?________(填“能”或“否”)理由是________。
(5)與A具有含有相同官能團的芳香化合物的同分異構體還有________種(不含立體異構),其中核磁共振氫譜為六組峰,且峰面積之比為1:1:2:2:2:2的結構簡式為________。
(6)參照有機物W的上述合成路線,以M和CH3Cl為原料制備F的合成路線(無機試劑任選)________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 五種元素的原子結構,回答下列問題:
五種元素的原子結構,回答下列問題:
(1)只有![]() 層與
層與![]() 層的原子有______;
層的原子有______;
(2)含有![]() 層的原子有______;
層的原子有______;
(3)最外層電子數相同的原子有______;
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有四種元素的基態原子的電子排布式:
①![]() ; ②
; ②![]() ;
;
③![]() ; ④
; ④![]() 。
。
則下列有關比較中正確的是
A. 電負性:④>③>②>① B. 原子半徑:④>③>②>①
C. 第一電離能:④>③>②>① D. 最高正化合價:④>③=②>①
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,表中的字母分別代表一種化學元素。
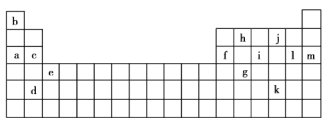
(1)a和c的I1大小關系是______大于______。(填字母)
(2)上述元素中,原子中未成對電子數最多的是______(填字母),寫出該元素基態原子的核外電子排布式:______。
(3)根據下表所提供的電離能數據,回答下列問題。
鋰 | X | Y | |
I1 | 520 | 496 | 580 |
I2 | 7296 | 4570 | 1820 |
I3 | 11799 | 6920 | 2750 |
I4 | 9550 | 11600 |
①表中X可能為以上13種元素中的______(填字母)元素。用元素符號表示![]() 和j形成的一種化合物的化學式:______。
和j形成的一種化合物的化學式:______。
②Y是周期表中第______族元素。
③以上13種元素中,______(填字母)元素原子失去核外第一個電子需要的能量最多。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示的各圖中,表示2A(g)+B(g)2C(g)(△H<0)這個可逆反應的正確圖象為(注:(C)表示C的質量分數,P表示氣體壓強,C表示濃度)
A. B.
B.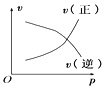 C.
C.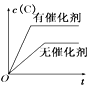 D.
D.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】綠礬(FeSO47H2O)在化學合成上用作還原劑及催化劑,工業上常用廢鐵屑溶于一定濃度的硫酸溶液制備綠礬。
(1)98% 1.84g/cm3的濃硫酸在稀釋過程中,密度下降,當稀釋至50%時,密度為1.4g/cm3,50%的硫酸物質的量濃度為______(保留兩位小數),50%的硫酸與30%的硫酸等體積混合,混合酸的濃度為______(填>、<、=)40%。
(2)實際生產用20%發煙硫酸(100克發煙硫酸含SO320克)配制稀硫酸,若用SO3nH2O表示20%的發煙硫酸,則n=______(保留兩位小數)。
(3)某廠廢水中含1.00×10﹣3mol/L的Cr2O72-,其毒性較大.某研究性學習小組為了變廢為寶,將廢水處理得到磁性材料Cr0.5Fe1.5FeO4 (Cr的化合價為+3,Fe的化合價依次為+3、+2).欲使1L該廢水中的Cr2O72-完全轉化為Cr0.5Fe1.5FeO4.理論上需要加入______g FeSO47H2O。
(4)硫酸亞鐵銨[(NH4)2SO4FeSO46H2O](俗稱莫爾鹽),較綠礬穩定,在分析化學中常用來配制Fe2+的標準溶液,用此Fe2+的標準溶液可以測定剩余稀硝酸的量.現取8.64克Cu2S和CuS的混合物用200mL2mol/L稀硝酸溶液處理,發生反應如下:
10NO3﹣+3Cu2S+16H+→6Cu2++10NO↑+3SO42﹣+8H2O
8NO3﹣+3CuS+8H+→3Cu2++3 SO42﹣+8NO↑+4H2O
剩余的稀硝酸恰好與48mL 2mol/L (NH4)2Fe(SO4)2溶液完全反應.
已知:NO3﹣+3Fe2++4H+→NO↑+3Fe3++2H2O
試計算混合物中CuS的質量分數(保留兩位小數)。______________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業合成是一個需要經歷多步反應的過程,我們常用的塑料包裝繩(主要成分為聚氯乙烯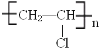 就是通過多步反應生產出來的。現在有1,2-二溴乙烷,氫氧化鈉醇溶液、二氧化錳、鋅粒、稀硫酸等主要原料,請您設計反應的步驟得到聚氯乙烯,將每一步反應的化學方程式寫出__________________________________
就是通過多步反應生產出來的。現在有1,2-二溴乙烷,氫氧化鈉醇溶液、二氧化錳、鋅粒、稀硫酸等主要原料,請您設計反應的步驟得到聚氯乙烯,將每一步反應的化學方程式寫出__________________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CO2和CH4在一定條件下合成乙酸:CO2+CH4![]() CH3COOH。完成下列填空:
CH3COOH。完成下列填空:
(1)①寫出碳原子最外電子層的軌道表示式______
②鈦(Ti)是22號元素,它是______(選填編號)
a.主族元素 b.副族元素 c.短周期元素 d.長周期元素
(2)CS2分子的電子式為______;其熔沸點比CO2高,原因是______常溫下,向1L pH=10的 NaOH溶液中持續通入CO2。通入CO2的體積(V)與溶液中水電離產生的OH﹣離子濃度(c)的關系如圖所示
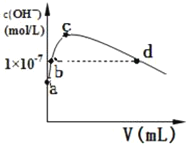
(3)c點溶液中離子濃度由大至小的關系是:______
(4)a點溶液中由水電離產生的c(H+)=______;b點溶液中c(H+)______1×10﹣7mol/L(填寫“等于”、“大于”或“小于”)
(5)能使0.1mol/L乙酸溶液的電離程度以及pH都增大的是______(選填序號)
a.加水稀釋 b.加入少量乙酸鈉固體 c.通氯化氫 d.加入少量苛性鈉固體
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com