
| A. | 0.1 mol | B. | 0.2 mol | C. | 0.3 mol | D. | 0.4 mol |
分析 堿式碳酸銅和稀硫酸反應生成硫酸銅、水和二氧化碳,所以加入0.05mol堿式碳酸銅[Cu2(OH)2CO3]相當于加入0.1molCuO、0.05molH2O,根據生成物知,陰極上銅離子和氫離子放電、陽極上氫氧根離子放電,根據銅和氫氣的物質的量與轉移電子之間的關系式計算轉移電子的物質的量.
解答 解:電解硫酸銅溶液后溶液呈酸性,向電解后的溶液中加入堿式碳酸銅能恢復原溶液,堿式碳酸銅和硫酸反應生成硫酸銅、水和二氧化碳,溶液質量增加的量是銅、氫氧根離子,所以實際上電解硫酸銅溶液分兩個階段:
第一階段2CuSO4+2H2O$\frac{\underline{\;電解\;}}{\;}$2Cu+O2↑+2H2SO4,
第二階段:2H2O$\frac{\underline{\;電解\;}}{\;}$2H2↑+O2↑,
將堿式碳酸銅化學式改變為2CuO•H2O•CO2,所以加入0.05molCu2(OH)2CO3 就相當于加入0.1molCuO和0.05mol水,
第一階段:根據銅原子守恒知,電解硫酸銅溶液析出n(Cu)=n(CuO)=0.1mol,轉移電子的物質的量=0.1mol×2=0.2mol;
第二階段:電解生成0.1mol水轉移電子的物質的量=0.05mol×2=0.1mol,
所以解過程中共轉移的電子數為0.2mol+0.1mol=0.3mol,
故選:C.
點評 本題考查了電解原理,為高頻考點,側重考查學生的分析能力和計算能力,明確實際上加入的物質是解本題關鍵,再根據原子守恒、轉移電子守恒來分析解答,難度中等.


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化學 來源: 題型:選擇題

| A. | 圖中膜為陰膜(只允許陰離子通過),OH-從右往左通過該膜 | |
| B. | 電解時,陰極電極反應式為:2H++2e-═H2↑ | |
| C. | 電解時,如有3mol電子通過導線,則一定生成0.6mol KIO3 | |
| D. | 電池總反應為:KI+3H2O $\frac{\underline{\;電解\;}}{\;}$KIO3+3H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 食鹽中加有碘,用其配成的溶液遇淀粉變藍 | |
| B. | 廁所清潔劑、食用醋、肥皂水、廚房清潔劑四種溶液的pH逐漸增大 | |
| C. | 使用氯氣自來水消毒時,氯氣會與自來水中的有機物反應,生成的有機氯化物可能對人有害 | |
| D. | 硅膠、生石灰、氯化鈣等都是食品包裝袋中常用的干燥劑. |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | -48.5kJ/mol | B. | +48.5kJ/mol | C. | -45.5kJ/mol | D. | +45.5kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入硝酸銀溶液產生白色沉淀,一定有Cl- | |
| B. | 加入碳酸鈉溶液產生白色沉淀,再加鹽酸白色沉淀消失,一定有Ba2+ | |
| C. | 加入氫氧化鈉溶液并加熱,產生的氣體能使濕潤紅色石蕊試紙變藍,一定有NH4+ | |
| D. | 加入氯化鋇溶液有白色沉淀產生,再加鹽酸,沉淀不消失,一定有SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

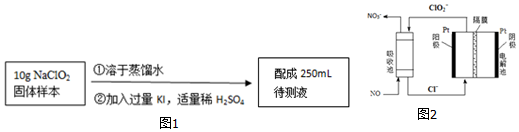
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com