
【題目】工業上,常采用氧化還原方法處理尾氣中的CO、NO。
方法1:氧化法。瀝青混凝土可作為反應:2CO(g)+O2(g)![]() 2CO2(g)的催化劑。圖甲表示在相同的恒容密閉容器、相同起始濃度、相同反應時間段下,使用同質量的不同瀝青混凝土(α型、β型)催化時,CO的轉化率與溫度的關系。
2CO2(g)的催化劑。圖甲表示在相同的恒容密閉容器、相同起始濃度、相同反應時間段下,使用同質量的不同瀝青混凝土(α型、β型)催化時,CO的轉化率與溫度的關系。
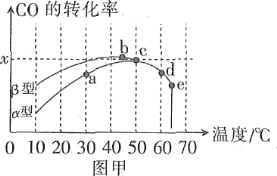
(1)在a、b、c、d四點中,未達到平衡狀態的是____。
(2)已知c點時容器中O2濃度為0.04mol·L-1,則50℃時,在α型瀝青混凝土中CO轉化反應的平衡常數K=____(用含x的代數式表示)。
(3)下列關于圖甲的說法正確的是____。
A.CO轉化反應的平衡常數K(a)<K(c)
B.在均未達到平衡狀態時,同溫下β型瀝青混凝土中CO轉化速率比α型要大
C.b點時CO與O2分子之間發生有效碰撞的幾率在整個實驗過程中最高
D.e點轉化率出現突變的原因可能是溫度升高后催化劑失去活性
方法2:還原法。某含鈷催化劑可以催化消除柴油車尾氣中的碳煙(C)和NOx。不同溫度下,將模擬尾氣(成分如表所示)以相同的流速通過該催化劑,測得所有產物(CO2、N2、N2O)與NO的相關數據結果如圖乙所示。
模擬尾氣 | 氣體(10 mol) | 碳煙 | ||
NO | O2 | He | ||
物質的量(mol) | 0.025 | 0.5 | 9.475 | n |
(4)375℃時,測得排出的氣體中含0.45molO2和0.052molCO2,則Y的化學式為____。
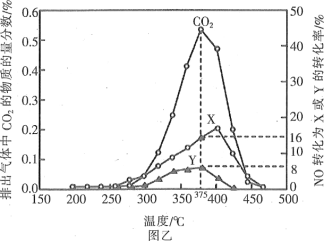
(5)實驗過程中采用NO模擬NOx,而不采用NO2的原因是____。
【答案】a ![]() BD N2 由于存在反應2NO2
BD N2 由于存在反應2NO2![]() N2O4會導致一定的分析誤差
N2O4會導致一定的分析誤差
【解析】
此題為化學平衡的綜合題,有判斷有計算,平衡的判斷和平衡常數的計算。圖像要根據橫縱坐標的意義和曲線的變化情況進行判斷。
(1)CO和O2反應是放熱反應,當達到平衡后升高溫度,CO的轉化率降低,所以,b、c、d點表示平衡狀態,a點對應的狀態是不平衡狀態。
(2)令CO起始濃度為a mol·L-1。
2CO(g)+O2(g)![]() 2CO2(g)
2CO2(g)
起始濃度(mol·L-1): a 0
轉化濃度(mol·L-1): ax ax
平衡濃度(mol·L-1):a(1-x) 0.04 ax
![]() 。
。
(3)CO和O2反應是放熱反應,a點未達到平衡,沒有平衡常數。若達到平衡后,溫度升高,平衡向左移動,平衡常數K減小,A項錯誤;觀察圖象知,β催化劑作用下CO的轉化速率大于α催化劑,B項正確;有效碰撞幾率與反應速率有關,溫度越高,反應速率越大,有效碰撞幾率越高,故在圖象中e點有效碰撞幾率最高,C項錯誤;催化劑需要一定活性溫度,轉化率出現突變,可能是因溫度高而催化劑失去活性,D項正確。故選BD。
(4)觀察圖象,NO生成X、Y的轉化率之和為24%,即NO參加反應的物質的量n(NO)=0.025mol×(16%+8%)=0.006 mol,根據原子守恒,X和Y的物質的量之和等于0.003mol。先根據O原子守恒求N2O的物質的量,再根據N守恒求N2的物質的量。
由投入各物質和排出各物質的物質的量知,
NO+C+O2→CO2+N2+N2O
物質的量:0.006 0.05 0.052 0.001 0.002
根據圖象,X的體積是Y的2倍。故Y為N2。
(5)NO2、N2O4共存,二者存在轉化平衡,用NO2模擬實驗會產生較大誤差。


 小天才課時作業系列答案
小天才課時作業系列答案 一課四練系列答案
一課四練系列答案 黃岡小狀元滿分沖刺微測驗系列答案
黃岡小狀元滿分沖刺微測驗系列答案 新輔教導學系列答案
新輔教導學系列答案科目:高中化學 來源: 題型:
【題目】依據反應:2Ag+(aq)+Cu(s)=Cu2+ (aq)+2Ag(s)設計的原電池如下圖所示。

請回答下列問題:
(1)電極X的材料是___________,電解質溶液Y是___________;
(2)銀電極為電池的___________極,發生的電極反應為___________;X電極上發生的電極反應為_________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】心腦血管疾病是一種致殘率高的疾病,由于沒有明顯的臨床癥狀,因而被稱為“沉默的疾病”,人類健康的第一殺手。下圖是合成一種治療心腦血管疾病藥物路線中的某一步驟,下列說法中正確的是( )
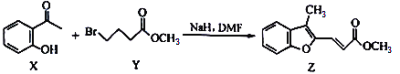
A. Y的分子式為C5H10BrO2
B. X的同分異構體中,含有苯環和羧基的結構共有4種
C. X中所有原子可能在同一平面上
D. 1mol Z最多可與6mol H2發生反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】由芳香烴X可合成多種在化工、醫藥等領域的物質,過程如下(部分產物、合成路線、反應條件略去)。其中A是一氯代物,H為聚合物。
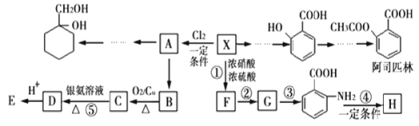
已知:
Ⅰ.芳香烴X的質譜圖如圖所示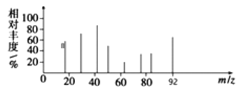
II.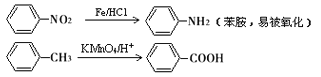
(1)X的分子式為______________,B的結構簡式為________________;
(2)阿司匹林中含氧官能團的名稱為__________________________;
(3)③的反應類型為___________;由A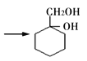 的過程中發生的反應為:苯環的加成反應→消去反應→加成反應→__________________;
的過程中發生的反應為:苯環的加成反應→消去反應→加成反應→__________________;
(4)反應④的化學方程式為____________________________________________;
(5)反應⑤的化學方程式為____________________________________________;
(6)![]() 的一種同系物
的一種同系物![]() 有多種同分異構體,其中符合下列要求的共有_____________種(不考慮立體異構);
有多種同分異構體,其中符合下列要求的共有_____________種(不考慮立體異構);
①能與NaHCO3反應放出CO2 ②能與FeCl3溶液發生顯色反應
寫出其中核磁共振氫譜為5組峰,且峰面積比為2:2:2:1:1的結構簡式__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“暖冰”是韓國首爾大學科學家將水置于一個足夠強的電場中,在20℃時,水分子瞬間凝固形成的.某老師在課堂上做了一個如圖所示的實驗,發現燒杯中酸性KMnO4溶液褪色.若將燒杯中的溶液換成含有少量KSCN的FeCl2溶液,則溶液呈血紅色.則下列說法中不正確的是( )
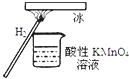
A. 在電場作用下,水分子間更易形成氫鍵,因而可以制得“暖冰”
B. 水凝固形成20℃時的“暖冰”所發生的變化是化學變化
C. 該條件下H2燃燒生成了既具有氧化性又具有還原性的物質
D. 該條件下H2燃燒的產物中可能含有一定量的H2O2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期元素X、Y、Z、W、Q在元素周期表中的相對位置如下圖。下列說法錯誤的是( )

A.X與Y對應的簡單氫化物的電子數相同B.W的最高價氧化物對應水化物的酸性比Q的強
C.X與Z的最高正化合價之和的數值等于8D.![]() 和
和![]() 的核外電子數和電子層數都相同
的核外電子數和電子層數都相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組物質中,滿足表中圖示物質在一定條件下,一步轉化關系的組合有( )
序號 | X | Y | Z | W |
|
① | Si | Na2SiO3 | H2SiO3 | SiO2 | |
② | Na | NaOH | Na2CO3 | NaCl | |
③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A.①②③B.①③C.②③D.①④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、W是原子序數依次增大的四種短周期元素,A、B、C、D、F都是由其中的兩種或三種元素組成的化合物,E是由Z元素形成的單質,0.1mol·L-1D溶液的pH為13(25℃)。它們滿足如圖轉化關系,則下列說法不正確的是

A. B晶體中陰、陽離子個數比為1:2
B. 等體積等濃度的F溶液與D溶液中,陰離子總的物質的量F>D
C. 0.1molB與足量A或C完全反應轉移電子數均為0.1NA
D. Y、Z分別形成的簡單氫化物的穩定性前者弱于后者,是因為后者分子間存在氫鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是中學化學實驗中常見的制備氣體并進行某些物質的檢驗和性質實驗的裝置,A是制備氣體的裝置,C、D、E、F中盛裝的液體可能相同,也可能不同。試回答:
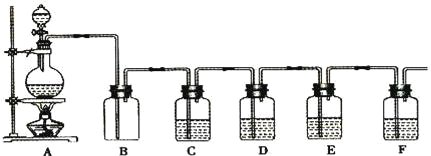
如果A中的固體物質是碳,分液漏斗中盛裝的是濃硫酸,試寫出發生的化學反應方程式:____,若要檢驗生成的產物,則B、C、D、E、F中應分別加入的試劑為__、__、__、__、__,E中試劑所起的作用__。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com