
主要實驗步驟:①準確稱取工業純堿試樣2.00 g;②用適量水配制成體積一定的溶液;③準確稱取一定量的所配試液,再用0.01 mol·L-1鹽酸標準滴定,測其總堿度。請回答以下問題:
(1)稱取固體工業純堿試樣時,為什么試樣取量盡量多些并且力求均勻?
____________________________________。
(2)在準確稱取純堿試樣后,為繼續進行實驗,除選用燒杯、玻璃棒、酸式滴定管、堿式滴定管、錐形瓶之外,還需要的儀器用品(試劑除外)有___________ 。
(3)在滴定操作中,應選用的指示劑是___________。
(4)假如所稱取的純堿試樣中,除含有2%的NaCl外,另外的雜質中只有NaHCO3,那么NaHCO3含量的大小對該試樣總堿度的測定值有何影響?
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
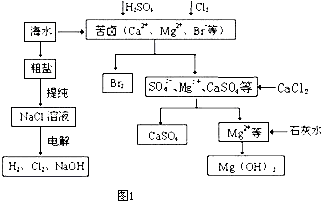
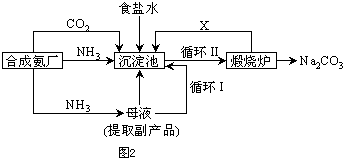
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化學 來源:模擬題 題型:填空題

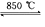 NaCl(l)+ K(g)。工業上應采用哪些措施才能使反應向正反應方向移動?___________________
NaCl(l)+ K(g)。工業上應采用哪些措施才能使反應向正反應方向移動?___________________ 查看答案和解析>>
科目:高中化學 來源:不詳 題型:問答題
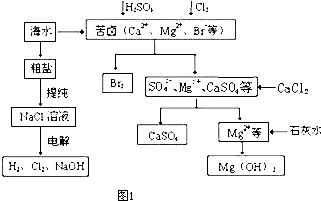
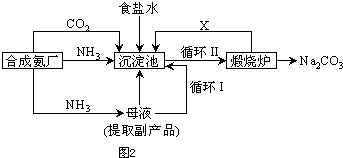
查看答案和解析>>
科目:高中化學 來源:2012-2013學年重慶市墊江實驗中學高二(上)期中化學試卷(解析版) 題型:解答題


 CO2+H2
CO2+H2查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com