
分析 (1)根據生成氨氣的物質的量,利用物質的量之比等于化學計量數之比計算參加反應的氮氣的物質的量,t時刻時氮氣的物質的量與參加反應的氮氣的物質的量之和為a的值;
(2)計算出混合氣體總的物質的量,利用體積分數計算氨氣的物質的量;
(3)原混合氣體的物質的量減去氮氣的物質的量為氫氣的物質的量,據此計算;
(4)計算出達到平衡時,N2和H2的轉化率,據此計算.
解答 解:(1)反應進行到t時,測的N2為3mol,NH3為6mol,由方程式可知,參加反應的氮氣的物質的量為6mol×$\frac{1}{2}$=3mol,故氮氣的起始物質的量為:13mol+3mol=16mol,即a=16,故答案為:16;
(2)反應達平衡時,混合氣體$\frac{716.8L}{22.4L/mol}$=32mol,其中NH3的物質的量為32mol×25%=8mol.
故答案為:8mol;
(3)利用差量法計算:
N2 (g)+3H2(g) 2NH3(g),物質的量減少△n
2NH3(g),物質的量減少△n
1mol 3mol 2mol 2mol
轉化:4mol 12mol 8mol 8mol
故原混合氣體為32mol+8mol=40mol,由(1)知a=16mol,則b=40mol-16mol=24mol,
反應達平衡時,混合氣體的體積為716.8L(標準狀況下),$\frac{716.8L}{22.4L/mol}$=32mol,原混合氣體與平衡混合氣體的壓強之比等于混合氣體物質的量之比,即p(始):p(平)=(a+b):32=40mol:32mol=5:4,
故答案為:5:4;
(4)達到平衡時,N2和H2的轉化率之比α(H2):α(N2)=$\frac{16mol}{4mol}$:$\frac{24mol}{12mol}$=2:1.
故答案為:2:1.
點評 本題考查化學平衡的計算,題目難度不大,注意利用三段式法結合化學方程式計算.


科目:高中化學 來源: 題型:選擇題
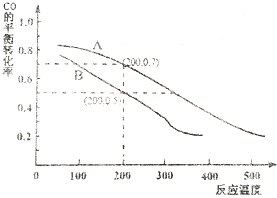
| A. | 保持其他條件不變,升高溫度,H2S濃度增加,表明該反應是吸熱反應 | |
| B. | 通入CO后,正反應速率逐漸增大 | |
| C. | 反應前H2S物質的量為7 mol | |
| D. | CO的平衡轉化率為80% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | HClO是弱酸,所以NaClO是弱電解質 | |
| B. | CCl4可用于鑒別溴水和碘水 | |
| C. | 漂白粉在空氣中不穩定,因此可用于漂白紙張 | |
| D. | 用乙醇萃取的方法可以分離溶于水的碘,是因為碘在乙醇中的溶解度較大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 鋅做負極發生氧化反應 | |
| B. | 供電時的總反應為:Zn+2H+═Zn2++H2↑ | |
| C. | 該裝置可實現化學能轉化為電能 | |
| D. | 產生1 g H2,消耗鋅的質量65 g |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向某溶液中滴加KSCN溶液,變為血紅色,則原溶液中含有Fe3+ | |
| B. | 向某溶液中滴加NaOH溶液,生成白色沉淀,繼而變為灰綠色,最終變為紅褐色,則原溶液中含有Fe2+ | |
| C. | 將淀粉和氯化鈉的混合溶液裝入半透膜中,將半透膜浸泡在盛有蒸餾水的燒杯中,為檢驗半透膜是否破損,可向蒸餾水中加入硝酸銀溶液來驗證 | |
| D. | 硫酸亞鐵溶液中,常放入一些鐵粉 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④⑥ | B. | ②③⑤ | C. | ①③④ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3.0 mol | B. | 1.5mol | C. | 1.0mol | D. | 0.75mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com