
【題目】密閉容器中發生如下反應:A(g)+3B(g)![]() 2C(g) ΔH<0,根據下列速率—時間圖像,回答下列問題。
2C(g) ΔH<0,根據下列速率—時間圖像,回答下列問題。
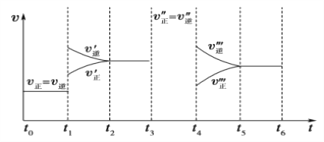
(1)下列時刻所改變的外界條件是:t1________;t4________;
(2)物質A的體積分數最大的時間段是_____;(時間段用t0~t1形式表示,下同)(3)反應速率最大的時間段是________。
(4)t0~t1、t3~t4、t5~t6時間段的平衡常數K0、K3、K5的關系___________。
科目:高中化學 來源: 題型:
【題目】下列敘述錯誤的是( )
A.酸、堿、鹽、氧化物在組成上的共同點是都含有非金屬元素
B.只含有一種元素的物質不一定都是純凈物
C.電離產生H+的化合物叫酸,其分子中氫原子的個數即是該酸的元數
D.壓強恒定時,氣體在水中的溶解度隨溫度的升高而降低
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某有機物X(C4H6O5)廣泛存在于許多水果內。該化合物具有如下性質:①1molX與足量金屬鈉反應產生1.5mol氣體;②在有濃硫酸和加熱條件下,X與醇或羧酸均反應生成有香味的產物;根據上述信息,對X的結構判斷正確的是
A. 含有碳碳雙鍵 B. 含有兩個羧基和一個羥基
C. 含有一個羧基和兩個羥基 D. 含有三個羥基和一個﹣COOR
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】歸納法是高中化學學習常用的方法之一,某化學研究性學習小組在學習了《化學反應原理》后作出了如下的歸納總結,其中正確的是
①常溫下,pH=3的醋酸溶液與pH=11的NaOH溶液等體積混合,則有c (Na+) + c(H+)=c(OH-) + c(CH3COO-)
②對已建立化學平衡的某可逆反應,當改變條件使化學平衡向正反應方向移動時,生成物的百分含量一定增加
③常溫下,AgCl在同物質的量濃度的CaCl2和NaCl溶液中的溶解度相同
④常溫下,已知醋酸電離平衡常數為Ka;醋酸根水解平衡常數為Kh;水的離子積為Kw;則有:Ka·Kh=Kw
⑤電解精煉銅時,電解質溶液中銅離子濃度不變 。
A.①④ B.①②④ C.①②④⑤ D.①②③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】能與NaOH溶液,新制Cu(OH)2懸濁液、純堿溶液、溴水、苯酚鈉、甲醇都起反應的是( )
A.CH3COOH B.CH2===CHCOOH
C.鹽酸 D.乙酸甲酯
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的是( )
A. 用金屬活動性順序可解釋反應:Na(l)+KCl(l)=NaCl(l)+K(g)
B. 水的電離是吸熱過程,升高溫度,水的離子積增大、pH減小
C. 對于平衡2HI(g)I2(g)+H2(g),壓縮容器體積,平衡不移動,氣體的顏色不變
D. 由反應SiO2+2C ![]() Si+2CO↑,可得出C的非金屬性強于Si
Si+2CO↑,可得出C的非金屬性強于Si
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面的排序不正確的是
A. 晶體熔點的高低: >
>
B. 硬度由大到小:金剛石>碳化硅>晶體硅
C. 熔點由高到低:Na>Mg>Al
D. 晶格能由大到小:NaF>NaCl>NaBr>NaI
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com