
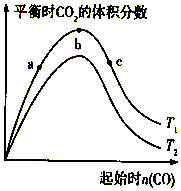
 燃煤脫硫可減少SO2尾氣的排放,燃煤脫硫技術受到各界科研人員的關注.一種燃煤脫硫技術的原理是:CaO(s)+3CO(g)+SO2(g)?CaS(s)+3CO2(g)△H=-394.0kJ/mol.保持其他條件不變,不同溫度下起始CO物質的量與平衡時體系中CO2的體積分數的關系如圖所示(T表示溫度):下列有關說法正確的是( )
燃煤脫硫可減少SO2尾氣的排放,燃煤脫硫技術受到各界科研人員的關注.一種燃煤脫硫技術的原理是:CaO(s)+3CO(g)+SO2(g)?CaS(s)+3CO2(g)△H=-394.0kJ/mol.保持其他條件不變,不同溫度下起始CO物質的量與平衡時體系中CO2的體積分數的關系如圖所示(T表示溫度):下列有關說法正確的是( )| A. | T1比T2高 | |
| B. | b點SO2轉化率最高 | |
| C. | b點后曲線下降是因CO體積分數升高 | |
| D. | 減小壓強可提高CO、SO2轉化率 |
分析 A、CaO(s)+3CO(g)+SO2(g)?CaS(s)+3CO2(g)△H=-394.0kJ/mol,正反應是放熱反應,溫度越高二氧化碳的含量越少;
B、增加一種反應物本身的轉化率降低,但另一種物質的轉化率升高;
C、一氧化碳的物質的量增加,導致一氧化碳體積分數變大,二氧化碳的體積分數減小;
D、CaO(s)+3CO(g)+SO2(g)?CaS(s)+3CO2(g)正反應是氣體體積縮小的反應;
解答 解:A、CaO(s)+3CO(g)+SO2(g)?CaS(s)+3CO2(g)△H=-394.0kJ/mol,正反應是放熱反應,溫度越高二氧化碳的含量越少,所以由圖可知T1比T2低,故A錯誤;
B、增加一種反應物本身的轉化率降低,但另一種物質的轉化率升高,所以b點二氧化硫的轉化率最低,而c點二氧化硫的轉化率最高,故B錯誤;
C、一氧化碳的物質的量增加,導致一氧化碳體積分數變大,二氧化碳的體積分數減小,所以b點后曲線下降是因CO體積分數升高,故C正確;
D、CaO(s)+3CO(g)+SO2(g)?CaS(s)+3CO2(g)正反應是氣體體積縮小的反應,所以增大壓強,平衡正向移動,則減小壓強可降低CO、SO2轉化率,故D錯誤;
故選C.
點評 本題考查平衡移動原理,難度中等,注意判斷曲線表示哪一物質的體積分數是關鍵,側重考查學生對圖象的分析與平衡移動的理解,難度較大.


科目:高中化學 來源: 題型:選擇題
| A. | 加入氯化鋇溶液產生白色沉淀,一定含有SO42- | |
| B. | 取溶液進行焰色反應是黃色,一定含有Na+ | |
| C. | 加入碳酸鈉溶液產生白色沉淀,一定含有Ca2+ | |
| D. | 加入稀鹽酸產生無色氣體,一定含有CO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
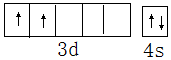
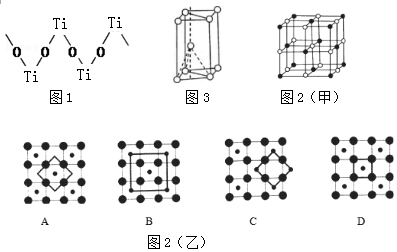
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
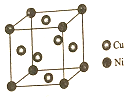 東晉《華陽國志南中志》卷四種已有關于白銅的記載,云南鎳白銅(銅鎳合金)文明中外,曾主要用于造幣,亦可用于制作仿銀飾品.回答下列問題:
東晉《華陽國志南中志》卷四種已有關于白銅的記載,云南鎳白銅(銅鎳合金)文明中外,曾主要用于造幣,亦可用于制作仿銀飾品.回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
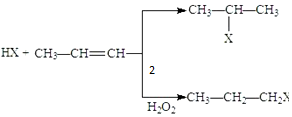 (X為鹵素原子)
(X為鹵素原子)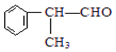 的物質,該物質是一種香料.
的物質,該物質是一種香料.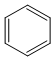 $→_{催化劑}^{①CH_{2}=CH-CH_{3}}$A$→_{一氯代物}^{②光照}$B$\stackrel{③}{→}$C$→_{HCl}^{④}$D$\stackrel{⑤}{→}$E$\stackrel{⑥氧化反應}{→}$
$→_{催化劑}^{①CH_{2}=CH-CH_{3}}$A$→_{一氯代物}^{②光照}$B$\stackrel{③}{→}$C$→_{HCl}^{④}$D$\stackrel{⑤}{→}$E$\stackrel{⑥氧化反應}{→}$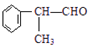
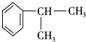 .
.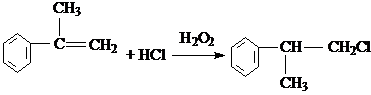 、2
、2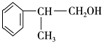 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O.
+2H2O.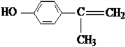 、
、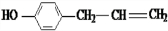 、
、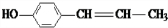 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com