(2013?廣東)銀銅合金廣泛用于航空工業.從切割廢料中回收銀并制備銅化工產品的工藝如下:
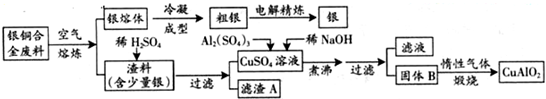
(注:Al(OH)
3和Cu(OH)
2開始分解的溫度分別為450℃和80℃)
(1)電解精煉銀時,陰極反應式為
Ag++e-=Ag
Ag++e-=Ag
;濾渣A與稀HNO
3反應,產生的氣體在空氣中迅速變為紅棕色,該氣體變色的化學方程式為
2NO+O2=2NO2
2NO+O2=2NO2
.
(2)固體混合物B的組成為
Al(OH)3和CuO
Al(OH)3和CuO
;在生成固體B的過程中,需控制NaOH的加入量,若NaOH過量,則因過量引起的反應的離子方程式為
Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
.
(3)完成煅燒過程中一個反應的化學方程式:
4
4
CuO+
2
2
Al
2O
3 4
4
CuAlO
2+
O2
O2
↑
(4)若銀銅合金中銅的質量分數為63.5%,理論上5.0kg廢料中的銅可完全轉化為
50.0
50.0
mol CuAlO
2,至少需要1.0mol?L
-1的Al
2(SO
4)
3溶液
25.0
25.0
L.
(5)CuSO
4溶液也可用于制備膽礬,其基本操作是
蒸發濃縮、冷卻結晶
蒸發濃縮、冷卻結晶
、過濾、洗滌和干燥.




 浙江名校名師金卷系列答案
浙江名校名師金卷系列答案
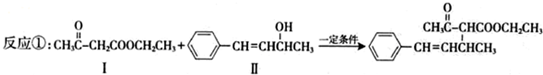
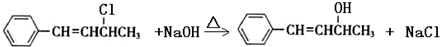
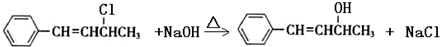
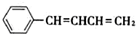
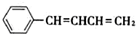
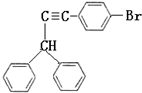
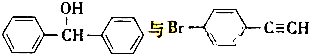 ,也可以發生類似反應①的反應,有機產物的結構簡式為
,也可以發生類似反應①的反應,有機產物的結構簡式為