
 含鋇化合物在實驗室和工業生產中都有廣泛的用途.
含鋇化合物在實驗室和工業生產中都有廣泛的用途.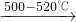 2BaO2.現有16.0噸的氧化鋇在足量的氧氣中加熱反應后,固體的質量變為17.6噸.那么實際參加反應的氧化鋇的質量為______噸.
2BaO2.現有16.0噸的氧化鋇在足量的氧氣中加熱反應后,固體的質量變為17.6噸.那么實際參加反應的氧化鋇的質量為______噸.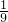 ,求該反應條件下混合氣體的平均式量?
,求該反應條件下混合氣體的平均式量?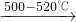 2BaO2
2BaO2 =15.3噸
=15.3噸 =2.117g,20℃時,Ba(OH)2飽和溶液的質量分數為
=2.117g,20℃時,Ba(OH)2飽和溶液的質量分數為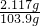 =0.02,
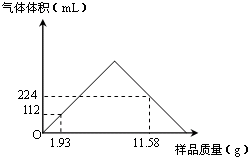
=0.02,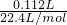 =0.005mol,根據碳原子守恒可知碳酸鋇的物質的量為0.005mol,故11.58g混合物中含有的碳酸鋇的物質的量為0.005mol×
=0.005mol,根據碳原子守恒可知碳酸鋇的物質的量為0.005mol,故11.58g混合物中含有的碳酸鋇的物質的量為0.005mol×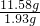 =0.03mol,故11.58g樣品中BaCO3的質量為0.03mol×197g/mol=5.91g,
=0.03mol,故11.58g樣品中BaCO3的質量為0.03mol×197g/mol=5.91g,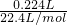 =0.01mol,故生成二氧化碳消耗的鹽酸的物質的量為0.01mol×2=0.02mol,與氫氧化鋇反應消耗的鹽酸的物質的量為0.08L×1mol/L-0.02mol=0.06mol,故氫氧化鈉晶體的物質的量為0.06mol×
=0.01mol,故生成二氧化碳消耗的鹽酸的物質的量為0.01mol×2=0.02mol,與氫氧化鋇反應消耗的鹽酸的物質的量為0.08L×1mol/L-0.02mol=0.06mol,故氫氧化鈉晶體的物質的量為0.06mol× =0.03mol,故0.03×(171+18n)=5.57,解得n=1,
=0.03mol,故0.03×(171+18n)=5.57,解得n=1, =2mol,故混合物水的物質的量為9mol-1mol-2mol=6mol,故混合氣體的平均相對分子質量為
=2mol,故混合物水的物質的量為9mol-1mol-2mol=6mol,故混合氣體的平均相對分子質量為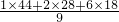 =23.11,
=23.11, ,故混合氣體中二氧化碳與CO的物質的量之比為0.94×
,故混合氣體中二氧化碳與CO的物質的量之比為0.94× :0.02=47:3,轉化的甲烷物質的量為2.0×106 mol×95%,由碳元素守恒可知,二氧化碳、CO的總的物質的量為2.0×106 mol×95%,故二氧化碳為2.0×106 mol×95%×
:0.02=47:3,轉化的甲烷物質的量為2.0×106 mol×95%,由碳元素守恒可知,二氧化碳、CO的總的物質的量為2.0×106 mol×95%,故二氧化碳為2.0×106 mol×95%×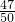 ,CO物質的量為2.0×106 mol×95%×
,CO物質的量為2.0×106 mol×95%× ,結合方程式可知生成BaS的物質的量為2.0×106 mol×95%×
,結合方程式可知生成BaS的物質的量為2.0×106 mol×95%×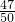 +2.0×106 mol×95%×
+2.0×106 mol×95%× ×
×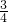 =2.0×106×95%×
=2.0×106×95%× mol,故生成BaS的質量為2.0×106×95%×
mol,故生成BaS的質量為2.0×106×95%× mol×169g/mol=316.28×106 g=316.28噸,
mol×169g/mol=316.28×106 g=316.28噸, 計算二氧化碳的物質的量,根據碳原子守恒計算碳酸鋇的物質的量,根據定組成計算11.58g混合物中含有的碳酸鋇的物質的量,進而根據m=nM計算碳酸鋇的質量;
計算二氧化碳的物質的量,根據碳原子守恒計算碳酸鋇的物質的量,根據定組成計算11.58g混合物中含有的碳酸鋇的物質的量,進而根據m=nM計算碳酸鋇的質量; 計算二氧化碳的物質的量,計算生成二氧化碳消耗的鹽酸的物質的量,進而計算與氫氧化鋇反應消耗的鹽酸的物質的量,可得氫氧化鈉晶體的物質的量,進而計算氫氧化鋇晶體中n的值;
計算二氧化碳的物質的量,計算生成二氧化碳消耗的鹽酸的物質的量,進而計算與氫氧化鋇反應消耗的鹽酸的物質的量,可得氫氧化鈉晶體的物質的量,進而計算氫氧化鋇晶體中n的值; =
= 計算;
計算; ,據此計算混合氣體中二氧化碳與CO的物質的量之比,根據轉化的甲烷計算二氧化碳、CO的物質的量,結合方程式計算BaS的物質的量,進而計算其質量.
,據此計算混合氣體中二氧化碳與CO的物質的量之比,根據轉化的甲烷計算二氧化碳、CO的物質的量,結合方程式計算BaS的物質的量,進而計算其質量.

 同步輕松練習系列答案
同步輕松練習系列答案 課課通課程標準思維方法與能力訓練系列答案
課課通課程標準思維方法與能力訓練系列答案湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com