
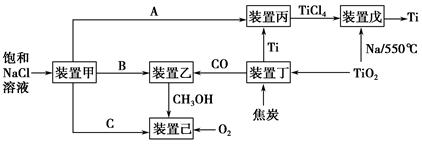
| 溫度/℃ | 250 | 350 |
| K | 2.041 | x |
| | c(CO) | c(H2) | c(CH3OH) |
| 0 min | 0.8 mol·L-1 | 1.6 mol·L-1 | 0 |
| 2 min | 0.6 mol·L-1 | y | 0.2 mol·L-1 |
| 4 min | 0.3 mol·L-1 | 0.6 mol·L-1 | 0.5 mol·L-1 |
| 6 min | 0.3 mol·L-1 | 0.6 mol·L-1 | 0.5 mol·L-1 |
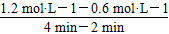 =0.3 mol·L-1·min-1;4 min時,反應達到平衡,故CO的轉化率為
=0.3 mol·L-1·min-1;4 min時,反應達到平衡,故CO的轉化率為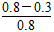 ×100%=62.5%;0~2 min的反應速率比2~4 min的反應速率小,故2 min時可能使用了催化劑。
×100%=62.5%;0~2 min的反應速率比2~4 min的反應速率小,故2 min時可能使用了催化劑。

 陽光同學一線名師全優好卷系列答案
陽光同學一線名師全優好卷系列答案科目:高中化學 來源:不詳 題型:單選題
| CaAl2Si2O8 | + | Mg2SiO4 | ? | CaMg2Al2Si3O12 | |
| (鈣長石) | (鎂橄欖石) | (鈣鎂)石榴子石 | |||
| 摩爾質量(g/mol) | 278 | 140.6 | 413.6 | ||
| 密度(g/cm3) | 2.70 | 3.22 | 3.50 |
| A.鈣長石生成 | B.鎂橄欖石生成 |
| C.鈣長石和鎂橄欖石共存 | D.(鈣鎂)石榴子石生成 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 C(g) + D(g)的平衡常數K值與溫度的關系如表所示。830℃時,向一個2 L的密閉容器中充入0.20 mol A和0.20 mol B,10 s時達平衡。下列說法不正確的是
C(g) + D(g)的平衡常數K值與溫度的關系如表所示。830℃時,向一個2 L的密閉容器中充入0.20 mol A和0.20 mol B,10 s時達平衡。下列說法不正確的是| 溫度/℃ | 700 | 830 | 1200 |
| K值 | 1.7 | 1.0 | 0.4 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.一定溫度下,反應MgCl2(l)=Mg(l)+Cl2(g)的ΔH<0ΔS>0 |
B.水解反應NH4++H2O NH3·H2O+H+達到平衡后,升高溫度平衡逆向移動 NH3·H2O+H+達到平衡后,升高溫度平衡逆向移動 |
| C.鉛蓄電池放電時的負極和充電時的陽極均發生還原反應 |
| D.對于反應2H2O2=2H2O+O2↑,加入MnO2或升高溫度都能加快O2的生成速率 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 CH3OH(g),其他條件不變,在300 ℃和500 ℃時,甲醇物質的量n(CH3OH)反應時間t的變化曲線如圖所示,下列說法正確的是( )
CH3OH(g),其他條件不變,在300 ℃和500 ℃時,甲醇物質的量n(CH3OH)反應時間t的變化曲線如圖所示,下列說法正確的是( )| A.該反應的ΔH>0 |
B.其他條件不變,升高溫度反應的平衡常數增大 |
C.300 ℃時,0~t1 min內 CH3OH的平均生成速率為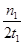 mol·L-1·min-1 mol·L-1·min-1 |
D.A點的反應體系從300 ℃升高到500 ℃,達到平衡時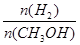 減小 減小 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 Fe(s)+CO2(g) ΔH>0。已知在1 100 ℃時,該反應的化學平衡常數K=0.263。
Fe(s)+CO2(g) ΔH>0。已知在1 100 ℃時,該反應的化學平衡常數K=0.263。 CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,現向體積為1 L的密閉容器中,充入1 mol CO2和3 mol H2,反應過程中測得CO2和CH3OH(g)的濃度隨時間的變化如圖所示。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,現向體積為1 L的密閉容器中,充入1 mol CO2和3 mol H2,反應過程中測得CO2和CH3OH(g)的濃度隨時間的變化如圖所示。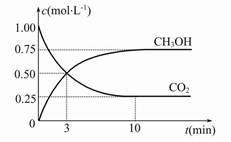
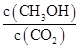 增大的是 (填符號)。
增大的是 (填符號)。| A.升高溫度 | B.再充入H2 | C.再充入CO2 | D.將H2O(g)從體系中分離 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
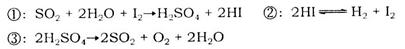
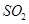 b.
b. c.
c.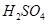 d.HI
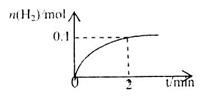
d.HI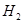 的物質的量隨時間的變化如圖所示。0~2min內的平均反應速率
的物質的量隨時間的變化如圖所示。0~2min內的平均反應速率 _________。
_________。
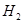 的體積分數
的體積分數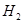 ,反應時溶液中水的電離平衡______移動(選填“向左”、“向右”或“不”);若加入少量下列試劑中的_____(選填編號),產生
,反應時溶液中水的電離平衡______移動(選填“向左”、“向右”或“不”);若加入少量下列試劑中的_____(選填編號),產生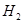 的速率將增大。
的速率將增大。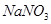 b.
b.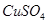 c.
c. d.
d.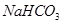
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
| | N2+3H2 2NH3 2NH3 | |||
| 溫度 | 25℃ | 200℃ | 400℃ | 600℃ |
| 平衡常數K | 5×108 | 650 | 0.507 | 0.01 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
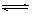 C(g)+D(g),在不同溫度下,D的物質的量n(D)和時間t的關系如圖。
C(g)+D(g),在不同溫度下,D的物質的量n(D)和時間t的關系如圖。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com