
【題目】實驗室用O2氧化NH3制備硝酸的裝置如圖所示(夾持裝置略),下列說法不正確的是

A.球形干燥管B中可以填充堿石灰或五氧化二磷
B.實驗過程中,若熄滅酒精燈,裝置C中的氧化鉻繼續保持紅熱,說明裝置C中的反應放熱
C.球形干燥管D中的無水氯化鈣可吸收尾氣中的氨氣和水蒸氣
D.裝置E中的石蕊試液最終變紅,說明錐形瓶中有硝酸產生
 新思維假期作業寒假吉林大學出版社系列答案
新思維假期作業寒假吉林大學出版社系列答案科目:高中化學 來源: 題型:
【題目】環氧乙烷(![]() )是一種最簡單的環醚,常用于有機合成。某研究小組以環氧乙烷和甲苯為原料按下列流程合成有機化合物G和I。
)是一種最簡單的環醚,常用于有機合成。某研究小組以環氧乙烷和甲苯為原料按下列流程合成有機化合物G和I。
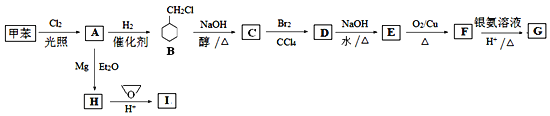
已知:CH3Cl CH3MgCl
CH3MgCl CH3CH2CH2OH
CH3CH2CH2OH
回答下列問題:
(1)A分子中最多有_____個原子共平面。
(2)D的結構簡式為_____。
(3)寫出下列反應的化學方程式:
E→F:______;G和I在濃硫酸催化下生成酯:______。
(4)I有多種同分異構體,寫出其中滿足以下條件的同分異構體的結構簡式:_______。
①屬于芳香族化合物; ② 能與FeCl3溶液發生顯色反應;
③核磁共振氫譜顯示不同環境的氫原子個數比1:2:3:6
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溴乙烷在不同溶劑中與NaOH反應生成不同的產物,同學們據此展開探究。
(實驗1)甲同學利用如圖所示裝置進行實驗:
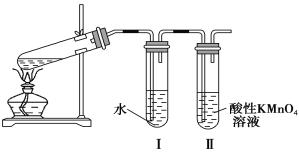
(1)甲同學的實驗目的為____________________________。
(2)實驗過程中可觀察到試管Ⅱ中的現象為__________________________________________________。
(3)試管Ⅰ的作用為_________________________________________________________。
(實驗2)乙同學在試管中加入3 mL溴乙烷和3 mL NaOH溶液,振蕩,加熱。
(4)此反應的化學方程式為_________________________________________。
(5)停止加熱并冷卻后,欲證明確實發生了上述反應,還應進行的操作為_____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與生產、生活密切相關,下列說法不正確的是( )
A. 用報紙包裝食物屬于資源的充分利用,應以提倡。
B.  是礦泉水瓶、飲料瓶底的常見標志,表示可回收利用,只能一次性使用,不能長期使用。
是礦泉水瓶、飲料瓶底的常見標志,表示可回收利用,只能一次性使用,不能長期使用。
C. 具有吸水性的植物纖維加工后可用作食品干燥劑。
D. 防偽熒光油墨由顏料與樹脂連接料等制成,其中樹脂屬于有機高分子材料。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組中的兩種物質互為同分異構體的有
①乙醇和二甲醚 ②正丁烷和異丁烷 ③金剛石和富勒烯 ④![]() 和
和![]() ⑤蔗糖和麥芽糖 ⑥蛋白質和氨基酸
⑤蔗糖和麥芽糖 ⑥蛋白質和氨基酸
A.③④⑥B.①②④C.①②⑤D.③⑤⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二氧化碳的捕捉、封存與再利用是實現溫室氣體減排的重要途徑之一。
(1)二氧化碳的電子式為___________。
(2)下列利用二氧化碳的反應中原子利用率達100%的是_____(填序號)。
a.CO2+2NH3 ![]() CO(NH2)2+H2O
CO(NH2)2+H2O
b.CO2+CH4![]() CH3COOH
CH3COOH
c.CO2+3H2![]() CH3OH+H2O
CH3OH+H2O
d.
(3)一種正在開發的利用二氧化碳制取甲醇的流程如下:

①反應(Ⅰ)將CO2和H2O轉化為甲酸常用途徑有兩種,如下圖(a)和 (b)。

圖(a)中能量主要轉化方式為____,圖(b)中發生反應的化學方程式為_____。
②在5L的恒溫恒容密閉容器中充入1moLCO和4molH2,加入催化劑發生反應,測得CO及CH3OH的物質的量隨時間變化如下圖所示。

圖中第______min(填數字)反應達到平衡,CO在0~4min內的平均反應速率比在4~8min內的快,其原因是______;達到平衡時氫氣的濃度為______。
(4)已知斷裂(或生成)1mol化學鍵吸收(或放出)的能量稱為鍵能,反應H2(g)+ I2(g)=2HI(g)相關鍵能數據如下:
化學鍵 | H—I | H—H | I—I |
鍵能/kJ·mol-1 | 298.7 | 436.0 | 152.7 |
則該反應的△H為_________kJ·mol-1。
(5)氨氣可作為脫硝劑,在恒溫恒容密閉容器中充入一定量的NO和NH3,在一定條件下發生反應:6NO(g) + 4NH3(g) ![]() 5N2(g) +6H2O(g)。
5N2(g) +6H2O(g)。
①能說明該反應已達到平衡狀態的標志是_________(不定項選擇)。
a.反應速率v( NH3) =v( N2)
b.容器內壓強不再隨時間而發生變化
c.容器內N2的物質的量分數不再隨時間而發生變化
d.容器內n(NO)∶n(NH3)∶n(N2)∶n(H2O) = 6∶4∶5∶6
②某次實驗中測得容器內NO及N2的物質的量隨時間變化如下圖所示,圖中v(正)與v(逆)相等的點為______(選填字母)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】磷酸是重要的化學試劑和工業原料。請回答下列問題:
(1)已知:25℃時,磷酸和氫氟酸的電離常數如下表所示。
物質 | H3PO4 | HF |
電離常數 | Ka1=7.1×103; Ka2=6.3×108; Ka3=4.2×1013 | Ka=6.6×104 |
向NaF溶液中滴加少量H3PO4溶液,反應的離子方程式為____________
(2)已知:
Ⅰ.CaO(s)+H2SO4(l)![]() CaSO4(s)+H2O(l) ΔH=-271kJ·mol1
CaSO4(s)+H2O(l) ΔH=-271kJ·mol1
Ⅱ.5CaO(s)+3H3PO4(l)+HF(g)![]() Ca5(PO4)3F(s)+5H2O(l) ΔH=-937kJ·mol1
Ca5(PO4)3F(s)+5H2O(l) ΔH=-937kJ·mol1
則:①工業上用Ca5(PO4)3F和硫酸反應制備磷酸的熱化學方程式為____________。
②一定條件下,在密閉容器中只發生反應Ⅱ,達到平衡后縮小容器容積,HF的平衡轉化率________(填“增大”“減小”或“不變”,下同);HF的平衡濃度________。
(3)工業上用磷尾礦制備Ca5(PO4)3F時生成的副產物CO可用于制備H2,原理為CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH。
CO2(g)+H2(g) ΔH。
①一定溫度下,向10L密閉容器中充入0.5mol CO和1mol H2O(g),2min達到平衡時,測得0~2min內用CO2表示的反應速率v(CO2)=0.02mol·L1·min1。則CO的平衡轉化率α=________;該反應的平衡常數K=________。
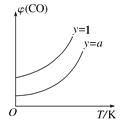
②在壓強不變的密閉容器中發生上述反應,設起始的![]() =y,CO的平衡體積分數(φ)與溫度(T)的關系如圖所示。則:該反應的ΔH___0(填“>”“<”或“=”,下同)。a_____1,理由為_____________
=y,CO的平衡體積分數(φ)與溫度(T)的關系如圖所示。則:該反應的ΔH___0(填“>”“<”或“=”,下同)。a_____1,理由為_____________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對大量盆栽鮮花施用了S﹣誘抗素制劑,以保持鮮花盛開,S﹣誘抗素的分子結構如圖,下列關于該分子的說法中正確的是( )
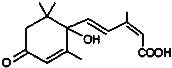
A. 含有碳碳雙鍵、羥基、醛基、羧基
B. 能發生加成反應、氧化反應、取代反應、縮聚反應
C. 1mol該分子能與含2mol NaOH的溶液完全反應
D. 該分子能與溴水反應而使溴水褪色且1mol它能與溴水中的4mol Br2反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:常溫下, ![]() 。現有1L 0.1mol·L-1的兩種溶液:①NaClO溶液;② NaF溶液。下列說法正確的是
。現有1L 0.1mol·L-1的兩種溶液:①NaClO溶液;② NaF溶液。下列說法正確的是
A. c(H+):①>②
B. 分別加入1L 0.1mol·L-1HCl溶液后,兩溶液的pH:①<②
C. 分別加入等濃度的鹽酸至溶液呈中性,消耗鹽酸的體積:①<②
D. n(HF)+n(F-)=n(HClO)+n(ClO-)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com