
| A. | 7.1g C12與足量NaOH溶液反應轉移的電子數為0.2NA | |
| B. | 46 g NO2 和 N2O4混合氣體中含有原子數為3NA | |
| C. | 1mol Na2O2 固體中含離子總數為4NA | |
| D. | 標準狀況下,2.24L辛烷所含分子數為0.1NA |
分析 A、求出氯氣的物質的量,然后根據氯氣和堿的反應為歧化反應來分析;
B、NO2 和 N2O4的最簡式均為NO2;
C、過氧化鈉由2個鈉離子和1個過氧根構成;
D、標況下辛烷為液態.
解答 解:A、7.1g氯氣的物質的量為0.1mol,而氯氣和堿的反應為歧化反應,故0.1mol氯氣轉移0.1NA個電子,故A錯誤;
B、NO2 和 N2O4的最簡式均為NO2,故46g混合物中含有的NO2的物質的量為1mol,故含3NA個原子,故B正確;
C、過氧化鈉由2個鈉離子和1個過氧根構成,故1mol過氧化鈉中含3mol離子即3NA個,故C錯誤;
D、標況下辛烷為液態,故不能根據氣體摩爾體積來計算其物質的量,故D錯誤.
故選B.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:多選題
| 選項 | 實驗操作 | 實驗目的或結論 |
| A | 用硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液變黃色 | 氧化性:H2O2>Fe3+ |
| B | 向盛有Fe(NO3)2溶液的試管中加入1mol/LH2SO4 | 若試管口出現紅棕色氣體,說明NO3-被Fe2+還原為NO |
| C | 淀粉碘化鉀溶液久置顯藍色 | 是由于I-被還原,析出的I2溶于溶液中 |
| D | 向含有少量的FeBr3的FeCl3溶液中,加入適量氯水,再加CCl4萃取分液 | 除去FeCl3溶液中的FeBr3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 無色溶液:Ca2+、Na+、Cl-、HCO3- | |
| B. | 能使pH試紙呈紅色的溶液:Na+、NH4+、I-、NO3- | |
| C. | 水電離出的c(H+)=10-13mol•L-1的溶液中:K+、Na+、SO42-、AlO2- | |
| D. | 有較多Fe3+的溶液中:Na+、NH4+、SCN-、HCO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 合金材料中可能含有非金屬元素 | |
| B. | 燃燒化石燃料排放的廢氣中含大量CO2、SO2造成大氣污染,使雨水pH=5.6,形成酸雨 | |
| C. | 廢棄的玻璃、金屬、紙制品是可回收利用的資源 | |
| D. | 用CO2合成聚碳酸酯可降解塑料,實現“碳”的循環利用 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | +3 | B. | +4 | C. | +5 | D. | +6 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cl2O7、P2O5、SO3、CO2、NO2均屬于酸性氧化物 | |
| B. | K2O、K2O2、KO2為相同元素組成的金屬氧化物,都屬于堿性氧化物 | |
| C. | 根據能否發生丁達爾效應,可以區分膠體和溶液 | |
| D. | 根據溶液導電能力強弱,將電解質分為強電解質、弱電解質 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗目的 | 試劑及方法 |
| 證明炭粉中含有CuO | |
| 鑒別MgCl2和AlCl3溶液 | |
| 分離Na2SO4和CaCO3固體混合物 | |
| 除去NaHCO3溶液中混有的Na2CO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
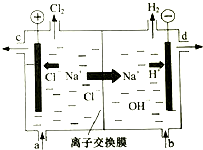 工業中的氯堿工業是離子交換膜法電解精制飽和食鹽水如下圖,離子交換膜只允許陽離子通過.
工業中的氯堿工業是離子交換膜法電解精制飽和食鹽水如下圖,離子交換膜只允許陽離子通過.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
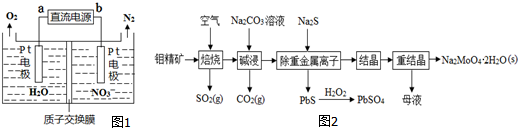
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com