
科目:高中化學 來源: 題型:



| ||
| ||
 2BO3,在一個固定容積為2L的密閉容器中充入0.20mol的BO2和0.10mol的O2,半分鐘后達到平衡,測得容器中含BO3為0.18mol,則v(o2 )=
2BO3,在一個固定容積為2L的密閉容器中充入0.20mol的BO2和0.10mol的O2,半分鐘后達到平衡,測得容器中含BO3為0.18mol,則v(o2 )=查看答案和解析>>
科目:高中化學 來源:寧夏自治區模擬題 題型:推斷題

(1)寫出F的電子式____________。
(2)氣體H有毒,可用Na2CO3溶液吸收,生成兩種酸式鹽,該反應的化學方程式為:________________。
(3)加熱E的水溶液后并灼燒,最終得到的固體為____________, 原因為_______________, ____________。(用化學反應方程式來表示)
(4)室溫下,向F的水溶液中加入等體積等濃度的鹽酸反應后所得溶液的PH>7,則此溶液中離子濃度由小到大的順序為:_______________。
(5)將氣體H放在空氣中充分燃燒可得到氣體氧化物BO2,BO2可與氧氣繼續反應:2BO2+O2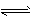 2BO3,在一個固定容積為2L的密閉容器中充入0.20 mol的BO2和0.10mol的O2,半分鐘后達到平衡,測得容器中含BO3為0.18mol,則
2BO3,在一個固定容積為2L的密閉容器中充入0.20 mol的BO2和0.10mol的O2,半分鐘后達到平衡,測得容器中含BO3為0.18mol,則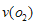 = ________ mol·L-1·min-1。若繼續通入0.20mol BO2和0.10mol O2,再次達到新平衡后,BO3的物質的量介于__________之間。
= ________ mol·L-1·min-1。若繼續通入0.20mol BO2和0.10mol O2,再次達到新平衡后,BO3的物質的量介于__________之間。
查看答案和解析>>
科目:高中化學 來源:湖北省模擬題 題型:推斷題

(1)寫出F的電子式____________。
(2)氣體H有毒,可用Na2CO3溶液吸收,生成兩種酸式鹽,該反應的化學方程式為:________________。
(3)加熱E的水溶液后并灼燒,最終得到的固體為____________, 原因為_______________, ____________。(用化學反應方程式來表示)
(4)室溫下,向F的水溶液中加入等體積等濃度的鹽酸反應后所得溶液的PH>7,則此溶液中離子濃度由小到大的順序為:_______________。
(5)將氣體H放在空氣中充分燃燒可得到氣體氧化物BO2,BO2可與氧氣繼續反應:2BO2+O2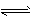 2BO3,在一個固定容積為2L的密閉容器中充入0.20 mol的BO2和0.10mol的O2,半分鐘后達到平衡,測得容器中含BO3為0.18mol,則
2BO3,在一個固定容積為2L的密閉容器中充入0.20 mol的BO2和0.10mol的O2,半分鐘后達到平衡,測得容器中含BO3為0.18mol,則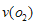 = ________ mol·L-1·min-1。若繼續通入0.20mol BO2和0.10mol O2,再次達到新平衡后,BO3的物質的量介于__________之間。
= ________ mol·L-1·min-1。若繼續通入0.20mol BO2和0.10mol O2,再次達到新平衡后,BO3的物質的量介于__________之間。
查看答案和解析>>
科目:高中化學 來源:福建省月考題 題型:推斷題

(1)寫出F的電子式____________。
(2)氣體H有毒,可用Na2CO3溶液吸收,生成兩種酸式鹽,該反應的化學方程式為:________________。
(3)加熱E的水溶液后并灼燒,最終得到的固體為____________, 原因為_______________, ____________。(用化學反應方程式來表示)
(4)室溫下,向F的水溶液中加入等體積等濃度的鹽酸反應后所得溶液的PH>7,則此溶液中離子濃度由小到大的順序為:_______________。
(5)將氣體H放在空氣中充分燃燒可得到氣體氧化物BO2,BO2可與氧氣繼續反應:2BO2+O2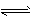 2BO3,在一個固定容積為2L的密閉容器中充入0.20 mol的BO2和0.10mol的O2,半分鐘后達到平衡,測得容器中含BO3為0.18mol,則
2BO3,在一個固定容積為2L的密閉容器中充入0.20 mol的BO2和0.10mol的O2,半分鐘后達到平衡,測得容器中含BO3為0.18mol,則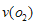 = ________ mol·L-1·min-1。若繼續通入0.20mol BO2和0.10mol O2,再次達到新平衡后,BO3的物質的量介于__________之間。
= ________ mol·L-1·min-1。若繼續通入0.20mol BO2和0.10mol O2,再次達到新平衡后,BO3的物質的量介于__________之間。
查看答案和解析>>
科目:高中化學 來源:同步題 題型:填空題
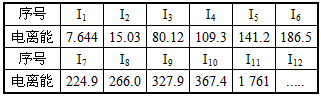
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com