
| A. | H2CO3?H2O+CO2↑ | B. | KOH═K++O2-+H+ | ||
| C. | HClO═H++ClO- | D. | Na2CO3═2Na++CO32- |
 口算題卡加應用題集訓系列答案
口算題卡加應用題集訓系列答案 綜合自測系列答案
綜合自測系列答案科目:高中化學 來源: 題型:選擇題
| A. | Y單質能溶于X元素的最高價氧化物的水化物 | |
| B. | W2能與H2Z發生置換反應 | |
| C. | 離子半徑由大到小:Z2->X+>Y3+>W2- | |
| D. | W、X形成兩種離子化合物,陰、陽離子個數比一定是1:2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| 氫氧化鈉質量(g) | 氯化鈉質量(g) | |
| ① | 2.40 | 3.51 |
| ② | 2.32 | 2.34 |
| ③ | 3.48 | 3.51 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 切開的金屬Na暴露在空氣中,光亮的表面逐漸變暗,發生的反應為2Na+O2═Na2O2 | |
| B. | 單質鈉具有很強的還原性,鈉離子具有很弱的氧化性 | |
| C. | Na著火時不能用水滅火,可用細沙覆蓋滅火 | |
| D. | 將少量Na投入到CuSO4溶液中,既有沉淀生成又有氣體放出 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
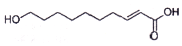 王漿酸是蜂王漿中特有的一種不飽和脂肪酸,在自然界中只有蜂王漿中才含有這種物質.其結構簡式如圖:下列有關干漿酸的結構與性質的說法正確的是( )
王漿酸是蜂王漿中特有的一種不飽和脂肪酸,在自然界中只有蜂王漿中才含有這種物質.其結構簡式如圖:下列有關干漿酸的結構與性質的說法正確的是( )| A. | 含有兩種官能團 | |
| B. | 與足里NaOH反應生成Cl0H18O3Na2 | |
| C. | 能發生加成反應,氧化反應、取代反應、加聚反應 | |
| D. | 能使Br/CCl4溶液、酸性KMnO4溶液褪色,褪色原理相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 碳酸鈣與鹽酸反應:CO32-+2H+═H2O+CO2↑ | |
| B. | 稀H2SO4與鐵粉反應:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 氫氧化鋇溶液與稀H2SO4反應:Ba2++SO42-═BaSO4↓ | |
| D. | 氧化鎂與稀硫酸混合:MgO+2H+═Mg2++H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com