
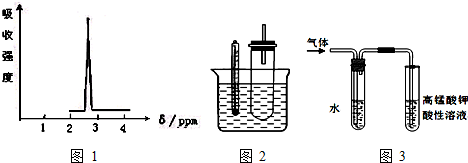
| A. |  分散系的分類 | B. |  稀釋濃硫酸的過程 | ||
| C. |  向碳酸鈉溶液中逐滴滴入鹽酸 | D. |  比較Na2CO3、NaHCO3的穩定性 |
分析 A.依據分散系的本質區別是分散質微粒直徑的大小判斷;
B.濃硫酸不導電;
C.碳酸鈉與鹽酸先反應生成碳酸氫鈉,碳酸氫鈉再與鹽酸反應生成二氧化碳;
D.要驗證碳酸氫鈉穩定性弱于碳酸鈉,應將碳酸氫鈉放在內管;
解答 解:A.膠體分散質粒子直徑在1到100納米之間,溶液分散質粒子直徑小于1納米,濁液分散質粒子直徑大于100納米,故A錯誤;
B.濃硫酸不導電,稀釋過程中導電能力先增大后較小,故B錯誤;
C.向Na2CO3溶液中逐滴滴加鹽酸先后發生Na2CO3+HCl=NaHCO3+NaCl,NaHCO3+HCl=NaCl+H2O+CO2↑,開始無氣體,后來才產生氣體,且前后所加鹽酸的體積比為1:1,故C正確;
D.要驗證碳酸氫鈉穩定性弱于碳酸鈉,應將碳酸氫鈉放在內管,故D錯誤;
故選:ABD.
點評 本題考查了常見分散系的特征、物質反應的反應先后順序,影響電解質導電能力原因,明確分散系分類依據、物質的性質是解題關鍵,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 侯氏制堿法的工藝過程中應用了物質溶解度的差異 | |
| B. | 工業上以氯氣和石灰乳為原料制備漂白粉 | |
| C. | 單質硅常用做光導纖維的材料,這與硅的半導體性能有一定關系 | |
| D. | 高壓鈉燈發出的黃光射程遠、透霧能力強,常用做路燈 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 常溫下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲線如圖所示(體積變化忽略不計).回答下列問題:
常溫下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲線如圖所示(體積變化忽略不計).回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol的氨氣與1mol的銨根離子所含電子數、質子數均為10NA | |
| B. | 14g乙烯和14g聚乙烯所含的原子數均為3NA | |
| C. | 標準狀況下,11.2LCH3CH20H中含有的C-H鍵的個數為2.5NA | |
| D. | 1L1mol•L-1的NaAl02溶液中含有Al02-的數目為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH4+、Al3+、SO42-、NO3- | B. | K+、Na+、CO32-、NO3- | ||
| C. | K+、NH4+、MnO4-、SO42- | D. | Na+、K+、NO3-、HSO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com