
【題目】當發動機工作時,反應產生的NO尾氣是主要污染物之一,NO的脫除方法和轉化機理是當前研究的熱點。請回答下列問題:
(1)已知:2NO(g)+O2 (g) =2NO2(g) △H1= -113kJ/mol
6NO2(g)+O3(g)=3N2O5(g) △H2= -227 kJ/mol
4NO2 (g)+O2(g)=2N2O5(g) △H3= -57 kJ/mol
則 2O3(g)= 3O2(g)是_________反應(填“放熱”或“吸熱”),以上 O3氧化脫除氮氧化物的總反應是NO(g)+O3(g)=NO2(g)+O2(g) △H4=_______kJ/mol,最后將NO2與_________劑反應轉化為無污染的氣體而脫除。
步驟 | 反應 | 活化能 | 正反應速率方程 | 逆反應速率方程 |
I | 2NO(g) | Ea1 |
|
|
II | N2O2(g)+O2(g) | Ea2 |
|
|
(2)已知:2NO(g)+O2(g) ![]() 2NO2(g)的反應歷程分兩步:
2NO2(g)的反應歷程分兩步:
①表中k1、k2、k3、k4是只隨溫度變化的常數,溫度升高將使其數值_____(填“增大”或“減小”)。
②反應I瞬間建立平衡,因此決定2NO(g)+O2(g)![]() 2NO2(g)反應速率快慢的是反應II,則反應I與反應II的活化能的大小關系為Ea1____Ea2(填“>”“<”或“=”),請依據有效碰撞理論微觀探析其原因______________________________________________。
2NO2(g)反應速率快慢的是反應II,則反應I與反應II的活化能的大小關系為Ea1____Ea2(填“>”“<”或“=”),請依據有效碰撞理論微觀探析其原因______________________________________________。
③一定溫度下,反應2NO(g)+O2(g)![]() 2NO2(g)的速率方程為
2NO2(g)的速率方程為![]() ,則k=_______ (用k1、k2、k3表示)。
,則k=_______ (用k1、k2、k3表示)。
(3)將一定量的 NO2放入恒容密閉容器中發生下列反應:2NO2(g) ![]() 2NO(g)+O2(g),測得其平衡轉化率α(NO2)隨溫度變化如圖所示,從 b 點到 a 點降溫平衡將向_____移動。圖中 a點對應溫度下,NO2的起始壓強為 160kPa,該溫度下反應的平衡常數Kp= __________(用平衡分壓代替平衡濃度計算,分壓=總壓×物質的量分數)
2NO(g)+O2(g),測得其平衡轉化率α(NO2)隨溫度變化如圖所示,從 b 點到 a 點降溫平衡將向_____移動。圖中 a點對應溫度下,NO2的起始壓強為 160kPa,該溫度下反應的平衡常數Kp= __________(用平衡分壓代替平衡濃度計算,分壓=總壓×物質的量分數)

【答案】放熱 -198 還原 增大 < 活化能低,同條件下單位體積內活化分子數多,有效碰撞幾率大,速率快 ![]() 左 108kPa
左 108kPa
【解析】
(1) 根據蓋斯定律計算反應熱并判斷反應為放熱還是吸熱反應;根據氧化還原反應規律,二氧化氮轉化為氮氣,氮元素化合價降低,需要加入還原劑與之反應;
(2) ①溫度升高化學反應速率加快;
②反應I反應速率快,反應II反應速率慢,根據碰撞理論,活化能低,同條件下單位體積內活化分子數多,有效碰撞幾率大,速率快;
③步驟I反應:2NO(g)![]() N2O2(g) ,
N2O2(g) ,![]() 1正=k1 c2 (NO),
1正=k1 c2 (NO),![]() 1逆=k2 c(N2O2),
1逆=k2 c(N2O2),
步驟II反應:N2O2(g)+O2(g)![]() 2NO2(g) ,
2NO2(g) ,![]() 2正=k3c(N2O2)c(O2),
2正=k3c(N2O2)c(O2),
步驟I反應+步驟II反應得總反應:2NO(g)+O2(g) ![]() 2NO2(g)
2NO2(g)
v正=![]() ×k3c(N2O2)c(O2)=
×k3c(N2O2)c(O2)=![]() ·c2 (NO)·c(O2)= k·c2 (NO)·c(O2);
·c2 (NO)·c(O2)= k·c2 (NO)·c(O2);
(3) 根據溫度對化學平衡的影響分析平衡移動方向;列出三段式找出平衡時各組分的平衡分壓,根據Kp= ![]() 計算。
計算。
(1) 已知: ①2NO(g)+O2 (g) =2NO2(g) △H1=-113kJ/mol
②6NO2(g)+O3(g)=3N2O5(g) △H2=-227 kJ/mol
③4NO2 (g)+O2(g)=2N2O5(g) △H3=-57 kJ/mol
根據蓋斯定律②![]() 2-③
2-③![]() 3得④2O3(g)= 3O2(g) △H=-283kJ/mol,因△H<0,所以為放熱反應;
3得④2O3(g)= 3O2(g) △H=-283kJ/mol,因△H<0,所以為放熱反應;
根據蓋斯定律(①+④)![]() 2得NO(g)+O3(g)=NO2(g)+O2(g) △H=[(-113kJ/mol)+(-283kJ/mol)]
2得NO(g)+O3(g)=NO2(g)+O2(g) △H=[(-113kJ/mol)+(-283kJ/mol)]![]() 2=-198 kJ/mol, 最后將NO2與還原劑反應轉化為無污染的氣體N2而脫除。
2=-198 kJ/mol, 最后將NO2與還原劑反應轉化為無污染的氣體N2而脫除。
故答案為:放熱;-198;還原;
(2) ①溫度升高化學反應速率加快, 所以溫度升高將使k1、 k2、 k3、 k4值增大;
②反應I反應速率快,反應II反應速率慢。根據碰撞理論,活化能越低,則在相同條件下單位體積內活化分子數越多,有效碰撞幾率就越大,化學反應速率就越快。 因此,反應
③步驟I反應:2NO(g)![]() N2O2(g) ,
N2O2(g) ,![]() 1正=k1 c2 (NO),
1正=k1 c2 (NO),![]() 1逆=k2 c(N2O2),
1逆=k2 c(N2O2),
步驟II反應:N2O2(g)+O2(g)![]() 2NO2(g) ,
2NO2(g) ,![]() 2正=k3c(N2O2)c(O2),
2正=k3c(N2O2)c(O2),
步驟I反應+步驟II反應得總反應:2NO(g)+O2(g) ![]() 2NO2(g)
2NO2(g)
v正=![]() ×k3c(N2O2)c(O2)=
×k3c(N2O2)c(O2)=![]() ·c2 (NO)·c(O2)= k·c2 (NO)·c(O2),故k =
·c2 (NO)·c(O2)= k·c2 (NO)·c(O2),故k =![]() ,
,
故答案為:增大;< ;活化能低,同條件下單位體積內活化分子數多,有效碰撞幾率大,速率快;![]() ;
;
(3) 根據反應2NO(g)+O2 (g) =2NO2(g) △H1=-113kJ/mol 為放熱反應,
則反應2NO2(g) ![]() 2NO(g)+O2(g)為吸熱反應,從 b 點到 a 點降溫平衡將向左移動。
2NO(g)+O2(g)為吸熱反應,從 b 點到 a 點降溫平衡將向左移動。
圖中 a點對應溫度下, NO2的起始壓強為 160kPa, 設起始時NO2的物質的量為a,則
2NO2(g) ![]() 2NO(g)+O2(g)
2NO(g)+O2(g)
起始(mol) a 0 0
轉化(mol)0.6a 0.6a 0.3a
平衡(mol)0.4a 0.6a 0.3a
平衡時總物質的量為0.4a+0.6a+0.3a=1.3a,恒溫恒容條件下,壓強之比等于物質的量之比,平衡時總壓強為160kPa![]() =208 kPa,
=208 kPa,
平衡時NO2、NO和O2的平衡分壓分別為208 kPa×![]() =64 kPa、208 kPa×
=64 kPa、208 kPa×![]() =96 kPa、208 kPa×
=96 kPa、208 kPa×![]() =48kPa,
=48kPa,
Kp= ![]() =
=![]() =108kPa,
=108kPa,
故答案為:左 ;108kPa。


科目:高中化學 來源: 題型:
【題目】C,Si、B,N、Cl在工業生產中具有重要的應用,試回答下列問題:

(1)碳納米管有單層或多層石墨層卷曲而成,其結構類似于石墨晶體,每個碳原子通過________雜化與周圍碳原子成鍵,多層碳納米管的層與層之間靠________結合在一起。
(2)現在新開發出一種具有和“龍芯”主要成分一樣的六角形籠狀結構單質Si12,它可能在未來的量子計算機中是一種理想的貯存信息的材料,根據圖示推斷這種六角形籠狀結構:Si12是____晶體,它與單晶硅互稱為________。
(3)SiC晶體結構與金剛石相似,碳化硅的結構與金剛石類似,其硬度僅次于金剛石,具有較強的耐磨性能。其中C原子的雜化方式為____________,微粒間存在的作用力是_____________,每個Si原子周圍距離最近的C原子為______個,其鍵角為_________。設晶胞邊長為a cm,密度為b g·cm-3,則阿伏加德羅常數可表示為____________________(用含A,b的式子表示)。
(4)氮化硼(BN)是一種重要的功能陶瓷材料,以天然硼砂為起始物,經過一系列反應可以得到BN。由于BN與CC屬于等電子體物質,其結構和性質有很大的相似性。
①BN有兩種晶體,對BN兩種晶體的描述中不正確的是______ 。
A.其中一種晶體可用作耐磨材料
B.其中一種晶體可用作潤滑材料
C.其中一種晶體鍵角為90°
D.其中一種晶體中存在六元環
②在與石墨結構相似的六方氮化硼晶體中,層內B原子與N原子之間的作用力為________,層間作用力為__________。B原子和N原子的雜化類型分別是________、__________。
③六方氮化硼在高溫高壓下,可以轉化為立方氮化硼,其結構與金剛石相似,硬度與金剛石相當,晶胞邊長為a cm,立方氮化硼晶胞中含有____個氮原子、_____個硼原子,晶胞頂點上的原子的配位數為______,立方氮化硼的密度是_________g·cm-3(阿伏加德羅常數為NA)。
④立方氮化硼比晶體硅具有更高硬度和耐熱性的原因是_____________________________。
(5)已知氮化碳晶體是新發現的高硬度材料,且構成該晶體的微粒間只以單鍵結合。下列關于該晶體的說法錯誤的是____________。
A.氮化碳屬于原子晶體,比金剛石中的硬度更大
B.該晶體中每個碳原子與4個氮原子相連,每個氮原子與3個碳原子相連,氮化碳的化學式為C3N4
C.該晶體中碳原子和氮原子的最外層都滿足8電子結構
D.該晶體與金剛石相似,都是原子間以非極性鍵形成空間網狀結構
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】三乙酸錳可作單電子氧化劑,用如下反應可以制取三乙酸錳:
4Mn(NO3)2·6H2O+26(CH3CO)2O=4(CH3COO)3Mn +8HNO2+ 3O2↑+40CH3COOH。
(1)基態錳原子的價層電子排布式為______,基態Mn3+含有的未成對電子數是______。
(2) CH3COOH中碳原子的雜化形式為________。
(3) NO3-的空間構型是________,與NO3-互為等電子體的分子的化學式為__________(任寫一種)。
(4) CH3COOH能與H2O以任意比互溶的原因是____________________。
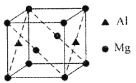
(5)某種鎂鋁合金可作為儲鈉材料,該合金晶胞結構如圖所示,晶胞棱長為anm,該合金的化學式為_______,晶體中每個鎂原子周圍距離最近的鋁原子數目為_______,該晶體的密度為______g/cm3(阿伏伽德羅常數的數值用NA表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】堿式碳酸鈷用作催化劑及制鈷鹽原料,陶瓷工業著色劑,電子、磁性材料的添加劑。利用以下裝置測定堿式碳酸鈷[Cox(OH)y(CO3)z·H2O]的化學組成。

已知:堿式碳酸鈷中鈷為+2價,受熱時可分解生成三種氧化物。請回答下列問題:
(1)選用以上裝置測定堿式碳酸鈷[Cox(OH)y(CO3)z·H2O]的化學組成,其正確的連接順序為a→b→____(按氣流方向,用小寫字母表示)。
(2)樣品分解完,打開活塞K,緩緩通入氮氣數分鐘,通入氮氣的目的是_______________。
(3)取堿式碳酸鈷樣品34.9 g,通過實驗測得分解生成的水和二氧化碳的質量分別為3.6 g、8.8 g,則該堿式碳酸鈷的化學式為______________________________。
(4)某興趣小組以含鈷廢料(含少量Fe、Al等雜質)制取CoCl2·6H2O的一種實驗設計流程如下:

已知:25 ℃時,部分陽離子以氫氧化物形成沉淀時,溶液的pH見下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
開始沉淀(pH) | 1.9 | 7.0 | 7.6 | 3.4 |
完全沉淀(pH) | 3.2 | 9.0 | 9.2 | 4.7 |
①操作Ⅰ用到的玻璃儀器主要有___________、_____________、___________;
②加鹽酸調整pH為2~3的目的為____________________________________________;
③操作Ⅱ的過程為_______________、_______________、____________、洗滌、干燥。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA表示阿伏加德羅常數的值, 下列敘述正確的是
A. 1mol H2O中含有的極性共價鍵數目為2NA
B. 16 g16O2和18O2混合物中含有的質子數目為8NA
C. Zn和濃硫酸反應得到22.4LSO2和 H2混合氣體時, 轉移的電子數為4NA
D. 標準狀況下2 mol NO與1 mol O2充分反應后分子數共2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】標準狀況下VL氨氣溶解在1L水中(水的密度近似為1g/mL),所得溶液的密度為ρg/mL,質量分數為ω,物質濃度為c mol/L,則下列關系中不正確的是
A. ![]()
B. ![]()
C. ![]()
D. ![]() =1000Vρ/(17V+22400)
=1000Vρ/(17V+22400)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】固體表面的化學過程研究對于化學工業非常重要。在Fe催化劑、一定壓強和溫度下合成氨的反應機理如下圖所示。下列說法不正確的是( )

A. N2和H2分子被吸附在鐵表面發生反應
B. 吸附在鐵表面的N2斷裂了N≡N鍵
C. NH3分子中的N-H鍵不是同時形成
D. Fe催化劑可以有效提高反應物的平衡轉化率
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種新型燃料電池,它以多孔鎳板為電極插入KOH溶液中,然后分別向兩極上通乙烷和氧氣,其電極反應式為:C2H6+18OH--14e- =2CO32-+12H2O,7H2O+![]() O2+14e- =14OH-,有關此電池的推斷正確的是
O2+14e- =14OH-,有關此電池的推斷正確的是
A. 電解質溶液中電子向正極移動
B. 放電一段時間后,KOH的物質的量濃度不變
C. 通乙烷的電極為負極
D. 參加反應的O2和C2H6的物質的量之比為2:7
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法中不正確的是
A.從1 L 1 mol·L-1的NaCl溶液中取出10 mL,其濃度仍是1 mol·L-1
B.配制0.5 L 10 mol·L-1的鹽酸,需要氯化氫氣體112 L(標準狀況)
C.0.5 L 2 mol·L-1BaCl2溶液中,Ba2+和Cl-總數為3×6.02×1023
D.10 g 98%的硫酸(密度為1.84 g· cm-3)與10 mL 18.4 mol·L-1硫酸的濃度是不同的
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com