
下列實驗操作、現象和結論均正確的是( )
選項 | 實驗操作 | 現象 | 結 |
A | 分別加熱Na2CO3和NaHCO3固體 | 試管內壁都有水珠 | 兩種物質均受熱分解 |
B | 向稀的苯酚水溶液中滴加飽和溴水 | 生成白色沉淀 | 產物三溴苯酚不溶于水 |
C | 向含I-的無色溶液中滴加少量新制氯水,再滴加淀粉溶液 | 加入淀粉后溶液變成藍色 | 還原性:Cl- > I- |
D | 向FeSO4溶液中先滴入KSCN溶液再滴加H2O2溶液 | 加入H2O2后溶液變成血紅色 | Fe2+既有氧化性又有還原性 |
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源:2016-2017學年甘肅省高二上10月月考化學試卷(解析版) 題型:選擇題
氨水中所含的分子和離子有 
①NH4+ ②H2O ③NH3 ④NH3·H2O ⑤H+ ⑥OH-
A.①②③ B.②③④⑤ C.②③④⑤⑥ D.①②③④⑤⑥
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省黃山市高三上月考二化學卷(解析版) 題型:實驗題
某化學興趣小組同學展開對漂白劑亞氯酸鈉(NaClO2)的研究。
實驗I.制取NaClO2晶體
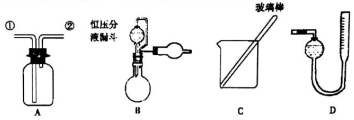
已知:NaClO2飽和溶液在溫度低于38 ℃時析出的晶體是NaClO2·3H2O,高于38 ℃時析出的晶體是NaClO2,高于60 ℃時NaClO2分解成NaClO3和NaCl。現利用下圖所示裝置進行實驗。

(1) 裝置③的作用是 。
(2) 裝置②中產生ClO2的化學方程式為 ;裝置④中制備NaClO2的化學方程式為 。
(3) 從裝置④反應后的溶液獲得NaClO2晶體的操作步驟如下:
① 減壓,55 ℃蒸發結晶;② 趁熱過濾;③ ;④ 低于60 ℃干燥,得到成品。
實驗II.測定某亞氯酸鈉樣品的純度
設計如下實驗方案,并進行實驗:
① 確稱取所得亞氯酸鈉樣品m g于燒杯中,加入適量蒸餾水和過量的碘化鉀晶體,再滴入適量的稀硫酸,充分反應(已知:ClO2- + 4 I- + 4 H+ = 2 H2O + 2 I2 + Cl-);將所得混合液配成250 mL待測溶液。
②移取25.00mL待測溶液于錐形瓶中,加幾滴淀粉溶液,用cmol·L-1Na2S2O3標準液滴定,至滴定終點。重復2次,測得平均值為VmL(已知:I2+2S2O32-=2I-+S4O62-)。
(4) 達到滴定終點時的現象為 。
(5) 該樣品中NaClO2的質量分數為 (用含m、c、V的代數式表示)。
(6) 在滴定操作正確無誤的情況下,此實驗測得結果偏高,原因用離子方程式表示為 。
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省黃山市高三上月考二化學卷(解析版) 題型:選擇題
Cyrneine A對治療神經系統疾病有著很好的療效。可用香芹酮經過多步反應合成: ,下列說法不正確的是( )
,下列說法不正確的是( )
A.香芹酮的分子式為C10H14O
B.Cyrneine A可以發生加成反應、消去反應和氧化反應
C.香芹酮和Cyrneine A均能使酸性KMnO4溶液褪色
D.與香芹酮互為同分異構體,分子中有4種不同化學環境的氫原子的酚類化合物共有3種
查看答案和解析>>
科目:高中化學 來源:2017屆重慶一中高三上學期第二次月考化學試卷(解析版) 題型:實驗題
2Zn(OH)2·ZnCO3是制備活性ZnO的中間體,以鋅焙砂(主要成分為ZnO,含少量Cu2、Mn2+等離子)為原料制備2Zn(OH)2·ZnCO3的工藝流程如下:
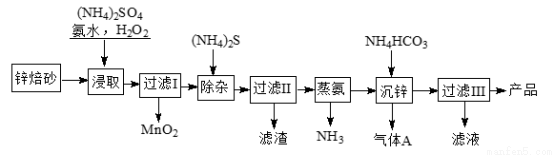
請回答下列問題:
(1)當(NH4)2SO4、NH3·H2O的混合溶液中存在c(NH4+)=2c(SO42?)時,溶液呈 (填“酸”、“堿”或“中”)性。
(2)“浸取”時為了提高鋅的浸出率,可采取的措施是 (任寫兩種)。
(3)“浸取”時加入的NH3·H2O過量,生成MnO2的離子方程式為 。
(4)適量S2?能將Cu2+硫化物沉淀而除去,若選擇ZnS進行除雜,是否可行?用計算說明原因: 。
[已知:Ksp(ZnS)=1.6×10?24,Ksp(CuS)=1.3×10?36;一般認為反應的平衡常數K>105,該反應進行基本完全。]
(5)“沉鋅”的離子方程式為___________________。
(6)上述流程中多次需要過濾,實驗室進行過濾操作需要用到的玻璃儀器有__________。“過濾III”所得濾液可循環使用,產品需洗滌干燥后備用,檢驗產品洗滌干凈的操作和現象是_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com