
(15分)能源是國民經濟發展的重要基礎,我國目前使用的能源主要是化石燃料。
(1)在25℃、101 kPa時,16 g CH4完全燃燒生成液態水時放出的熱量是890.31 kJ,則CH4燃燒的熱化學方程式為__________________________________________。
(2)已知:C(s)+O2(g)===CO2(g);ΔH=-437.3 kJ·mol-1
H2(g)+O2(g)===H2O(g);ΔH=-285.8 kJ·mol-1
CO(g)+O2(g)===CO2(g);ΔH=-283.0 kJ·mol-1
則煤氣化反應C(s)+H2O(g)===CO(g)+H2(g)的焓變ΔH=________kJ·mol-1。
(3)如下圖所示組成閉合回路,其中,甲裝置中CH4為負極,O2和CO2的混合氣體為正極,稀土金屬材料為電極,以熔融碳酸鹽為電解質;乙裝置中a、b為石墨,b極上有紅色物質析出,CuSO4溶液的體積為200 mL。
①甲裝置中氣體A為 (填“CH4”或“O2和CO2”),d極上的電極反應式為_____________。
②乙裝置中a極上的電極反應式為____________________________。
若在a極產生112mL(標準狀況)氣體,則甲裝置中消耗CH4________ mL (標準狀況),乙裝置中所得溶液的pH=__________。(忽略電解前后溶液體積變化)
③如果乙中電極不變,將溶液換成飽和Na2SO4溶液,當陰極上有a mol氣體生成時,同時有w g Na2SO4·10H2O晶體析出,若溫度不變,剩余溶液中溶質的質量分數應為________(用含w、a的表達式表示,不必化簡)。
 應用題作業本系列答案
應用題作業本系列答案 暑假作業暑假快樂練西安出版社系列答案
暑假作業暑假快樂練西安出版社系列答案科目:高中化學 來源: 題型:閱讀理解
(20分)能源是國民經濟發展的重要基礎,我國目前使用的能源主要是化石燃料。(1) 在25℃、101 kPa時,16 g CH4完全燃燒生成液態水時放出的熱量是890.31 kJ,則CH4燃燒的熱化學方程式為__________________________________________。
(2) 已知:C(s)+O2(g)===CO2(g);ΔH=-437.3 kJ·mol-1
H2(g)+O2(g)===H2O(g);ΔH=-285.8kJ·mol-1
CO(g)+O2(g)===CO2(g);ΔH=-283.0 kJ·mol-1
則煤氣化反應C(s)+H2O(g)===CO(g)+H2(g) 的焓變ΔH=_____________。
(3) 高爐煉鐵是CO氣體的重要用途之一,其基本反應為:
FeO(s)+CO(g)Fe(s)+CO2(g) ΔH>0,已知在1100℃時,該反應的化學平衡常數K=0.263。
① 溫度升高,化學平衡移動后達到新的平衡,此時平衡常數K值__________(填“增大”、“減小”或“不變”);
② 1100℃時測得高爐中,c(CO2)=0.025mol·L-1,c(CO)=0.1 mol·L-1,則在這種情況下,該反應是否處于化學平衡狀態____________(填“是”或“否”),其判斷依據是______
____________________________________________________________。
(4) 如下圖所示組成閉合回路,其中,甲裝置中CH4為負極,O2和CO2的混合氣體為正極,稀土金屬材料為電極,以熔融碳酸鹽為電解質;乙裝置中a、b為石墨,b極上有紅色物質析出,CuSO4溶液的體積為200 mL。
① 甲裝置中氣體A為 (填“CH4”或“O2和CO2”),d極上的電極反應式為
_____________________________________。
② 乙裝置中a極上的電極反應式為__________________________________。
若在a極產生112mL(標準狀況)氣體,則甲裝置中消耗CH4________ mL (標準狀況),乙裝置中所得溶液的pH=__________。(忽略電解前后溶液體積變化)
③ 如果乙中電極不變,將溶液換成飽和Na2SO4溶液,當陰極上有a mol氣體生成時,同時有w g Na2SO4·10H2O晶體析出,若溫度不變,剩余溶液中溶質的質量分數應為__________________________(用含w、a的表達式表示,不必化簡)。
查看答案和解析>>
科目:高中化學 來源: 題型:
(15分)能源是國民經濟發展的重要基礎,我國目前使用的能源主要是化石燃料。
(1)在25℃、101kPa時,16 g CH4完全燃燒生成液態水時放出的熱量是890.31 kJ,則CH4燃燒的熱化學方程式為__________________________________________。
(2)已知:C(s)+O2(g)===CO2(g);ΔH=-437.3 kJ·mol-1
H2(g)+O2(g)===H2O(g);ΔH=-285.8 kJ·mol-1
CO(g)+O2(g)===CO2(g);ΔH=-283.0 kJ·mol-1
則煤氣化反應C(s)+H2O(g)===CO(g)+H2(g) 的焓變ΔH=________kJ·mol-1。
(3)如下圖所示組成閉合回路,其中,甲裝置中CH4為負極,O2和CO2的混合氣體為正極,稀土金屬材料為電極,以熔融碳酸鹽為電解質;乙裝置中a、b為石墨,b極上有紅色物質析出,CuSO4溶液的體積為200 mL。
①甲裝置中氣體A為 (填“CH4”或“O2和CO2”),d極上的電極反應式為_____________。
②乙裝置中a極上的電極反應式為____________________________。
若在a極產生112mL(標準狀況)氣體,則甲裝置中消耗CH4________mL (標準狀況),乙裝置中所得溶液的pH=__________。(忽略電解前后溶液體積變化)
③如果乙中電極不變,將溶液換成飽和Na2SO4溶液,當陰極上有a mol氣體生成時,同時有w g Na2SO4·10H2O晶體析出,若溫度不變,剩余溶液中溶質的質量分數應為________(用含w、a的表達式表示,不必化簡)。
查看答案和解析>>
科目:高中化學 來源:2011-2012學年山東省高三下學期假期學習效果檢測考試化學試卷 題型:填空題
(20分)能源是國民經濟發展的重要基礎,我國目前使用的能源主要是化石燃料。(1) 在25℃、101 kPa時,16 g CH4完全燃燒生成液態水時放出的熱量是890.31 kJ,則CH4燃燒的熱化學方程式為__________________________________________。
(2) 已知:C(s)+O2(g)===CO2(g);ΔH=-437.3 kJ·mol-1
H2(g)+O2(g)===H2O(g);ΔH=-285.8 kJ·mol-1
CO(g)+O2(g)===CO2(g);ΔH=-283.0 kJ·mol-1
則煤氣化反應C(s)+H2O(g)===CO(g)+H2(g) 的焓變ΔH=_____________。
(3) 高爐煉鐵是CO氣體的重要用途之一,其基本反應為:
FeO(s)+CO(g) Fe(s)+CO2(g) ΔH>0,已知在1100℃時,該反應的化學平衡常數K=0.263。
Fe(s)+CO2(g) ΔH>0,已知在1100℃時,該反應的化學平衡常數K=0.263。
① 溫度升高,化學平衡移動后達到新的平衡,此時平衡常數K值__________(填“增大”、“減小”或“不變”);
② 1100℃時測得高爐中,c(CO2)=0.025mol·L-1,c(CO)=0.1 mol·L-1,則在這種情況下,該反應是否處于化學平衡狀態____________(填“是”或“否”),其判斷依據是______
____________________________________________________________。
(4) 如下圖所示組成閉合回路,其中,甲裝置中CH4為負極,O2和CO2的混合氣體為正極,稀土金屬材料為電極,以熔融碳酸鹽為電解質;乙裝置中a、b為石墨,b極上有紅色物質析出,CuSO4溶液的體積為200 mL。

① 甲裝置中氣體A為 (填“CH4”或“O2和CO2”),d極上的電極反應式為
_____________________________________。
② 乙裝置中a極上的電極反應式為__________________________________。
若在a極產生112mL(標準狀況)氣體,則甲裝置中消耗CH4________ mL (標準狀況),乙裝置中所得溶液的pH=__________。(忽略電解前后溶液體積變化)
③ 如果乙中電極不變,將溶液換成飽和Na2SO4溶液,當陰極上有a mol氣體生成時,同時有w g Na2SO4·10H2O晶體析出,若溫度不變,剩余溶液中溶質的質量分數應為__________________________(用含w、a的表達式表示,不必化簡)。
查看答案和解析>>
科目:高中化學 來源:2011-2012學年山東省濟南市高三12月月考化學試卷 題型:填空題
(15分)能源是國民經濟發展的重要基礎,我國目前使用的能源主要是化石燃料。
(1)在25℃、101 kPa時,16 g CH4完全燃燒生成液態水時放出的熱量是890.31 kJ,則CH4燃燒的熱化學方程式為__________________________________________。
(2)已知:C(s)+O2(g)===CO2(g);ΔH=-437.3 kJ·mol-1
H2(g)+O2(g)===H2O(g);ΔH=-285.8 kJ·mol-1
CO(g)+O2(g)===CO2(g);ΔH=-283.0 kJ·mol-1
則煤氣化反應C(s)+H2O(g)===CO(g)+H2(g) 的焓變ΔH=________kJ·mol-1。
(3)如下圖所示組成閉合回路,其中,甲裝置中CH4為負極,O2和CO2的混合氣體為正極,稀土金屬材料為電極,以熔融碳酸鹽為電解質;乙裝置中a、b為石墨,b極上有紅色物質析出,CuSO4溶液的體積為200 mL。
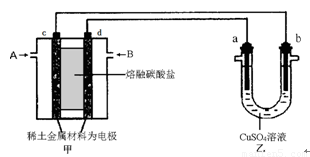
①甲裝置中氣體A為 (填“CH4”或“O2和CO2”),d極上的電極反應式為_____________。
②乙裝置中a極上的電極反應式為____________________________。
若在a極產生112mL(標準狀況)氣體,則甲裝置中消耗CH4________ mL (標準狀況),乙裝置中所得溶液的pH=__________。(忽略電解前后溶液體積變化)
③如果乙中電極不變,將溶液換成飽和Na2SO4溶液,當陰極上有a mol氣體生成時,同時有w g Na2SO4·10H2O晶體析出,若溫度不變,剩余溶液中溶質的質量分數應為________(用含w、a的表達式表示,不必化簡)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com