
| A. | 濃硫酸(98%)的物質的量濃度 | B. | 常溫下氯化鈉的溶解度 | ||
| C. | 標準狀況下氣體摩爾體積 | D. | 0.2g金剛石所含的C原子數 |
分析 假設12C的相對原子質量為24,且以0.024 千克12C所含有的原子數為阿伏加德羅常數,則在規定12C的相對原子質量為24時,實際上是把作為相對原子質量的標準從原來用12C質量的$\frac{1}{24}$改為$\frac{1}{24}$,但是單個碳原子的質量并沒有因此而發生改變;原來是以0.012kg12C所含有的碳原子數作為阿伏加德羅常數(即6.02×1023),現在用0.024kg12C中所含的原子個數為阿伏加德羅常數(NA),很明顯0.024kg12C中所含的原子個數是0.012kg12C中所含的原子個數的2倍;故阿伏加德羅常數(NA)變為原來阿伏加德羅常數的2倍(即2×6.02×1023),以此來解答.
解答 解:A.由假設12C的相對原子質量為24,且以0.024 千克12C所含有的原子數為阿伏加德羅常數,碳原子的質量不變,則阿伏加德羅常數(NA)變為原來阿伏加德羅常數的2倍(即2×6.02×1023),濃硫酸(98%)的物質的量濃度變為原來一半,故A不選;
B.一定溫度下,100g水溶解氯化鈉的質量為定值,溶解度不變,故B選;
C.氣體摩爾體積是單位物質的量的氣體所占的體積,阿伏伽德羅常數變大,則物質的量變了,即氣體摩爾體積也變化了,故C不選;
D.由假設12C的相對原子質量為24,且以0.024 千克12C所含有的原子數為阿伏加德羅常數,碳原子的質量不變,則阿伏加德羅常數(NA)變為原來阿伏加德羅常數的2倍(即2×6.02×1023),0.2g金剛石所含的C原子數變為原來1半,故D不選;
故選:B.
點評 本題考查阿伏伽德羅常數,明確常數的規定發生變化時其數值的變化是解答本題的關鍵,并熟悉摩爾質量、摩爾體積等概念來解答.


 津橋教育計算小狀元系列答案
津橋教育計算小狀元系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
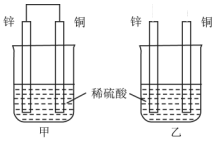 關于如圖所示裝置的敘述,正確的是( )
關于如圖所示裝置的敘述,正確的是( )| A. | 兩燒杯中銅片表面均無氣泡產生 | B. | 甲中銅片是正極,乙中銅片是負極 | ||
| C. | 甲中電流由鋅片經導線流向銅片 | D. | 兩燒杯鋅片均發生氧化反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 .
. .
. 和
和 ,寫出另3種同分異構體的結構簡式
,寫出另3種同分異構體的結構簡式 、
、 、
、 .
.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
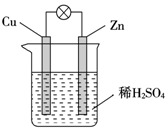
| A. | 電子從銅片經外電路流向鋅 | B. | Zn為負極,Cu為正極 | ||
| C. | H+在銅片上得電子發生氧化反應 | D. | 該裝置能將電能轉化為化學能 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com