
【題目】苯乙酸銅是合成優良催化劑、傳感材料納米氧化銅的重要前驅體之一。下面是它的一種實驗室合成路線:


制備苯乙酸的裝置如右圖所示(加熱和夾持裝置等略),已知:苯乙酸的熔點為76.5 ℃,微溶于冷水,溶于乙醇。回答下列問題:(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸時,加入蒸餾水與濃硫酸的先后順序是_____________________。
(2)將a中的溶液加熱至100 ℃,緩緩滴加40 g苯乙腈到硫酸溶液中,然后升溫至130 ℃繼續反應。在裝置中,儀器b的作用是______________;儀器c的名稱是__________,其作用是__________________。反應結束后加適量冷水,再分離出苯乙酸粗品。加人冷水的目的是_______。下列儀器中可用于分離苯乙酸粗品的是___________(填標號)。
A.分液漏斗 B.漏斗C.燒杯 D.直形冷凝管 E.玻璃棒
科目:高中化學 來源: 題型:
【題目】通過以下反應可獲得新型能源二甲醚(CH3OCH3)。下列說法不正確的是
①C(s) + H2O(g)=CO(g) + H2(g) ΔH1 = a kJmol-1
②CO(g) + H2O(g)=CO2 (g) + H2 (g) ΔH2 = b kJmol-1
③CO2(g) + 3H2(g)=CH3OH(g) + H2O(g) ΔH3= c kJmol-1
④2CH3OH(g)=CH3OCH3(g) + H2O(g) ΔH4= d kJmol-1
A. 反應①、②為反應③提供原料氣
B. 反應③也是CO2資源化利用的方法之一
C. 反應CH3OH(g)![]() 1/2 CH3OCH3 (g) +1/2H2O(l)的ΔH=d/2kJ·mol1
1/2 CH3OCH3 (g) +1/2H2O(l)的ΔH=d/2kJ·mol1
D. 反應 2CO(g) + 4H2 (g)![]() CH3OCH3 (g) + H2O(g)的ΔH= ( 2b+ 2c+d)
CH3OCH3 (g) + H2O(g)的ΔH= ( 2b+ 2c+d)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學是一門實驗科學,化學反應過程中的能量變化和速率變化是中學化學研究的重要內容
Ⅰ.利用如圖所示裝置測定中和熱
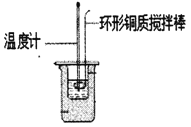
(1)圖中明顯有一處錯誤,請指出___________
(2)________(填“能”或“不能”)用Ba(OH)2 溶液和硫酸代替氫氧化鈉溶液和鹽酸進行中和熱測定
Ⅱ.探究硫酸銅的量對氫氣生成速率的影響。將表中所給的混合溶液分別加入到6個盛有過量Zn粒的反應瓶中,收集產生的氣體,記錄獲得相同體積氣體所需的時間。
實驗 混合溶液 | A | B | C | D | E | F |
4mol/L H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
飽和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
(1) 請完成此實驗設計,其中: V8=_________
(2) 當CuSO4溶液少量時,反應速率明顯加快,原因_______
(3) 當加入的CuSO4溶液超過一定量時,生成氫氣的速率反而會下降。請分析氫氣生成速率下降的主要原因:______________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NH3可用于生產硝酸和尿素。
(1)生產硝酸:
① NH3催化氧化是工業制硝酸的第一步反應,其化學方程式是_____。
② 除此之外,還可能發生以下副反應:
4NH3 (g)+ 4O2 (g) === 2N2O (g) +6H2O (g) ΔH=-1105 kJ/mol
4NH3 (g) + 3O2 (g) === 2N2 (g) +6H2 O(g) ΔH=-1269 kJ/mol
兩個副反應在理論上趨勢均很大,但實際生產中影響并不大,原因是_____。
(2)生產尿素:
① 尿素的合成分兩步進行:
a.2NH3 (g)+CO2(g) ![]() NH2COONH4(l) ΔH=-117 kJ/mol
NH2COONH4(l) ΔH=-117 kJ/mol
b.NH2COONH4(l) ![]() CO(NH2)2(l)+H2O(l) ΔH=+15 kJ/mol
CO(NH2)2(l)+H2O(l) ΔH=+15 kJ/mol

寫出總反應的熱化學方程式:______。
② 右圖為n(NH3):n(CO2) = 4 : 1時,溫度對CO2的轉化率的影響。解釋溫度升高CO2的平衡轉化率增大的原因:______。
③ 測定尿素樣品含氮量的方法如下:取a g尿素樣品,將所含氮完全轉化為NH3,所得NH3用過量的v1 mL c1 mol·L1 H2SO4溶液吸收完全,剩余H2SO4用v2 mL c2 mol·L1 NaOH溶液恰好中和,則尿素樣品中氮元素的質量分數是______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】PEI [ ]是一種非結晶性塑料。其合成路線如下(某些反應條件和試劑已略去):
]是一種非結晶性塑料。其合成路線如下(某些反應條件和試劑已略去):

已知:
(1)A為鏈狀烴。A的化學名稱為______。
(2)A→B的反應類型為______。
(3)下列關于D的說法中正確的是______(填字母)。
a.不存在碳碳雙鍵
b.可作聚合物的單體
c.常溫下能與水混溶
(4)F由4-氯-1,2-二甲苯催化氧化制得。F所含官能團有-Cl和______。
(5)C的核磁共振氫譜中,只有一個吸收峰。僅以2-溴丙烷為有機原料,選用必要的無機試劑也能合成C寫出有關化學方程式:______。
(6)F→K 的反應過程中有多種副產物。其中一種含有3個環的有機物的結構簡式是___。
(7)以E和K為原料合成PEI分為三步反應。

寫出中間產物1、中間產物2的結構簡式:______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲醇是一種可再生能源,具有開發和應用的廣闊前景,請回答下列問題:
(1)一定溫度下,在一恒容的密閉容器中,由CO和H2合成甲醇:
CO(g)+2H2(g) ![]() CH3OH(g)
CH3OH(g)
①下列情形能說明該反應已達到平衡狀態的是___________(填序號)
A.每消耗1mol CO的同時生成2molH2
B.混合氣體總物質的量不變
C.生成CH3OH的速率與消耗CO的速率相等
D.CH3OH、CO、H2的濃度都不再發生變化
②CO的平衡轉化率(α)與溫度、壓強的關系如圖所示。B、C兩點的平衡常數K(C)____K(B)(填“>”、“=”或“<”)
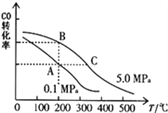
③某溫度下,將2.0mol CO和6.0molH2充入2L的密閉容器中,達到平衡時測得c(CO)=0.25mol/L,CO的轉化率=______,此溫度下的平衡常數K=______(保留二位有效數字)
(2)常溫下,將V mL、0.20mol/L氫氧化鈉溶液逐滴加入到20.00mL、0.20mol/L甲酸溶液中,充分反應,溶液pH=7,此時V______20.00(填“>”、“=”或“<”);當氫氧化鈉溶液與甲酸溶液恰好完全反應時,溶液中所含離子濃度由大到小排列順序_____________
(3)溫度650℃的熔融鹽燃料電池,用(CO、H2)作反應物,空氣與CO2的混合氣體為正極反應物,鎳作電極,用Li2CO3和Na2CO3混合物作電解質。該電池的正極反應式為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】隨原子序數的遞增,八種短周期元素原子半徑的相對大小、最高正價或最低負價的變化如下圖所示。
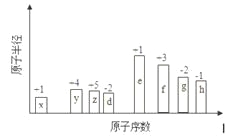
根據判斷出的元素回答問題:
(1)f在元素周期表的位置是__________。
(2)比較d、e常見離子的半徑的大小(用化學式表示,下同)_______>__________;比較g、h
的最高價氧化物對應的水化物的酸性強弱是:_______>__________。
(3)任選上述元素組成一種四原子共價化合物,寫出其電子式__________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com