
體積為1ml、濃度均為0.10mol/L的XOH和X2CO3溶液分別加水稀釋至體積為V,pH隨lgV的變化情況如圖所示,下列敘述中正確的是( )
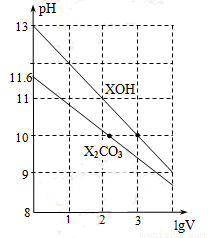
A.XOH是弱堿
B.pH=10的兩種溶液中的c(X+):XOH大于X2CO3
C.已知H2CO3的電離平衡常數Ka1遠遠大于Ka2,則Ka2約為1.0×10-10.2
D.當lgV=2時,若X2CO3溶液升高溫度,溶液堿性增強,則c(HCO3-)/c(CO32-)減小
科目:高中化學 來源:2015-2016學年河北省冀州市高一下期末理科化學A卷(解析版) 題型:選擇題
實驗室里有200 mLCH3COOCH2CH3,經檢驗,發現其中溶有少量CH3COOH。如果要除去這些CH3COOH,請選擇下列中的有效方法 ( )
A.蒸餾
B.水洗后分液
C.用過量飽和Na2 CO3溶液洗滌后分液
CO3溶液洗滌后分液
D.用過量NaCl溶液洗滌后分液
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江蘇省高二下第二次月考化學試卷(解析版) 題型:選擇題
下列關于有機物的說法正確的是
A.乙醛和甲苯都能與溴水反應
B.蛋白質和油脂都屬于天然高分子化合物
C.甲烷中混有的乙烯可通過溴的四氯化碳除去
D.苯酚能使酸性高錳酸鉀溶液褪色
查看答案和解析>>
科目:高中化學 來源:2016屆吉林省長春十一高三下考前沖刺理綜化學試卷二(解析版) 題型:實驗題
ClO2與Cl2的氧化性相近。在自來水消毒和果蔬保鮮等方面應用廣泛。某興趣小組通過圖1裝置(夾持裝置略)對其制備、吸收、釋放和應用進行了研究。
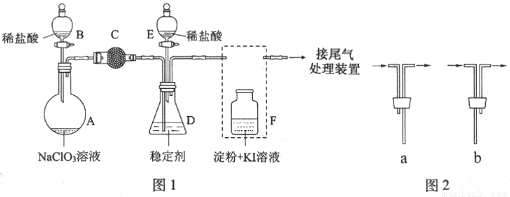
(1)儀器D的名稱是___________,安裝F中導管時,應選用圖2中的___________。
(2)打開B的活塞,A中發生反應:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O。為使ClO2在D中被穩定劑充分吸收,滴加稀鹽酸的速度宜___________(填“快”或“慢”).
(3)關閉B的活塞,ClO2在D中被穩定劑完全吸收生成NaClO2,此時F中溶液的顏色不變,則裝置C的作用是___________。
(4)已知在酸性條件下NaClO2可發生反應生成NaCl并釋放出ClO2,該反應的離子方程式為___________,在ClO2釋放實驗中,打開E的活塞,D中發生反應,則裝置F的作用是___________。
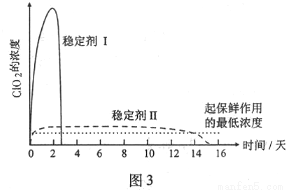
(5)已吸收ClO2氣體的穩定劑Ⅰ和穩定劑Ⅱ,加酸后釋放ClO2的濃度隨時間的變化如圖3所示,若將其用于水果保鮮,你認為效果較好的穩定劑是___________,原因是___________。
查看答案和解析>>
科目:高中化學 來源:2016屆安徽省高三畢業班最后一卷理綜化學試卷(解析版) 題型:簡答題
海水淡化及海水資源的提取利用是當今化工行業重要課題。
回答下列問題:
(1)下列屬于海水淡化常見工藝的是________(填序號)。
①電滲析法 ②蒸餾法 ③離子交換法 ④沉淀法
(2)采用“空氣吹出法”從濃海水中吹出Br2,并用純堿吸收。堿吸收溴的主要反應是 Br2+Na2CO3+H2O→ NaBr+NaBrO3+NaHCO3,吸收1 mol Br2時,轉移的電子為________mol。
(3)海水提鎂的一段工藝流程如下圖:

濃海水的主要成分如下:
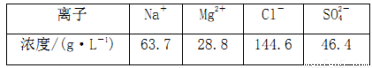
該工藝過程中,脫硫階段主要反應的離子方程式為____________________________________________,產品2 的化學式為________,1 L 濃海水最多可得到產品2 的質量為________g。
(4)采用石墨陽極、不銹鋼陰極電解熔融的氯化鎂,發生反應的化學方程式為:_______________。電解時,若有少量水存在會造成產品鎂的消耗,寫出有關反應的化學方程式:__________________
查看答案和解析>>
科目:高中化學 來源:2016屆安徽省高三畢業班最后一卷理綜化學試卷(解析版) 題型:選擇題
常溫下,在0.2mol/LAlCl3溶液中,逐滴加入1.0mol/LNaOH溶液,實驗測得溶液pH隨NaOH溶液體積變化曲線如下圖,下列有關說法正確的( )
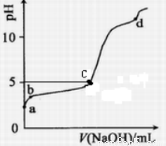
A.a 點時,溶液呈酸性的原因是Al3+水解,離子方程式為:Al3++3OH- Al(OH)3
Al(OH)3
B.b點水的電離程度小于a點
C.通過曲線變化,可估計約為1×10-20
D.d點時,溶液中已無沉淀剩余
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山西省高二5月月考化學試卷(解析版) 題型:選擇題
分子式為C8H10的芳香烴具有的同分異構體有
A. 3種 B. 4種 C. 5種 D. 6種
查看答案和解析>>
科目:高中化學 來源:2015-2016學年福建省高一下第二次月考化學試卷(解析版) 題型:推斷題
X、Y、Z、M、G五種元素分屬三個短周期,且原子序數依次增大。X、Z同主族,可形成離子化合物ZX;Y、M同主族,可形成MY2、MY3兩種分子。回答下列問題:
(1) Y在元素周期表中的位置為_____________________________.
(2) 上述元素的最高價氧化物對應的水化物酸性最強的是_____________________ (寫化學式),非金屬氣態氫化物還原性最強的是_________________(寫化學式)。
(3) Y、G的單質或兩元素之間形成的化合物可作水消毒劑的有__________________ (寫出其中兩種物質的化學式))。
(4) ZX的電子式為_________________;ZX與水反應放出氣體的化學方程式為_____________。
(5) 熔融狀態下,Z的單質和FeG2能組成可充電電池(裝置示意圖如下),放電時,電池的正極反應
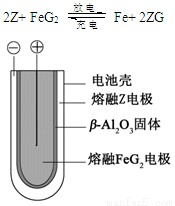
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com