
地球表面十公里厚的地層中,含鈦元素達千分之六,比銅多61倍,金屬鈦(Ti)被譽為21世紀金屬,其單質和化合物具有廣泛的應用價值。氮化鈦(Ti3N4)為金黃色晶體,由于具有令人滿意的仿金效果,越來越多地成為黃金的代替品。以TiCl4為原料,經過一系,列反應可以制得Ti3N4和納米TiO2(如下圖)。
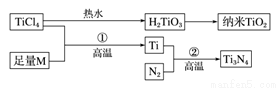
圖中的M是短周期金屬元素,M的部分電離能如下表:
I1 | I2 | I3 | I4 | I5 | |
電離能/(kJ·mol-1) | 738 | 1451 | 7733 | 10 540 | 13 630 |
請回答下列問題:
⑴TiO2為離子晶體,己知晶體中陽離子的配位數為6,陰離子的配位數為3,則陽離子的電子排布式為___________
⑵金屬Ti與金屬M的晶體原子堆積模式相同,其堆積模型為_________(填寫堆積模型名稱),晶體中原子在二維平面里的配位數為_____________
⑶室溫下TiCl4為無色液體,沸點為136.4℃,由此可知其晶體類型為__________,構成該晶體的粒子的空間構型為_____________
(4)有一種氮化鈦晶體的晶胞與NaCl晶胞相似,如下圖所示,已知該氮化鈦的密度為p g·cm-3,則該晶胞中N、Ti之間的最近距離為_____ pm,(NA為阿伏加德常數的數值,只列算式)。該晶體中與Ti原子距離相等且最近的Ti原子有___________個。
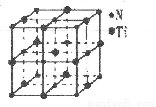
(5)科學家通過X射線探明KC1、MgO、CaO、TiN的晶體與NaCl的晶體結構相似。且知三種離子晶體的晶格能數據如下:
離子晶體 | NaCl | KC1 | CaO |
晶格能/(kJ·mol-1) | 786 | 715 | 3401 |
KC1、CaO、TiN三種離子晶體硬度由低到該的順序為_____________
 口算小狀元口算速算天天練系列答案
口算小狀元口算速算天天練系列答案科目:高中化學 來源:2016-2017學年山東省濰坊市高一下學期第一次月考模擬測試化學試卷(解析版) 題型:選擇題
9.2g金屬鈉投入到足量的重水中,則產生的氣體中含有
A. 0.2mol中子 B. 0.4mol電子 C. 0.2mol質子 D. 0.4mol分子
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖南省株洲市高一下學期第一次月考化學試卷(解析版) 題型:選擇題
下列說法正確的是
A. 由H原子形成1 mol H—H鍵要吸收能量
B. 所有燃燒的反應都是放熱反應
C. 鋁條與鹽酸的反應是吸熱反應
D. 凡經加熱而發生的化學反應都是吸熱反應
查看答案和解析>>
科目:高中化學 來源:2017屆遼寧省高三第五次模擬考試理綜化學試卷(解析版) 題型:簡答題
硒(Se),是一種非金屬元素。可以用作光敏材料、電解錳行業催化劑、動物體必需的營養元素和植物有益的營養元素等。請回答下列問題:
(1) Se原子的核外電子排布式為____________。
(2) 比較As的第一電離能比Se______(填“大”或“小”)。
(3) SeO42-中Se-O的鍵角比SeO3的鍵角____(填“大”或“小”)原因是______________
(4) H2SeO4比H2SeO3水溶液的酸性___________。
(5) 硒單質是紅色或灰色粉末,帶灰色金屬光澤的準金屬,灰硒的晶體為六方晶胞結構,原子排列為無限螺旋鏈,分布在六方晶格上,同一條鏈內原子作用很強,相鄰鏈之間原子作用較弱,其螺旋鏈狀圖、晶胞結構圖和晶胞俯視圖如下。
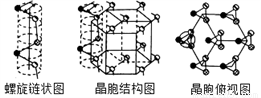
螺旋鏈中Se原子的雜化方式為__________。己知正六棱柱的邊長為acm,高為b cm,阿伏加德羅常數為NAmol-1,則該晶胞中含有的Se原子個數為_________,該晶體的密度為___________g/cm3 (用含NA、a、b的式子表示)。
查看答案和解析>>
科目:高中化學 來源:2017屆遼寧省高三第五次模擬考試理綜化學試卷(解析版) 題型:選擇題
短周期元素W、X、Y和Z的原子序數依次增大。元素W是形成化合物數量眾多,且分布極廣的元素,X原子的最外層電子數是其電子層數的3倍,元素Y是地殼中含量最豐富的金屬元素,Z元素的單質易溶于WZ2中。下列說法錯誤的是( )
A. 元素X、Y與Z的原子半徑大小:Y>Z>X
B. 元素W、Z的氯化物中,化學鍵類型相同,且各原子均滿足8電子
C. 元素X與元素Y形成的化合物是一種較好的耐火材料
D. 元素X可與元素Z可組成3種二價陰離子
查看答案和解析>>
科目:高中化學 來源:2017屆遼寧省撫順市高三3月模擬考試理科綜合化學試卷(解析版) 題型:選擇題
以下有機物同分異構體數目判斷中不正確的是
A. 立方烷( )的六氨基(-NH2)取代物有3種。
)的六氨基(-NH2)取代物有3種。
B. C3H7ClO(有羥基)的同分異構體數目有5種
C. 甲苯與氫氣充分加成后的—溴代物有4種。
D. 分子式為C5H10O2的有機物中能與NaOH溶液反應的有13種。
查看答案和解析>>
科目:高中化學 來源:2017屆浙江省寧波市高三新高考選考適應性考試化學試卷(解析版) 題型:簡答題
Fe2O3俗稱氧化鐵紅,常用作油漆等著色劑。某實驗小組用部分氧化的FeSO4為原料,以萃取劑X(甲基異丁基甲酮)萃取法制取高純氧化鐵并進行鐵含量的測定。實驗過程中的主要操作步驟如下:
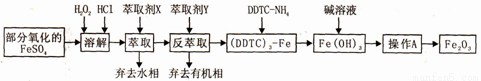
已知:①在較高的鹽酸濃度下,Fe3+能溶解于甲基異丁基甲酮,當鹽酸濃度降低時,該化合物解離。
② 3DDTC-NH4+Fe3+= (DDTC) 3-Fe↓+3NH4+
請回答下列問題:
(1)用萃取劑X萃取的步驟中,以下關于萃取分液操作的敘述中,正確的是____________。
A.FeSO4原料中含有的Ca2+、Cu2+等雜質離子幾乎都在水相中
B.為提高萃取率和產品產量,實驗時分多次萃取并合并萃取液
C.溶液中加入X,轉移至分液漏斗中,塞上玻璃塞,如圖用力振搖

D.振搖幾次后需打開分液漏斗上口的玻璃塞放氣
E.經幾次振搖并放氣后,手持分液漏斗靜置待液體分層
F.分液時,將分液漏斗上的玻璃塞打開或使塞上的凹槽對準漏斗口上的小孔,打開旋塞,待下層液體完全流盡時,關閉旋塞后再從上口倒出上層液體
(2)下列試劑中,可作反萃取的萃取劑Y最佳選擇是_______________。
A.高純水 B.鹽酸 C.稀硫酸 D.酒精
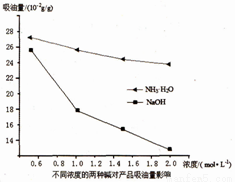
(3)吸油量是反映氧化鐵紅表面性質的重要指標。吸油量大,說明氧化鐵紅表面積較大,則用在油漆中會造成油漆假稠,影響質量。不同濃度的兩種堿溶液對產物吸油量影響如圖所示,則上述實驗過程中選用的堿溶液為_______________(填“NaOH”或“NH3·H2O”),反應的化學方程式為_________________。
(4)操作A為______________________。
(5)現準確稱取4.000g , 樣品,經酸溶、還原為Fe2+,在容量瓶中配成100mL溶液,用移液管移取25.00 mL溶液于錐形瓶中,用0.l000mol/L的K2Cr2O7溶液進行滴定(還原產物是Cr3+),消耗K2Cr2O7溶液20.80mL。
① 用移液管從容量瓶中吸取25.00mL溶液后,把溶液轉移到錐形瓶中的具體操作為_____。
② 產品中鐵的含量為_______(假設雜質不與K2Cr2O7反應)。
查看答案和解析>>
科目:高中化學 來源:2017屆浙江省寧波市高三新高考選考適應性考試化學試卷(解析版) 題型:選擇題
短周期元素W、X、Y、Z在元素周期表中的相對位置如表所示,這四種元素的原子最外層電子數之和為21。下列說法不正確的是
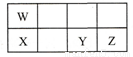
A. 原子半徑大小:X > Y > Z
B. W、Y兩種元素都能與氧元素形成化合物WO2、YO2
C. 最高價氧化物對應水化物的酸性:W > Y > Z
D. W元素的單質能從X的氧化物中置換出X單質
查看答案和解析>>
科目:高中化學 來源:2016-2017學年福建省四地六校高二下學期第一次聯考(3月)化學試卷(解析版) 題型:選擇題
下列實驗操作與結論合理的是( )
A. CH4與Cl2物質的量之比1:1混合光照充分反應可制得純凈的CH3Cl
B. 實驗室收集乙烯、乙炔均可采用向下排空氣法
C. 為得到平穩的乙炔氣流,制乙炔時用飽和食鹽水代替水
D. 濃硫酸與乙醇混合加熱至140℃,即可制得乙烯氣體
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com