
| A. | 由水電離產生的c(H+)=10-12 mol•L一1的溶液中:K+、Na+、Fe2+、NO3- | |
| B. | 常溫下,pH=7的溶液中:Al3+、Cl-、HCO3-、SO42- | |
| C. | 常溫下,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液:K+、Cu2+、S2-、Cl- | |
| D. | pH=1的溶液中:Fe3+、NO3-、SO42-、Na+ |
分析 A.由水電離產生的c(H+)=10-12 mol•L一1的溶液,為酸或堿溶液;
B.離子之間相互促進水解;
C.常溫下,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液,顯酸性;
D.pH=1的溶液,顯酸性.
解答 解:A.由水電離產生的c(H+)=10-12 mol•L一1的溶液,為酸或堿溶液,酸溶液中Fe2+、NO3-發生氧化還原反應,堿溶液中不能大量存在Fe2+,故A不選;
B.Al3+、HCO3-相互促進水解,不能共存,故B不選;
C.常溫下,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液,顯酸性,不能大量存在S2-,且S2-、Cu2+結合生成沉淀不能共存,故C不選;
D.pH=1的溶液,顯酸性,該組離子之間不反應,可大量共存,故D選;
故選D.
點評 本題考查離子的共存,為高頻考點,把握習題中的信息及常見離子之間的反應為解答的關鍵,側重分析與應用能力的考查,注意復分解反應、氧化還原反應的判斷,題目難度不大.


 開心蛙口算題卡系列答案
開心蛙口算題卡系列答案科目:高中化學 來源:2016-2017學年河北省高一上10月月考化學試卷(解析版) 題型:填空題
(1)已知16克A和20克B恰好完全反應生成0.05mol C和30克D,則C的摩爾質量為_________(2)0.3mol氨氣和0.4mol二氧化碳的質量___________(填“相等”或“不相等”,下 同),
同),
所含原子數____________。
(3)4 g H2與22.4 L(標準狀況)CO2相比,所含分子數目較多的是____________。
(4)3.01×1023個CO2分子中含 mol氧原子,在標準狀況下其體積為 L,它與 g H2O含有相同的氧原子數。
(5)寫出下列物質的電離方程式:硫酸銨__________ ____;氫氧化鋇_______ ___。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年甘肅省高二上第一次學段考試化學卷(解析版) 題型:選擇題
“綠色化學”的主要內容之一是從技術、經濟上設計可行的化學反應,使原子充分利用,不產生污染物.下列化學反應不符合“綠色化學”理念的是( )
A.制氯乙烷:CH2=CH2+HCl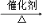 CH3CH2Cl
CH3CH2Cl
B.制甲基丙烯酸甲酯:CH3C≡CH+CO+CH3OH  CH2=C(CH3)COOCH3
CH2=C(CH3)COOCH3
C.制CuSO4:2Cu+O2 = 2CuO,CuO+H2SO4(稀)═CuSO4+H2O
D.制Cu(NO3)2:Cu+4HNO3(濃)═Cu(NO3)2+2NO2↑+2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
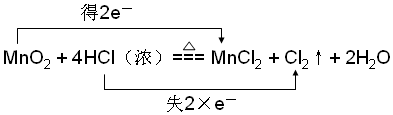 .
.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| MnO2 | 觸摸試管情況 | 觀察結果 | 反應完成所需的時間 |
| 粉末狀 | 很燙 | 劇烈反應,帶火星的木條復燃 | 3.5min |
| 塊狀 | 微熱 | 反應較慢,火星紅亮但木條未復燃 | 30min |
查看答案和解析>>
科目:高中化學 來源:2016-2017學年甘肅省高二上10月月考化學試卷(解析版) 題型:選擇題
有一支50mL酸式滴定管其中盛有溶液,液面恰好在10mL刻度處,現把管內溶液全部流下排出,用量筒承接,該溶液的體積應為
A.10mL B.40mL C.大于40mL D.小于40mL
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1s22s22p63s23p63d104s1 | B. | 1s22s22p63s23p63d64s2 | ||
| C. | 1s22s22p63s23p63d34s2 | D. | 1s22s22p63s23p63d44s2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使用催化劑,可加快反應速率,目的是提高生產效率 | |
| B. | 使用冰箱保存食物,是利用了化學反應速率理論 | |
| C. | 化學反應速率理論是研究怎樣提高原料轉化率 | |
| D. | 化學平衡理論是研究怎樣使用有限原料多出產品 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com