
| 物質 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
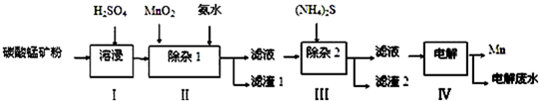
分析 向碳酸錳礦(主要成分為MnCO3,還含有鐵、鎳、鈷等碳酸鹽雜質)中加入硫酸,可以發生反應生成硫酸鹽,向其中就如具有氧化性的二氧化錳,可以將亞鐵離子氧化為鐵離子,調節pH可以將氫氧化鐵沉淀下來,向濾液中加入硫化銨,可以將鎳離子、鈷離子形成硫化物沉淀下來,最后對得到的含有錳離子的鹽電解,可以得到金屬錳,
(1)加稀硫酸時樣品中的MnCO3和硫酸反應生成可溶性的MnSO4,并產生二氧化碳和水;
(2)Mn2+離子易水解;
(3)據得失電子守恒有MnO2+2Fe2+--Mn2++2Fe3+,再據電荷守恒有MnO2+2Fe2++4H+--Mn2++2Fe3+,最后據原子守恒得MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
(4)根據操作方法判斷缺少的儀器;由于在第一次過濾之后的濾液中含有Mn2+、Ni2+、Co2+,向其中加入(NH4)2S,根據各物質的溶度積常數可確定有CoS和NiS沉淀(濾渣2)生成;
(5)由于將一級沉降根據MnS的Ksp=c(Mn2+)•c(S2-)進行計算即可.
解答 解:向碳酸錳礦(主要成分為MnCO3,還含有鐵、鎳、鈷等碳酸鹽雜質)中加入硫酸,可以發生反應生成硫酸鹽,向其中就如具有氧化性的二氧化錳,可以將亞鐵離子氧化為鐵離子,調節pH可以將氫氧化鐵沉淀下來,向濾液中加入硫化銨,可以將鎳離子、鈷離子形成硫化物沉淀下來,最后對得到的含有錳離子的鹽電解,可以得到金屬錳,
(1)加稀硫酸時樣品中的MnCO3和硫酸反應生成可溶性的MnSO4,并產生二氧化碳和水,步驟Ⅰ中,MnCO3與硫酸反應的化學方程式為:MnCO3+H2SO4=MnSO4+CO2↑+H2O,
故答案為:MnCO3+H2SO4=MnSO4+CO2↑+H2O;
(2)Mn2+離子易水解.加入過量硫酸,還可以抑制Mn2+的水解,
故答案為:抑制Mn2+的水解;
(3)步驟Ⅱ中,MnO2在酸性條件下可將Fe2+離子氧化為Fe3+,反應的離子方程式是據得失電子守恒有MnO2+2Fe2+-Mn2++2Fe3+,再據電荷守恒有MnO2+2Fe2++4H+-Mn2++2Fe3+,最后據原子守恒得,MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O,
故答案為:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
(4)步驟Ⅲ為過濾操作,需要用到的玻璃儀器除玻璃棒、漏斗外,還需要燒杯;
由于在第一次過濾之后的濾液中含有Mn2+、Ni2+、Co2+,向其中加入(NH4)2S,根據各物質的溶度積常數可確定有CoS和NiS沉淀(濾渣2)生成,
故答案為:燒杯;CoS和NiS;
(5)MnS的Ksp=c(Mn2+)•c(S2-)=1.0×10-11,為了將Mn2+降到1.0×10-5mol/L,則c(S2-)=$\frac{K{\;}_{sp}}{c(Mn{\;}^{2+})}$=$\frac{1.0×10{\;}^{-11}}{1.0×10{\;}^{-5}}$=1.0×10-6mol/L,即硫化鈉的濃度是1.0×10-6mol/L,
故答案為:1.0×10-6.
點評 本題考查了制備方案的設計,題目難度中等,根據制備流程明確制備原理為解答關鍵,注意掌握難溶物溶解平衡及溶度積的有關計算方法,試題培養了學生的分析、理解能力及化學實驗能力.


科目:高中化學 來源: 題型:推斷題
 R可以被KMnO4的酸性溶液氧化生成
R可以被KMnO4的酸性溶液氧化生成 COOH,但若烷基R中直接與苯環連接的碳原子上沒有C-H鍵,則不容易被氧化得到
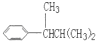
COOH,但若烷基R中直接與苯環連接的碳原子上沒有C-H鍵,則不容易被氧化得到 COOH.現有分子式是C11H16的一烷基取代苯,已知它可以被氧化成為
COOH.現有分子式是C11H16的一烷基取代苯,已知它可以被氧化成為 COOH的異構體共有7種,其中的3種是:
COOH的異構體共有7種,其中的3種是: CH2CH2CH2CH2CH3,
CH2CH2CH2CH2CH3,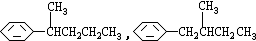
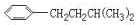 ,
,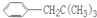 ,
, ,
, .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 23gNa在氧氣中完全燃燒失去NA個電子 | |
| B. | 常溫常壓下,6.2g Na2O含有的Na+離子數為0.2 NA | |
| C. | 標準狀況下,22.4LH2O含有NA個分子 | |
| D. | 1L0.5 mol/LFe2(SO4)3溶液中,SO42-的數目為1.5NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
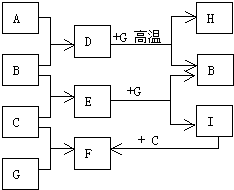 單質A、B、C在常溫下均為氣態,分別由甲、乙、丙三種短周期元素組成;丙元素的原子結構中次外層電子數比最外層電子數多1;G是常見的金屬單質,D在常溫下為液態,H是一種黑色晶體.各物質間的轉化關系如圖所示(反應條件多數已略去).
單質A、B、C在常溫下均為氣態,分別由甲、乙、丙三種短周期元素組成;丙元素的原子結構中次外層電子數比最外層電子數多1;G是常見的金屬單質,D在常溫下為液態,H是一種黑色晶體.各物質間的轉化關系如圖所示(反應條件多數已略去).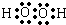 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 4.18 g | B. | 3.12 g | C. | 4.68 g | D. | 5.08 g |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com