
| A. | 完全氧化56gFe需要消耗氯氣33.6 L | |
| B. | 某濃度氫氧化鈉溶液恰好溶解5.4g的鋁,則被還原的水的分子數為0.6NA | |
| C. | 向100mL 1mol/L的NaHSO3溶液中加入足量的硫酸鐵,則反應后氫離子增加0.4mol | |
| D. | 利用鋁熱反應將磁鐵礦還原得到16.8g鐵單質,反應中Fe得到了0.9 NA電子 |
分析 A、氯氣所處的狀態不明確;
B、求出鋁的物質的量,然后根據鋁和氫氧化鈉溶液反應時,做氧化劑的為水分子來分析;
C、NaHSO3溶液中加入足量的硫酸鐵,發生的反應為:HSO3-+2Fe2++H2O=2Fe3++SO42-+3H+;
D、根據鐵的質量計算出物質的量,再計算出轉移的電子數.
解答 解:A、氯氣所處的狀態不明確,故消耗的氯氣的體積無法計算,故A錯誤;
B、5.4g鋁的物質的量為0.2mol,而鋁和氫氧化鈉溶液反應時,做氧化劑的為水分子:2Al+2NaOH+6H2O=2NaAlO2+4H2O+3H2↑,且從反應可以看出,當2mol鋁參與反應時,做氧化劑的水為6mol,故當0.2mol鋁反應時,被還原的水分子為0.6NA,故B正確;
C、NaHSO3溶液中加入足量的硫酸鐵,發生的反應為:HSO3-+2Fe2++H2O=2Fe3++SO42-+3H+,由于HSO3-能微弱電離出氫離子,故當1molHSO3-反應時,增加的氫離子小于3mol,故當0.1molNaHSO3完全反應時,反后增加的氫離子小于0.3mol,故C錯誤;
D、16.8g鐵單質的物質的量為0.3mol,由于鐵元素反應前為+$\frac{8}{3}$價,反應后變為0價,故當生成0.3mol鐵單質時,鐵元素得到0.8NA個電子,故D錯誤.
故選B.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


科目:高中化學 來源: 題型:實驗題
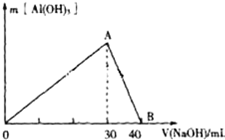 某無色廢水中可能含有Fe3+、Al3+、Na+、Cl-、OH-、SO42-、中的幾種離子.分別取三份廢水進行如下實驗:
某無色廢水中可能含有Fe3+、Al3+、Na+、Cl-、OH-、SO42-、中的幾種離子.分別取三份廢水進行如下實驗:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 、④HCHO等,其中碳原子不是采取sp2雜化的分子有②(填物質編號),HCHO分子的立體構型為平面三角形.
、④HCHO等,其中碳原子不是采取sp2雜化的分子有②(填物質編號),HCHO分子的立體構型為平面三角形.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
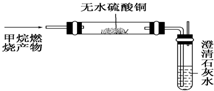 (1)我國西周年代寫成的算卦占卜的書《周易》中,在談到一些自然界發生的現象時說:“象曰:‘澤中有火’”試用化學方程式表示出澤中有火的化學反應CH4+2O2$\stackrel{點燃}{→}$CO2+2H2O.西氣東輸是我國油氣管道建設史上距離最長的輸氣管道,總長3900公里,設計年輸氣量120億立方米.這里說的氣就是天然氣,天然氣的主要成分是甲烷(填名稱),試分析使用天然氣的優點清潔無污染.
(1)我國西周年代寫成的算卦占卜的書《周易》中,在談到一些自然界發生的現象時說:“象曰:‘澤中有火’”試用化學方程式表示出澤中有火的化學反應CH4+2O2$\stackrel{點燃}{→}$CO2+2H2O.西氣東輸是我國油氣管道建設史上距離最長的輸氣管道,總長3900公里,設計年輸氣量120億立方米.這里說的氣就是天然氣,天然氣的主要成分是甲烷(填名稱),試分析使用天然氣的優點清潔無污染.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.21 mol | B. | 0.25 mol | C. | 0.3 mol | D. | 0.35 mol |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com