
| A. | 常溫常壓下,22.4 LCO2含有的原子數為3NA | |
| B. | 0.1 mol Na2O2固體含有的陰、陽離子總數是0.3NA | |
| C. | 1.8gNH4+含有的質子數為NA | |
| D. | 標準狀況下,2.24 L NO與1.12 L O2混合,所得氣體中分子數為0.15NA |
分析 A.常溫常壓下,不能使用標況下的氣體摩爾體積計算二氧化碳的物質的量;
B.0.1mol過氧化鈉中含有0.2mol鈉離子、0.1mol過氧根離子;
C.銨根離子中含有11個質子,1.8g銨根離子的物質的量為0.1mol,含有1.1mol質子;
D.NO和氧氣反應生成二氧化氮,導致混合氣體的分子數減少.
解答 解:A.不是標況下,不能使用標況下的氣體摩爾體積計算22.4L二氧化碳的物質的量,故A錯誤;
B.0.1mol過氧化鈉固體中含有0.2mol鈉離子、0.1mol過氧根離子,總共含有0.3mol離子,含有的陰、陽離子總數是0.3NA,故B正確;
C.1.8g銨根離子的物質的量為:$\frac{1.8g}{18g/mol}$=0.1mol,0.1mol銨根離子中含有的質子為:0.1mol×11=1.1mol,含有的質子數為1.1NA,故C錯誤;
D.標況下2.24L一氧化氮的物質的量為0.1mol,1.12L氧氣的物質的量為0.05mol,由于二者混合后發生反應生成二氧化氮,則混合氣體的物質的量堿性,故D錯誤;
故選B.
點評 本題考查阿伏加德羅常數的應用,題目難度中等,注意明確標況下氣體摩爾體積的使用條件,掌握好以物質的量為中心的各化學量與阿伏加德羅常數的關系,準確弄清分子、原子、原子核內質子中子及核外電子的構成關系.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題

| A. | 溶液中一定不存在CO32- | B. | 溶液中一定不存在Fe3+ | ||
| C. | 溶液中一定存在K+ | D. | 溶液中c(NO3-)=0.1mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
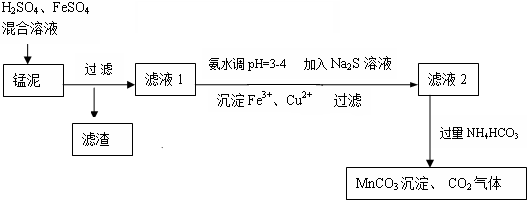
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 一定有乙烯 | B. | 可能有乙烯 | C. | 一定沒有甲烷 | D. | 可能有乙烷 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 質子數是94 | B. | 原子序數是239 | C. | 質量數是94 | D. | 中子數是239 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH4H是離子化合物 | |
| B. | NH4H溶于水形成的溶液呈堿性 | |
| C. | NH4H與水反應時,NH4H是氧化劑 | |
| D. | NH4H固體投入少量水中,可能有兩種氣體產生 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 8n | B. | 18n | C. | 14n | D. | 44n |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
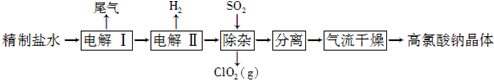
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | OCS中含有1個σ鍵和1個π鍵 | |
| B. | OCS高溫分解時,碳元素化合價升高 | |
| C. | OCS、C02、CO、S晶體類型相同 | |
| D. | 22.4LOCS中約含有3×6.02×1023個原子 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com