
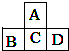
 A、B、C、D為短周期元素,它們的位置關(guān)系如圖所示,已知B、D兩元素原子序數(shù)之和是A元素的原子序數(shù)的4倍,則下列敘述中正確的是( )
A、B、C、D為短周期元素,它們的位置關(guān)系如圖所示,已知B、D兩元素原子序數(shù)之和是A元素的原子序數(shù)的4倍,則下列敘述中正確的是( )

 探究與鞏固河南科學(xué)技術(shù)出版社系列答案
探究與鞏固河南科學(xué)技術(shù)出版社系列答案
| 年級(jí) | 高中課程 | 年級(jí) | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源: 題型:
查看答案和解析>>
科目:高中化學(xué) 來源:2012屆寧夏銀川一中高三第三次模擬考試化學(xué)試卷(帶解析) 題型:填空題
【化學(xué)一選修3:物質(zhì)結(jié)構(gòu)與性質(zhì)】(15分)
現(xiàn)有六種元素,其中A、B、C、D為短周期主族元素,E、F為第四周期元素,它們的原子序數(shù)依次增大。請(qǐng)根據(jù)下列相關(guān)信息,回答問題.
| A元素原子的核外p電子總數(shù)比s電子總數(shù)少1 |
| B元素原子核外s電子總數(shù)與p電子總數(shù)相等,且不與A元素在同一周期 |
| C原子核外所有p軌道全滿或半滿 |
| D元素的主族序數(shù)與周期數(shù)的差為4 |
| E是前四周期中電負(fù)性最小的元素 |
| F在周期表的第七列 |

查看答案和解析>>
科目:高中化學(xué) 來源:2014屆黑龍江省高二下學(xué)期期末考試化學(xué)試卷(解析版) 題型:填空題
現(xiàn)有六種元素,其中A、B、C、D為短周期主族元素,E、F為第四周期元素,它們的原子序數(shù)依次增大。請(qǐng)根據(jù)下列相關(guān)信息,回答問題.
A原子核外電子分占3個(gè)不同能級(jí),且每個(gè)能級(jí)上排布的電子數(shù)相同
B元素原子的核外p電子總數(shù)比s電子總數(shù)少1
C原子p軌道上成對(duì)電子數(shù)等于未成對(duì)電子數(shù),且與A同周期
D元素的族序數(shù)與周期數(shù)的差為4,且不與A元素在同一周期
E位于周期表中第七列
F元素基態(tài)原子的M層全充滿,N層沒有成對(duì)電子,只有一個(gè)未成對(duì)電子
(1)A的基態(tài)原子最外層有 種不同運(yùn)動(dòng)狀態(tài)的電子,F(xiàn)位于 區(qū)。
(2)E2+的基態(tài)核外電子排布式為 ,AD4為 (填極性或非極性)分子。
(3)A、B、C三種元素的電負(fù)性由小到大的順序是 (用元素符號(hào)表示),B和C兩元素中,B的第一電離能較大的原因是 ,與AC2互為等電子體的分子的名稱為 。(只寫一種)
(4)BD3 中心原子的雜化方式為 ,其分子空間構(gòu)型為 。
(5)用晶體的x射線衍射法對(duì)F的測定得到以下結(jié)果:F的晶胞為面心立方最密堆積(如圖),又知該晶體的密度為ρg/cm3,晶胞中該原子的配位數(shù)為 ;F的原子半徑是 pm;(阿伏加德羅常數(shù)為NA)。

查看答案和解析>>
科目:高中化學(xué) 來源:2014屆河北省衡水市高二下學(xué)期期末考試化學(xué)試卷(解析版) 題型:填空題
現(xiàn)有六種元素,其中A、B、C、D為短周期主族元素,E、F為第四周期元素,它們的原子序數(shù)依次增大。請(qǐng)根據(jù)下列相關(guān)信息,回答問題。
A元素原子的核外p電子總數(shù)比s電子總數(shù)少1
B元素原子核外s電子總數(shù)與p電子總數(shù)相等,且不與A元素在同一周期
C原子核外所有p軌道全滿或半滿
D元素的主族序數(shù)與周期數(shù)的差為4
E是前四周期中電負(fù)性最小的元素
F在周期表的第七列
⑴A基態(tài)原子中能量最高的電子,其電子云在空間有 個(gè)方向,原子軌道呈 形。
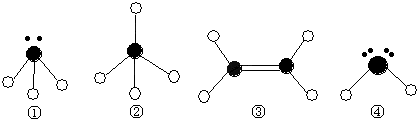
⑵某同學(xué)根據(jù)上述信息,所畫的B電子排布圖如圖 ,違背了 原理。
,違背了 原理。
⑶F位于 族 區(qū),其基態(tài)原子有 種運(yùn)動(dòng)狀態(tài)。
⑷CD3 中心原子的雜化方式為 ,用價(jià)層電子對(duì)互斥理論推測其分子空間構(gòu)型為 ,檢驗(yàn)E元素的方法是 。
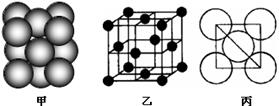
⑸若某金屬單質(zhì)晶體中原子的堆積方式如下圖甲所示,其晶胞特征如下圖乙所示,原子之間相互位置關(guān)系的平面圖如下圖丙所示。則晶胞中該原子的配位數(shù)為 ,該單質(zhì)晶體中原子的堆積方式為四種基本堆積方式中的 。若已知該金屬的原子半徑為d cm,NA代表阿伏加德羅常數(shù),金屬的相對(duì)原子質(zhì)量為M,則該晶體的密度為______g·cm-3(用字母表示)。
查看答案和解析>>
科目:高中化學(xué) 來源:2011-2012學(xué)年寧夏高三第三次模擬考試化學(xué)試卷(解析版) 題型:填空題
【化學(xué)一選修3:物質(zhì)結(jié)構(gòu)與性質(zhì)】(15分)
現(xiàn)有六種元素,其中A、B、C、D為短周期主族元素,E、F為第四周期元素,它們的原子序數(shù)依次增大。請(qǐng)根據(jù)下列相關(guān)信息,回答問題.
|
A元素原子的核外p電子總數(shù)比s電子總數(shù)少1 |
|
B元素原子核外s電子總數(shù)與p電子總數(shù)相等,且不與A元素在同一周期 |
|
C原子核外所有p軌道全滿或半滿 |
|
D元素的主族序數(shù)與周期數(shù)的差為4 |
|
E是前四周期中電負(fù)性最小的元素 |
|
F在周期表的第七列 |
(1)A基態(tài)原子中能量最高的電子,其電子云在空間有 個(gè)方向,原子軌道呈
形
(2)某同學(xué)根據(jù)上述信息,所畫的B電子排布圖如圖
違背了 原理。
(3)F位于 族 區(qū),其基態(tài)原子有 種運(yùn)動(dòng)狀態(tài)。
(4)CD3 中心原子的雜化方式為 ,用價(jià)層電子對(duì)互斥理論推測其分子空間構(gòu)型為 .檢驗(yàn)E元素的方法是
(5)若某金屬單質(zhì)晶體中原子的堆積方式如下圖甲所示,其晶胞特征如下圖乙所示,原子之間相互位置關(guān)系的平面圖如下圖丙所示。則晶胞中該原子的配位數(shù)為 ,該單質(zhì)晶體中原子的堆積方式為四種基本堆積方式中的 .

查看答案和解析>>
百度致信 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com