
【題目】(1)鋁土礦(主要成分為Al2O3,還含有SiO2、Fe2O3)是工業上制備氧化鋁的主要原料。工業上提取氧化鋁的工藝流程如下:
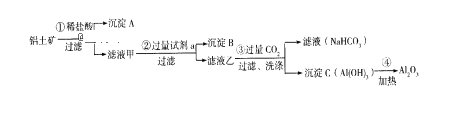
①沉淀A、B的成分分別是______、______;步驟②中的試劑a是_____;(以上均填化學式)。
②試寫出步驟③中生成沉淀C的離子方程式________________;
③簡述檢驗所得濾液甲中存在Fe3+的操作方法:______________。
(2)用含少量鐵的氧化銅制取氯化銅晶體(CuCl2xH2O)。有如下操作:
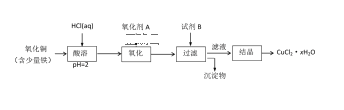
已知:在pH為4~5時,Fe3+幾乎完全轉化為Fe(OH)3沉淀,Cu2+卻不反應。
①試劑B可選用______(填編號)。
A.NaOH溶液 B.CuO C.濃氨水 D.Cu2(OH)2CO3
②若氧化劑A是H2O2溶液,寫出加入氧化劑A發生反應的離子方程式________
③從濾液經過結晶得到氯化銅晶體的方法是________
【答案】SiO2 Fe(OH)3 NaOH CO2 +AlO2- +2H2O=Al(OH)3 ↓+HCO3- 取少量溶液于試管中,滴入幾滴KSCN溶液,觀察溶液顏色,如果溶液顏色變為血紅色,說明溶液中含有Fe3+,否則不含Fe3+ BD 2Fe2++2H2O2+2H+=2Fe3++2H2O 蒸發濃縮、冷卻結晶、(過濾)
【解析】
(1)根據流程圖,鋁土礦加入稀鹽酸,Al2O3、Fe2O3能與鹽酸反應生成氯化鋁和氯化鐵, SiO2與鹽酸不反應,過濾得沉淀SiO2;濾液甲中含有氯化鋁和氯化鐵,濾液甲加入過量的氫氧化鈉溶液,氯化鋁與氫氧化鈉反應生成偏鋁酸鈉和水、氯化鐵與氫氧化鈉反應生成氫氧化鐵沉淀,過濾得沉淀氫氧化鐵;濾液乙中含有偏鋁酸鈉,向偏鋁酸鈉溶液中通入過量的二氧化碳氣體,生成氫氧化鋁沉淀和碳酸氫鈉。氫氧化鋁加熱分解為氧化鋁。
(2)含少量鐵的氧化銅加入鹽酸,生成氯化亞鐵和氯化鐵溶液;溶液中通入氯氣把氯化亞鐵氧化為氯化鐵,加入試B調節pH為4~5,Fe3+完全轉化為Fe(OH)3沉淀,過濾得氯化銅溶液,在氯化氫氣流中蒸發溶液得氯化銅晶體。
(1)①根據以上分析,鋁土礦中SiO2與鹽酸不反應,所以沉淀甲是SiO2;濾液甲加入過量的氫氧化鈉溶液,氯化鐵與過量氫氧化鈉反應生成氫氧化鐵沉淀,沉淀乙是Fe(OH)3;根據氫氧化鋁溶于強堿,所以步驟②中的試劑a是NaOH;
②步驟③中偏鋁酸鈉溶液與過量的二氧化碳氣體反應,生成氫氧化鋁沉淀和碳酸氫鈉,反應離子方程式是CO2 +AlO2- +2H2O=Al(OH)3 ↓+HCO3-;
③Fe3+遇KSCN溶液變紅,所以檢驗所得濾液甲中存在Fe3+的操作是:取少量溶液于試管中,滴入幾滴KSCN溶液,觀察溶液顏色,如果溶液顏色變為血紅色,說明溶液中含有Fe3+,否則不含Fe3+;
(2)①加入試劑B的目的是調節pH為4~5除去氯化銅中Fe3+; A.加入NaOH溶液,引入雜質離子Na+ B.加入CuO能消耗氫離子,使pH升高,不引入雜質離子; C.加入濃氨水,引入雜質離子NH4+;D.加入 Cu2(OH)2CO3能消耗氫離子,使pH升高,不引入雜質離子,故選BD;
②若氧化劑A是H2O2溶液,H2O2把Fe2+氧化為Fe3+,發生反應的離子方程式是2Fe2++2H2O2+2H+=2Fe3++2H2O;
③從濾液經過結晶得到氯化銅晶體,首先要加熱蒸發濃縮,冷卻結晶,再過濾即可。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
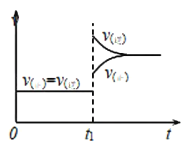
【題目】對于反應![]() ,減小壓強,平衡向______(填“正反應”或“逆反應”)方向移動,平衡混合氣體的平均相對分子質量在平衡移動時______(填“是”或“否”)發生改變,其原因是____________;下圖是反應速率與時間的關系圖,
,減小壓強,平衡向______(填“正反應”或“逆反應”)方向移動,平衡混合氣體的平均相對分子質量在平衡移動時______(填“是”或“否”)發生改變,其原因是____________;下圖是反應速率與時間的關系圖,![]() 時刻引起正、逆反應速率變化的原因可能是____________(寫一條合理原因)。
時刻引起正、逆反應速率變化的原因可能是____________(寫一條合理原因)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究性學習小組為合成1丁醇,查閱資料得知一條合成路線:CH3CH===CH2+CO+H2→CH3CH2CH2CHO![]() CH3CH2CH2CH2OH,CO的制備原理:HCOOH
CH3CH2CH2CH2OH,CO的制備原理:HCOOH![]() CO↑+H2O,并設計出原料氣的制備裝置(如圖)。
CO↑+H2O,并設計出原料氣的制備裝置(如圖)。
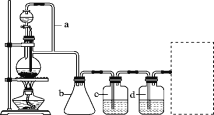
請填寫下列空白:
(1)實驗室現有鋅粒、稀硝酸、稀鹽酸、濃硫酸、2丙醇,從中選擇合適的試劑制備氫氣、丙烯。寫出化學方程式:______________________________________________。
(2)若用以上裝置制備干燥純凈的CO,裝置中a和b的作用分別是________、________;c和d中盛裝的試劑分別是________、________。
(3)制丙烯時,還產生少量SO2、CO2及水蒸氣,該小組用以下試劑檢驗這四種氣體,混合氣體通過試劑的順序是________(填序號)。
①飽和Na2SO3溶液 ②酸性KMnO4溶液 ③石灰水 ④無水CuSO4 ⑤品紅溶液
(4)合成正丁醛的反應為正向放熱的可逆反應,為增大反應速率和提高原料氣的轉化率,你認為應該采用的適宜反應條件是________。
a.低溫、高壓、催化劑 b.適當的溫度、高壓、催化劑
c.常溫、常壓、催化劑 d.適當的溫度、常壓、催化劑
(5)正丁醛經催化加氫得到含少量正丁醛的1丁醇粗品,為純化1丁醇,該小組查閱文獻得知:①R—CHO+NaHSO3(飽和)―→RCH(OH)SO3Na↓;②沸點:乙醚 34 ℃,1丁醇 118 ℃,并設計出如下提純路線:
粗品![]() 濾液
濾液![]() 有機層
有機層![]() 1丁醇、乙醚
1丁醇、乙醚![]() 純品
純品
試劑1為________,操作1為________,操作2為________,操作3為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硼和氮的單質及一些化合物在工農業生產等領域有重要應用。回答下列問題:
(1)N原子核外有___ 種不同運動狀態的電子。基態N原子中,能量最高的電子所占據的原子軌道的形狀為____________________________。
(2)經測定發現,N2O5固體由NO2+ 和NO3-兩種離子組成,該固體中N原子雜化類型為_________;與NO2+互為等電子體的微粒有_______(寫出一種)。
(3)HF和HI電離出H+較難的是________(填化學式,下同)。銨鹽大多不穩定,請預測NH4F、NH4I中,較易分解的是________。
(4)第二周期中,第一電離能介于B元素和N元素間的元素為_____(填“元素符號”)。
(5)晶體硼有多種變體,但其基本結構單元都是由硼原子組成的正二十面體( 見圖I),每個頂點為一個硼原子,每個三角形均為等邊三角形。則每一個此基本結構單元由_______個硼原子構成;若該結構單元中有2 個原子為10B(其余為11B),那么該結構單元有_____種不同類型。
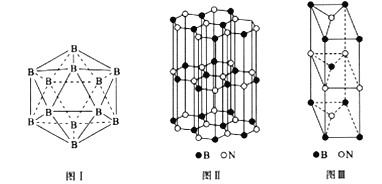
(6)硼和氮構成的一種氮化硼晶體的結構與石墨晶體結構相類似,B、N原子相互交替排列(見圖II),其晶胞結構如圖III所示。該晶胞有_____個B和_____個N。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】t ℃時,某平衡體系中含有X、Y、Z、W四種物質,此溫度下發生反應的平衡常數表達式為K=![]() 。有關該平衡體系的說法正確的是
。有關該平衡體系的說法正確的是
A. 當混合氣體的平均相對分子質量保持不變時,反應達平衡
B. 增大壓強,各物質的濃度不變
C. 升高溫度,平衡常數K增大
D. 增加X的量,平衡既可能正向移動,也可能逆向移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】羰基硫(COS)可作為一種糧食熏蒸劑,能防止某些昆蟲、線蟲和真菌的危害。在恒容密閉容器中,將CO和H2S混合加熱并達到下列平衡:CO(g)+H2S(g)![]() COS(g)+H2(g) K=0.1。反應前CO物質的量為10mol,平衡后CO物質的量為8mol。下列說法正確的是( )
COS(g)+H2(g) K=0.1。反應前CO物質的量為10mol,平衡后CO物質的量為8mol。下列說法正確的是( )
A. 平衡后若升高溫度,H2S濃度增加,表明該反應是吸熱反應
B. 當體系的壓強保持不變時,表明該反應達到化學平衡狀態
C. CO的平衡轉化率為80%
D. 反應前H2S物質的量為7mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表為元素周期表的一部分,請參照元素①~⑨在表中的位置,回答下列問題:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)③、④、⑧的原子半徑由大到小的順序為:______(用元素符號回答)。
(2)⑤、⑥、⑦的最高價氧化物對應的水化物堿性由強到弱的順序是:______。(用化學式回答)
(3)②和⑨兩種元素成的某化合物是一種常見的有機溶劑,則該化合物的電子式為:______ 。
(4)④和⑧形成的化合物屬于______晶體(填“離子”、“分子”、“原子”),該晶體中微粒間的作用力為:______。
(5)②形成的單質與③形成的最高價氧化物的水化物的濃溶液發生化學反應的方程式為:________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】檸檬烯是一種食用香料,其結構簡式如圖所示。有關檸檬烯的分析正確的是
![]()
A.一定條件下,它分別可以發生加成、取代、氧化、還原等反應
B.它和丁基苯(![]() )互為同分異構體
)互為同分異構體
C.它的分子中所有的碳原子一定在同一平面上
D.它的一氯代物有6種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗題:
1-溴丙烷是一種重要的有機合成中間體,沸點為71℃,密度為1.36g·cm-3。實驗室制備少量 1-溴丙烷的主要步驟如下:
步驟 1:在儀器 A 中加入攪拌磁子、12g 正丙醇及 20mL水,冰水冷卻下緩慢加入 28ml濃 H2SO4;冷卻至室溫,攪拌下加入 24gNaBr。
(已知: ①2NaBr+H2SO4(濃)![]() Na2SO4+2HBr↑
Na2SO4+2HBr↑
②正丙醇和濃硫酸共熱會產生丙烯、醚等副產品)
步驟 2:如圖所示搭建實驗裝置,緩慢加熱,直到無油狀物餾出為止。
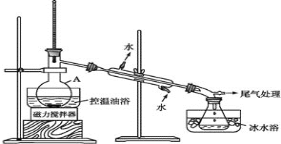
步驟 3:將餾出液轉入分液漏斗,分出有機相。
步驟 4:將分出的有機相轉入分液漏斗,依次用 12mLH2O、12ml5%Na2CO3 溶液和12mLH2O 洗滌,分液,得粗產品,進一步提純得 1-溴丙烷。
(1)儀器 A 的名稱是_____;
(2)反應時生成的主要有機副產物 2-溴丙烷和_______(答出一種即可給分)
(3)步驟 2 中需向接收瓶內加入少量冰水并置于冰水浴中的目的是____。
(4)步驟 1 中濃 H2SO4 用水稀釋,待冷卻至室溫后再加 NaBr 的目的是______。步驟 4 中用 Na2CO3 溶液洗滌的目的是_____。
(5)步驟 4 中進一步提純 1-溴丙烷的方法是_________;在進行此操作之前需要 用無水MgBr2 處理粗產品,其目的是_____。
(6)1-溴丙烷在一定條件下也可以制備 1-丙醇,請寫出由產物 1-溴丙烷制備 1-丙醇的化學反應方程式________________________ 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com