
下列說法中錯誤的是( )。
| A.質子數相同的原子,其核外電子排布也相同 |
| B.質量數相同的不同原子,其化學性質一定相同 |
| C.金屬性越強,其原子在反應中越易得到電子 |
| D.非金屬性越強,其陰離子越難失去電子 |
 全程金卷系列答案
全程金卷系列答案科目:高中化學 來源: 題型:單選題
元素R、X、T、Z、Q在元素周期表中的相對位置如下表所示, 其中R單質在暗處與H2劇烈化合并發生爆炸。則下列判斷正確的是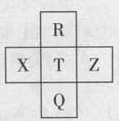
| A.非金屬性:Z<T<X |
| B.R與Q的電子數相差26 |
| C.氣態氫化物穩定性:R <T<Q |
| D.最高價氧化物的水化物的酸性:T>Q |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
已知X、Y均為1~18號之間的元素,X、Y可形成化合物X2Y和X2Y2,又知Y的原子序數小于X的原子序數,則兩種元素的原子序數之和為( )
| A.19 | B.18 | C.27 | D.9 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
A元素的最高價離子0.5 mol被還原成中性原子時,要得到6.02×1023個電子。它的單質同鹽酸充分反應時,放出0.02 g H2,用去0.4 g A。B元素的原子核外電子層數與A相同,且B元素形成的單質是紅棕色液體。
(1)寫出這兩種元素的名稱:A ,B 。
(2)用結構示意圖表示A、B兩元素常見離子:A ,B 。
(3)用電子式表示A、B形成的化合物。
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
原子結構決定元素的性質,下列說法中,正確的是
| A.Na、Al、Cl的原子半徑依次減小,Na+、Al3+、Cl-的離子半徑也依次減小 |
| B.在第ⅥA族元素的氫化物(H2R)中,熱穩定性最強的其沸點也一定最高 |
| C.第2周期元素的最高正化合價都等于其原子的最外層電子數 |
| D.非金屬元素的非金屬性越強,其氧化物對應水化物的酸性也一定越強 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
現有A、B、C、D四種短周期非金屬元素,原子最外層電子數之和為19。在化合物中,這四種元素常見化合價均不止一種,但有一種相同的化合價。其部分性質如下:
| 元素 | A | B | C | D |
| 原子半徑/nm | 0.102 | 0.077 | 0.117 | 0.075 |
| 最高正價或最低負價 | +6 | -4 | +4 | -3 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
已知碳有兩種常見的同位素12C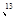 C;氧也有常見的三種同位素16O、17O、18O。由這5種粒子構成的二氧化碳分子中,其相對分子質量最多可能有( )。
C;氧也有常見的三種同位素16O、17O、18O。由這5種粒子構成的二氧化碳分子中,其相對分子質量最多可能有( )。
| A.6種 | B.10種 | C.11種 | D.12種 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com