
【題目】已知某溶液中含有下列8種離子中的5種(忽略水的電離及離子的水解):K+、Cu2+、Al3+、Fe2+、Cl﹣、CO32﹣、NO3﹣、SO42﹣ , 且5種離子的物質的量濃度相等.為了進一步探究該水溶液的組成,某同 學進行了如下實驗:
①用鉑絲蘸取少量溶液,在火焰上灼燒,透過藍色鈷玻璃觀察無紫色火焰.
②另取溶液加入足量鹽酸,有無色氣體生成,該無色氣體遇空氣變成紅棕色.
③另取溶液加入BaCl2溶液,有白色沉淀生成.
根據上述實驗,以下推測正確的是( )
A.無法確定溶液中是否存在Cu2+離子
B.原溶液中不含K+、Al3+、CO![]() 等離子
等離子
C.根據步驟②只能確定溶液中一定存在NO3﹣離子
D.步驟③所得到的白色沉淀共有2種鋇鹽
【答案】B
【解析】解:用鉑絲蘸取少量溶液,在火焰上灼燒,透過藍色鈷玻璃觀察無紫色火焰,則說明沒有K+;
另取溶液加入足量稀鹽酸,有無色氣體生成,該無色氣體遇空氣變成紅棕色,則說明含有具有氧化性的NO3﹣和還原性的Fe2+;
若向溶液中加入BaCl2溶液,有白色沉淀生成,說明原溶液中含有CO32﹣或SO42﹣ , 因為有Fe2+ , Fe2+與CO32﹣不能共存,所以沒有CO32﹣;
則溶液中的離子有Fe2+、NO3﹣、SO42﹣ ,
已知各種離子的物質的量濃度相等,陰離子電荷比陽離子電荷多,所以還有另外的陽離子Cu2+或Al3+ , 若有Cu2+ , 陽離子的電荷多還須有Cl﹣ , 若有Al3+ , 陰離子加上Cl﹣ , 電荷仍不守恒;
所以根據電荷守恒可知還有Cu2+、Cl﹣ ,
所以原溶液中所含的離子為:Cu2+、Fe2+、Cl﹣、NO3﹣、SO42﹣ , 一定不含:K+、Al3+、CO32﹣離子;
A.Cu2+一定存在,故A錯誤;
B.根據以上分析,原溶液中不含的離子為:K+、Al3+、CO32﹣ , 故B正確;
C.步驟②是另取溶液加入足量稀鹽酸,有無色氣體生成,該無色氣體遇空氣變成紅棕色,則說明含有具有氧化性的NO3﹣和還原性的Fe2+ , 無CO32﹣ , 故C錯誤;
D.另取溶液加入BaCl2溶液,只生成硫酸鋇沉淀,故D錯誤;
故選B.
用鉑絲蘸取少量溶液,在火焰上灼燒,透過藍色鈷玻璃觀察無紫色火焰,則說明沒有K+;
另取溶液加入足量稀鹽酸,有無色氣體生成,該無色氣體遇空氣變成紅棕色,則說明含有具有氧化性的NO3﹣和還原性的Fe2+;
若向溶液中加入BaCl2溶液,有白色沉淀生成,說明原溶液中含有CO32﹣或SO42﹣ , 因為有Fe2+ , Fe2+與CO32﹣不能共存,所以沒有CO32﹣;
則溶液中的離子有Fe2+、NO3﹣、SO42﹣ ,
已知各種離子的物質的量濃度相等,陰離子電荷比陽離子電荷多,所以還有另外的陽離子Cu2+或Al3+ , 若有Cu2+ , 陽離子的電荷多還須有Cl﹣ , 若有Al3+ , 陰離子加上Cl﹣ , 電荷仍不守恒;
所以根據電荷守恒可知還有Cu2+、Cl﹣ ,
所以原溶液中所含的離子為:Cu2+、Fe2+、Cl﹣、NO3﹣、SO42﹣ , 一定不含:K+、Al3+、CO32﹣離子,據此分析選項.


科目:高中化學 來源: 題型:
【題目】煤燃燒排放的煙氣含有SO2和NOx,形成酸雨、污染大氣,采用NaClO2溶液作為吸收劑可同時對煙氣進行脫硫、脫硝,回答下列問題:
(1)在鼓泡反應器中通入含有SO2和NO的煙氣,反應溫度為323 K,NaClO2溶液濃度為 5×103mol·L1。反應一段時間后溶液中離子濃度的分析結果如下表。
離子 | SO42- | SO32- | NO3- | NO2- | Cl- |
c/(mol·L1) | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
①寫出NaClO2溶液脫硝過程中主要反應的離子方程式___________________________________。增加壓強,NO的轉化率______________(填“提高”、“不變”或“降低”)。
②隨著吸收反應的進行,吸收劑溶液的pH逐漸______________ (填“增大”“不變”或“減小”)。
③由實驗結果可知,脫硫反應速率______脫硝反應速率(填“大于”或“小于”)。原因是除了SO2和NO在煙氣中的初始濃度不同,還可能是________________。
(2)在不同溫度下,NaClO2溶液脫硫、脫硝的反應中,SO2和NO的平衡分壓pc如圖所示。由圖分析可知,反應溫度升高,脫硫、脫硝反應的平衡常數均_________(填“增大”、“不變”或“減小”)。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】生物燃料電池是以有機物為燃料,直接或簡介利用酶作為催化劑的一類特殊的燃料電池,其能量轉化效率高,是一種真正意義上的綠色電池.其工作原理如圖所示.下列有關說法正確的是( ) 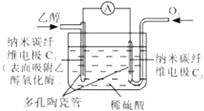
A.O2在C2電極上得電子,被氧化
B.電子由C2極經外電路流向C1極
C.每轉移6mole﹣1 , 理論上生成22.4LCO2
D.C1極的電極反應式為:C2H5OH+3H2O﹣12e﹣1=2CO2+12H+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】兩個化學興趣小組進行了以下探究活動:第一組:為研究鐵質材料與熱濃硫酸的反應.
(1)稱取鐵釘(碳素鋼)12.0g放入30.0mL濃硫酸中,加熱,充分反應后得到溶液X并收集到氣體Y.①甲同學認為X中除Fe3+外還可能含有Fe2+ . 若要確認其中是否含有Fe2+ , 應選擇加入的試劑為(選填序號).
a.KSCN溶液和氯水 b.鐵粉和KSCN溶液 c.濃氨水 d.酸性KMnO4溶液
②乙同學取672mL(標準狀況)氣體Y通入足量溴水中,發生反應:SO2+Br2+2H2O=2HBr+H2SO4然后加入足量BaCl2溶液,經適當操作后得到干燥固體4.66g.據此推知氣體Y中SO2的體積分數為(保留小數點后一位)分析上述實驗中SO2體積分數的結果,丙同學認為氣體Y中還可能含量有H2和CO2氣體.為此設計了下列探究實驗裝置(圖中夾持儀器省略).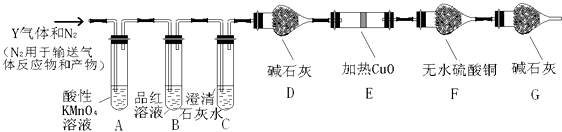
③寫出產生CO2的化學方程式 .
④裝置A中試劑的作用是 , 裝置G中試劑的作用是 .
⑤簡述確認氣體Y中含有CO2的實驗現象 .
⑤如果氣體Y中含有H2 , 預計實驗現象應是 .
(2)第二組:擬用下列裝置定量分析空氣中SO2的含量:  ①KMnO4溶液中導管末端做成球狀多孔結構的作用是
①KMnO4溶液中導管末端做成球狀多孔結構的作用是
②該實驗中已經知道的數據有氣體流速aL/min、酸性KMnO4溶液的體積bL,其濃度為cmol/L.若從氣體通入到紫色恰好褪去,用時5分鐘.則此次取樣處的空氣中二氧化硫含量為g/L.(己知KMnO4被還原的產物通常為Mn2+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有一無色未知溶液中檢驗出有Ba2+、Ag+ , 同時又測得其酸性很強.某學生還要鑒定此溶液中是否大量存在①Cu2+ ②Al3+ ③Cl﹣ ④NO ![]() ⑤NH4+ ⑥CO
⑤NH4+ ⑥CO ![]() ⑦S2﹣ ⑧Mg2+ ⑨Fe3+ , 而事實上有部分離子不用鑒定就能加以否定,你認為不必鑒定的是( )
⑦S2﹣ ⑧Mg2+ ⑨Fe3+ , 而事實上有部分離子不用鑒定就能加以否定,你認為不必鑒定的是( )
A.③⑤⑥⑦⑨
B.①③⑥⑦⑨
C.③④⑦⑧⑨
D.①②③⑤⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】原子序數依次遞增的甲、乙、丙、丁、戊是周期表中前30號元素,其中甲、乙、丙三元素的基態原子2p能級都有單電子,單電子個數分別是2、3、2;丁與戊原子序數相差18,戊元素是周期表中ds區的第一種元素。回答下列問題:
(1)甲能形成多種常見單質,在熔點很高的兩種常見單質中,原子的雜化方式分別為______、__________。
(2)+1價氣態基態陽離子再失去一個電子形成+2價氣態基態陽離子所需要的能量稱為第二電離能I2,依次還有I3、I4、I5…,推測丁元素的電離能突增應出現在第________電離能。
(3)戊的基態原子有________種形狀不同的原子軌道;
(4)甲、乙分別都能與丙形成原子個數比為 1:3的微粒,則該兩種微粒的空間構型分別為:_________________ ;__________________。
(5)丙和丁形成的一種離子化合物的晶胞結構如右圖,該晶體中陽離子的配位數為_________ 。距一個陰離子周圍最近的所有陽離子為頂點構成的幾何體為_______________。已知該晶胞的密度為ρ g/cm3,阿伏加德羅常數為NA,該化合物的相對分子質量為 M,則該晶胞中黑球的半徑r =_____cm。(用含ρ、NA的計算式表示)

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】合成氨技術的創立開辟了人工固氮的重要途徑,其研究自正確的理論指導,合成氨反應N2+3H2![]() 2NH3的平衡常數K值和溫度的關系如下:
2NH3的平衡常數K值和溫度的關系如下:
溫度/℃ | 360 | 440 | 520 |
K值 | 0.036 | 0.010 | 0.0038 |
(1)①由表中數據可知該反應為______反應(填“放熱”或“吸熱”)
②理論上,為了增大平衡時H2的轉化率,可采取的措施是______________(填字母序號)。
a.增大壓強 b.使用合適的催化劑
c.升高溫度 d.及時分離出產物中的NH3
(2)原料氣H2可通過反應CH4(g)+H2O(g) ![]() CO(g)+3H2(g)獲取,已知該反應中,當初始混合氣中的
CO(g)+3H2(g)獲取,已知該反應中,當初始混合氣中的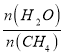 恒定時,溫度、壓強對平衡混合氣中CH4含量的影響如圖所示:
恒定時,溫度、壓強對平衡混合氣中CH4含量的影響如圖所示:

①圖中,兩條曲線表示壓強的關系是p1________p2(填“>”、“=”或“<”)。
②該反應為________反應(填“吸熱”或“放熱”)。
(3)原料氣H2還可通過反應CO(g)+H2O(g) ![]() CO2(g)+H2(g)獲取。T ℃時,向容積固定為2 L的容器中充入1 mol水蒸氣和1 mol CO,反應達平衡后,測得CO2的濃度為0.3 mol·L-1,則平衡時CO的轉化率為________
CO2(g)+H2(g)獲取。T ℃時,向容積固定為2 L的容器中充入1 mol水蒸氣和1 mol CO,反應達平衡后,測得CO2的濃度為0.3 mol·L-1,則平衡時CO的轉化率為________
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com