
【題目】如圖所示,以石墨為電極電解A的水溶液,并做下面一系列實驗.試根據實驗現象完成下列問題(電解質A的水溶液焰色反應呈紫色).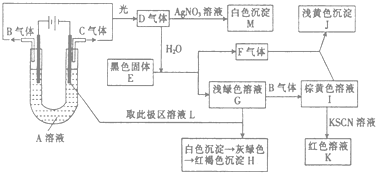
(1)A的化學式為 , E的名稱為 .
(2)I和F反應的離子方程式是 .
(3)若將電解裝置中的陽極換成鐵棒,則在U型管底部可觀察到的現象是 , 陽極的電極反應式為 , 陰極的電極反應式為 , 電解的化學方程式為 .
【答案】
(1)KCl;硫化亞鐵
(2)2Fe3++H2S=2Fe2++S↓+2H+
(3)產生了白色絮狀沉淀;Fe﹣2e﹣═Fe2+;2H++2e﹣═H2↑;Fe+2H2O ![]() Fe(OH)2↓+H2↑
Fe(OH)2↓+H2↑
【解析】解:電解質A的水溶液焰色反應呈淺紫色,由此可知電解質A含有鉀元素;二價鐵離子顯淺綠色,所以G含二價鐵離子,G和L反應生成H,根據實驗現象知,H 是氫氧化鐵,所以溶液L含氫氧根離子,即電解A后,電解液中含有氫氧根離子;C和G反應生成I,I和硫氰化鉀反應生成紅色溶液K,三價鐵離子顯黃色,所以I含三價鐵離子,二價鐵離子和C反應生成三價鐵離子,所以C是氯氣,I是氯化鐵溶液,G是氯化亞鐵溶液,所以A是氯化鉀;電解氯化鉀溶液時,生成物是氯氣、氫氣和氫氧化鉀,所以B是氫氣,L是氫氧化鉀溶液;B和C光照生成D,氫氣和氯氣光照生成氯化氫,所以D是氯化氫;氯化氫溶于水得鹽酸,鹽酸和硝酸銀反應生成白色沉淀氯化銀,所以M是氯化銀;黑色固體E和鹽酸反應生成硫化亞鐵和氣體F,F和氯化鐵反應生成淡黃色沉淀J,淡黃色固體有過氧化鈉、硫、和溴化銀;過氧化鈉在溶液中不存在,所以不是過氧化鈉,氯化鐵和氣體不能生成溴化銀,所以淡黃色沉淀是硫,黑色固體是硫化亞鐵,氣體F是硫化氫氣體.(1)通過以上分析知,A為KCl;E是硫化亞鐵.故答案為:KCl;硫化亞鐵;(2)通過以上分析知,I是氯化鐵溶液,F是硫化氫,氯化鐵有氧化性,硫化氫有還原性,所以氯化鐵和硫化氫能發(fā)生氧化還原反應生成氯化亞鐵和硫單質、鹽酸,離子方程式為:2Fe3++H2S=2Fe2++S↓+2H+ . 故答案為:2Fe3++H2S=2Fe2++S↓+2H+;(3)若將電解裝置中的陽極換成鐵棒,此時陽極是活潑電極,發(fā)生金屬鐵失電子的氧化反應,即Fe﹣2e﹣═Fe2+ , 陰極上是氫離子得電子的還原反應,即2H++2e﹣═H2↑,溶液的堿性增強,會和亞鐵離子結合產生白色沉淀氫氧化亞鐵,則在U型管底部可觀察到產生了白色絮狀沉淀,總反應為:Fe+2H2O ![]() Fe(OH)2↓+H2↑,故答案為:產生了白色絮狀沉淀;Fe﹣2e﹣═Fe2+;2H++2e﹣═H2↑;Fe+2H2O
Fe(OH)2↓+H2↑,故答案為:產生了白色絮狀沉淀;Fe﹣2e﹣═Fe2+;2H++2e﹣═H2↑;Fe+2H2O ![]() Fe(OH)2↓+H2↑. 電解質A的水溶液焰色反應呈淺紫色,由此可知電解質A含有鉀元素;二價鐵離子顯淺綠色,所以G含二價鐵離子,G和L反應生成H,根據實驗現象知,H是氫氧化鐵,所以溶液L含氫氧根離子,即電解A后,電解液中含有氫氧根離子;C和G反應生成I,I和硫氰化鉀反應生成紅色溶液K,三價鐵離子顯黃色,所以I含三價鐵離子,二價鐵離子和C反應生成三價鐵離子,所以C是氯氣,I是氯化鐵溶液,G是氯化亞鐵溶液,所以A是氯化鉀;電解氯化鉀溶液時,生成物是氯氣、氫氣和氫氧化鉀,所以B是氫氣,L是氫氧化鉀溶液;B和C光照生成D,氫氣和氯氣光照生成氯化氫,所以D是氯化氫;氯化氫溶于水得鹽酸,鹽酸和硝酸銀反應生成白色沉淀氯化銀,所以M是氯化銀;黑色固體E和鹽酸反應生成硫化亞鐵和氣體F,F和氯化鐵反應生成淡黃色沉淀J,淡黃色固體有過氧化鈉、硫、和溴化銀;過氧化鈉在溶液中不存在,所以不是過氧化鈉,氯化鐵和氣體不能生成溴化銀,所以淡黃色沉淀是硫,黑色固體是硫化亞鐵,氣體F是硫化氫氣體.(1)根據分析寫出A的化學式和E的名稱;(2)根據硫化氫的還原性和氯化鐵的氧化性分析并寫出離子方程式,注意氣體和單質寫化學式;(3)若將電解裝置中的陽極換成鐵棒,此時陽極是活潑電極,發(fā)生金屬鐵失電子的氧化反應,根據電解池的工作原理來回答.
Fe(OH)2↓+H2↑. 電解質A的水溶液焰色反應呈淺紫色,由此可知電解質A含有鉀元素;二價鐵離子顯淺綠色,所以G含二價鐵離子,G和L反應生成H,根據實驗現象知,H是氫氧化鐵,所以溶液L含氫氧根離子,即電解A后,電解液中含有氫氧根離子;C和G反應生成I,I和硫氰化鉀反應生成紅色溶液K,三價鐵離子顯黃色,所以I含三價鐵離子,二價鐵離子和C反應生成三價鐵離子,所以C是氯氣,I是氯化鐵溶液,G是氯化亞鐵溶液,所以A是氯化鉀;電解氯化鉀溶液時,生成物是氯氣、氫氣和氫氧化鉀,所以B是氫氣,L是氫氧化鉀溶液;B和C光照生成D,氫氣和氯氣光照生成氯化氫,所以D是氯化氫;氯化氫溶于水得鹽酸,鹽酸和硝酸銀反應生成白色沉淀氯化銀,所以M是氯化銀;黑色固體E和鹽酸反應生成硫化亞鐵和氣體F,F和氯化鐵反應生成淡黃色沉淀J,淡黃色固體有過氧化鈉、硫、和溴化銀;過氧化鈉在溶液中不存在,所以不是過氧化鈉,氯化鐵和氣體不能生成溴化銀,所以淡黃色沉淀是硫,黑色固體是硫化亞鐵,氣體F是硫化氫氣體.(1)根據分析寫出A的化學式和E的名稱;(2)根據硫化氫的還原性和氯化鐵的氧化性分析并寫出離子方程式,注意氣體和單質寫化學式;(3)若將電解裝置中的陽極換成鐵棒,此時陽極是活潑電極,發(fā)生金屬鐵失電子的氧化反應,根據電解池的工作原理來回答.


科目:高中化學 來源: 題型:
【題目】油脂是重要的工業(yè)原料.關于“油脂”的敘述錯誤的是
A.不能用植物油萃取溴水中的溴
B.皂化是高分子生成小分子的過程
C.和H2加成后能提高其熔點及穩(wěn)定性
D.水解可得到丙三醇
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A~G是幾種烴的分子球棍模型(如圖) 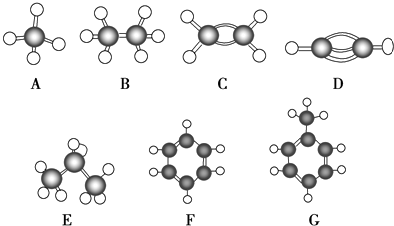
據此回答下列問題:
(1)常溫下含碳量最高的氣態(tài)烴是(填對應字母).
(2)能夠發(fā)生加成反應的烴有(填數字)種.
(3)一鹵代物種類最多的是(填對應字母) .
(4)寫出實驗室制取C的化學方程式 .
(5)寫出F發(fā)生溴代反應的化學方程式 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應中,屬于消去反應的是( )
A.CH2=CH2+HCl ![]() ?CH3CH2Cl
?CH3CH2Cl
B.CH4+Cl2 ![]() CH3Cl+HCl
CH3Cl+HCl
C.nCH2=CH2 ![]()
![]()
D.CH3CH2Br+NaOH ![]() CH2=CH2↑+NaBr+H2O
CH2=CH2↑+NaBr+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溶液中可能含有大量的Mg2+、Al3+、H+、Cl-和少量OH-,向該溶液中逐滴加入0.5 mol·L-1NaOH溶液,生成沉淀的質量和加入NaOH溶液的體積之間的關系如下圖所示,則可判斷原溶液中( )
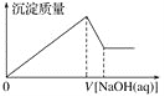
A. 有Mg2+,沒有Al3+
B. 有Al3+,沒有Mg2+
C. 有Mg2+和Al3+
D. 有大量的H+、Mg2+和Al3+
查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com