
【題目】下列物質中,既能跟鹽酸反應,又能跟NaOH溶液反應的是( )
A.NaHCO3
B.Fe2O3
C.Al2O3
D.SiO2
科目:高中化學 來源: 題型:
【題目】在t℃時,AgBr在水中的沉淀溶解平衡曲線如圖所示。又知t℃時AgCl的Ksp=4×10-10,下列說法不正確的是

A. 在t℃時,AgBr的Ksp為4.9×10-13
B. 在AgBr飽和溶液中加入NaBr固體,可使溶液由c點到b點
C. 圖中a點對應的是AgBr的不飽和溶液
D. 在t℃時,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)平衡常數K≈816
AgBr(s)+Cl-(aq)平衡常數K≈816
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某工廠用提取粗鹽后的鹽鹵(主要成分為MgCl2)制備金屬鎂,其工藝流程如下,下列說法中,錯誤的是( )
![]()
A. 操作①發生的反應為非氧化還原反應
B. 若在實驗室進行操作①只需要漏斗和燒杯兩種玻璃儀器
C. 操作②是蒸發濃縮結晶
D. 在整個制備過程中,未發生置換反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】aLCO2氣體通過足量Na2O2后,所得氣體再與bLNO混合時,可得到cL氣體(氣體體積均在相同狀況下測定),下列表達式中,錯誤的是( )
A. 若a則c<![]() (a+b) B. 若a則c>
(a+b) B. 若a則c>![]() (a+b)
(a+b)
C. 若a>b則c=![]() (a+b) D. 若a=b則c=
(a+b) D. 若a=b則c=![]() (a+b)
(a+b)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列分子或離子中中心原子價層電子對幾何構型為四面體且分子或離子空間構型為V形的是( )
A. NH B. PH3 C. OF2 D. H3O+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ、有一瓶澄清的溶液,其中可能含有H+、NH4+、Mg2+、Ba2+、Al3+、I﹣、NO3﹣、CO32﹣、SO42﹣、AlO2﹣,取該溶液進行以下實驗:
(1)取pH試紙檢驗,溶液呈酸性,可以排除______________的存在.
(2)取出部分溶液,加入少量CCl4及數滴新制氯水,經振蕩后CCl4呈紫紅色,可以排除_______存在.
(3)另取出部分溶液逐漸加入NaOH溶液,使溶液從酸性逐漸變為堿性,反應過程中均無沉淀產生,則又可排除____________的存在.
(4)取出部分上述堿性溶液加Na2CO3溶液后,有白色沉淀生成,證明有_______的存在,又可以排除__________的存在.
(5)根據上述實驗事實可以確定,該溶液中肯定存在的離子是____________,還不能確定是否存在的離子是_______________.
Ⅱ、某混合物 A,含有 KAl(SO4)2、Al2O3 和 Fe2O3,在一定條件下可實現下圖所示的物質之間的變化:
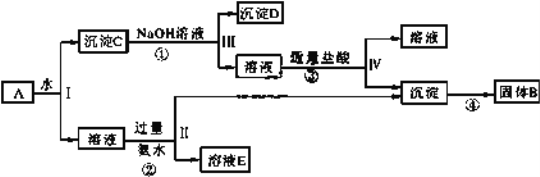
據此回答下列問題:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中對于溶液和沉淀的分離采取的方法是__________。
(2)根據上述框圖反應關系,寫出下列B、C、D 所含物質的化學式(提示:可為混合物)。
固體 B_________;沉淀 C__________;沉淀 D _________;
(3)寫出①、②反應離子方程式。
①___________________________________________;
②___________________________________________;
(4)步驟③較難操作,如何將實驗方案進行改進?________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以反應 5H2C2O4+2MnO4 -+6H+ = 10CO2↑+ 2Mn2+ + 8H2O 為例探究“外界條件對化學反應速率的影響”。實驗時,分別量取 H2C2O4 溶液和酸性 KMnO4溶液,迅速混合并開始計時,通過測定溶液褪色所需時間來判斷反應的快慢。
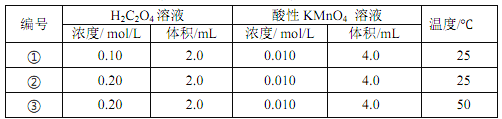
下列說法不正確的是
A. 實驗①、 ②、 ③所加的H2C2O4 溶液均要過量
B. 若實驗①測得 KMnO4溶液的褪色時間為 40 s, 則這段時間內平均反應速率 v(KMnO4)= 2. 5×10-4 mol/L/s
C. 實驗①和實驗②是探究濃度對化學反應速率的影響, 實驗②和③是探究溫度對化學反應速率的影響
D. 實驗①和②起初反應均很慢,過了一會兒速率突然增大,可能是生成的 Mn2+對反應起催化作用
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com