
【題目】X、Y、Z、W、R、Q為前30號元素,且原子序數依次增大。X是所有元素中原子半徑最小的,Y有三個能級,且每個能級上的電子數相等,Z原子單電子數在同周期元素中最多,W與Z同周期,第一電離能比Z的低,R與Y同一主族,Q的最外層只有一個電子,其他電子層電子均處于飽和狀態。請回答下列問題:
(1)Q+核外電子排布式為__________________。
(2)ZX3分子的空間構型為__________________, ZW3-離子的立體構型是__________。
(3)Y、R的最高價氧化物的沸點較高的是_______(填化學式),原因是_____________。
(4)將Q單質的粉末加入到ZX3的濃溶液中,并通入W2,充分反應后溶液呈深藍色,該反應的離子方程式為:______________________________________________。
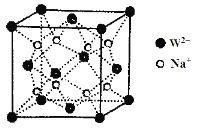
(5)W和Na的一種離子化合物的晶胞結構如圖,該離子化合物為________(填化學式)。Na+的配位數為________,距一個陰離子周圍最近的所有陽離子為頂點構成的幾何體為__________。
【答案】1s22s22p63s23p63d10 三角錐形 平面三角形 SiO2 SiO2為原子晶體,CO2為分子晶體 2Cu + 8NH3 + O2 + 2H2O == 2[Cu(NH3)4]2+ + 4OH Na2O 4 立方體
【解析】
X、Y、Z、W、R、Q為前30號元素,且原子序數依次增大.X是所有元素中原子半徑最小的,則X為H元素;Y有三個能級,且每個能級上的電子數相等,核外電子排布為1s22s22p2,故Y為C元素;R與Y同一主族,結合原子序數可以知道,R為Si元素;W與Z同周期,第一電離能比Z的低,故W為O元素;而Z原子單電子數在同周期元素中最多,則外圍電子排布為ns2np3,原子序數小于O元素,故Z為N元素;Q的最外層只有一個電子,其他電子層電子均處于飽和狀態,不可能為短周期元素,原子序數小于30,故核外電子排布為1s22s22p63s23p63d104s1,則Q為Cu元素.
(1)Cu+核外電子排布式為:1s22s22p63s23p63d10;
(2)ZX3為NH3,空間構型為三角錐形;ZW3-離子為NO3-,NO3-離子中N原子孤電子對數為(5+1-2×3)/2=0,價層電子對數為3+0=3,故其立體構型是平面三角形;
(3)Y、R的最高價氧化物分別為二氧化碳、二氧化硅,二氧化硅為原子晶體,二氧化碳為分子晶體,故沸點較高的是SiO2;
(4)將Cu單質的粉末加入到NH3的濃溶液中,并通入O2,充分反應后溶液呈深藍色,反應生成[Cu(NH3)4]2+,該反應的離子方程式為: 2Cu + 8NH3 + O2 + 2H2O == 2[Cu(NH3)4]2+ + 4OH;
(5)晶胞中Na+離子數目為8,O2-離子數目為8×1/8+6×1/2=4,Na+離子、O2-離子數目之比為2:1,故該晶體化學式為Na2O,由圖可以知道,每個Na+離子周圍有4個O2-離子,Na+離子配位數為4,距一個陰離子周圍最近的所有陽離子有8個,8個鈉離子構成的幾何體為立方體。


科目:高中化學 來源: 題型:
【題目】J、L、M、R、T是原子序數依次增大的短周期主族元素,J、R在周期表中的相對位置如下表。J元素最低負化合價的絕對值與其原子最外層電子數相等;M是地殼中含量最多的金屬元素。
J | ||||
R |
(1)M的離子結構示意圖為__________;元素T在周期表中位于第________族。
(2)J和氫組成的化合物分子有6個原子,其分子式為______________。
(3)M和T形成的化合物在潮濕的空氣中冒白煙,反應的化學方程式為___________。
(4)L的最簡單氣態氫化物甲的水溶液顯堿性。
①在微電子工業中,甲的水溶液可作刻蝕劑H2O2的清除劑,所發生反應的產物不污染環境,其化學方程式為__________________________________________________________。
②L的另一種氫化物乙通常用作火箭的燃料,其組成原子數之比為1∶2,則乙的化學式為_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有關下列四組實驗描述不正確的是
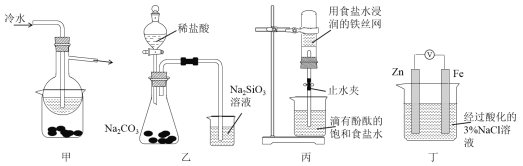
A. 加熱甲裝置中的燒杯可以分離SiO2和NH4Cl
B. 利用裝置乙可證明非金屬性強弱:Cl>C>Si
C. 打開丙中的止水夾,一段時間后,可觀察到燒杯內溶液上升到試管中
D. 向丁中鐵電極區滴入2滴鐵氰化鉀溶液,一段時間后,燒杯中不會有藍色沉淀生成
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙醛酸(HOOC-CHO)是有機合成的重要中間體。工業上用“雙極室成對電解法”生產乙醛酸,原理如圖所示,該裝置中陰、陽兩極為惰性電極,兩極室均可產生乙醛酸,其中乙二醛與M電極的產物反應生成乙醛酸。下列說法正確的是
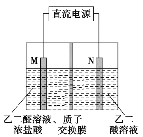
A. M極與直流電源的負極相連
B. 每得到lmol乙醛酸將有2molH+從右室遷移到左室
C. N電極上的電極反應式:HOOC-COOH-2eˉ+2H+ = HOOC-CHO+H2O
D. 每消耗0.1mol乙二醛在M電極放出2.24L氣體(標準狀況)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】疊氮化鈉(NaN3)是一種應用廣泛的化工產品,可用于合成抗生素頭孢菌素藥物的中間體,汽車安全氣囊等。
Ⅰ.實驗室制備NaN3
(1)實驗原理:
①把氨氣通入熔融金屬鈉反應制得氨基鈉(NaNH2),該反應的化學方程式為____________。
②將生成的NaNH2與N2O在210℃-220℃下反應可生成NaN3、NaOH和氣體X,該反應的化學方程式為2NaNH2+N2O═NaN3+NaOH+X,實驗室檢驗X氣體使用的試紙是濕潤的______。
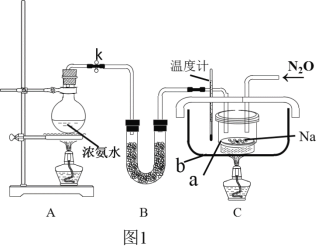
(2)實驗裝置(圖1)、步驟如下,回答下列問題:
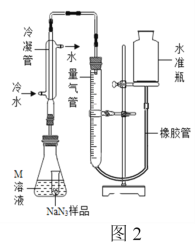
已知:i)NaN3是一種易溶于水的白色晶體,微溶于乙醇,不溶于乙醚;
ii)NaNH2的熔點為210℃,沸點為400℃,在水溶液中易水解。
①組裝儀器檢查裝置氣密性后,裝入藥品。裝置B中盛放的藥品是_______________。
②實驗過程應先點燃___(填“A”或“C”)處的酒精燈,理由是_______________________。
③讓氨氣和熔化的鈉充分反應后,停止加熱A并關閉止水夾k。向裝置C中b容器內充入加熱介質植物油并加熱到210℃-220℃,然后按圖通入N2O;
④裝置C反應完全結束后,冷卻,取出a中的混合物進行以下操作,得到NaN3固體:

操作II的目的是____________;
操作IV中選用的洗滌試劑最好的是_____。
A.水 B.乙醇 C.乙醇水溶液 D.乙醚
(3)圖中儀器a用不銹鋼材質的而不用玻璃的,其主要原因是____________________。
II.產品NaN3純度測定
精確稱量0.150 g NaN3樣品,設計如圖2所示裝置,連接好裝置后使錐形瓶傾斜,使小試管中的NaN3樣品與M溶液接觸,測量產生的氣體體積從而測定其純度。
已知2 NaN3→ 3N2(NaN3中的N全部轉化為N2,其他產物略),反應中放出大量的熱。
(4)使用冷水冷凝的目的是______。對量氣管讀數時,反應前后都需要進行的操作是______。
(5)常溫下測得量氣管讀數為60.0 mL(N2的密度為1.40 g/L)計算NaN3樣品的純度為______。(保留三位有效數字)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】許多元素及它們的化合物在科學研究和工業生產中具有許多用途。請回答下列有關問題:
(1)現代化學中,常利用_________上的特征譜線來鑒定元素。
(2)某同學畫出基態碳原子的核外電子排布圖:![]() ,該電子排布圖違背了__;CH3+、—CH3、CH3—都是重要的有機反應中間體。CH3+、CH3—的空間構型分別為___、____。
,該電子排布圖違背了__;CH3+、—CH3、CH3—都是重要的有機反應中間體。CH3+、CH3—的空間構型分別為___、____。
(3)基態溴原子的價層電子軌道排布圖為_______,第四周期中,與溴原子未成對電子數相同的金屬元素有_______種。
(4)磷化硼是一種耐磨涂料,它可用作金屬的表面保護層。
① 磷化硼晶體晶胞如圖甲所示:其中實心球為磷原子,在一個晶胞中磷原子空間堆積方式為_____,已知晶胞邊長apm,阿伏加德羅常數為NA。則磷化硼晶體的密度為___________g/cm3。
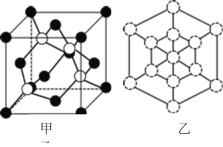
② 磷化硼晶胞沿著體對角線方向的投影(圖乙中![]() 表示P原子的投影),用
表示P原子的投影),用![]() 畫出B原子的投影位置_____。
畫出B原子的投影位置_____。
(5)Fe3O4晶體中,O2-圍成正四面體空隙(1、3、6、7號氧圍成)和正八面體空隙(3、6、7、8、9、12號氧圍成),Fe3O4中有一半的Fe3+填充在正四面體空隙中,Fe2+和另一半Fe3+填充在正八面體空隙中,晶體中正四面體空隙數與正八面休空隙數之比為__________,有__________%的正八面體空隙沒有填充陽離子。
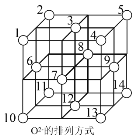
(6)一定溫度下,NiO晶體可以自發地分散并形成“單分子層”,可以認為O2-作密置單層排列,Ni2+填充其中(如圖),己知O2-的半徑為a pm,每平方米面積上分散的該晶體的質量為_____g(用a、NA表示)

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某電池總反應為Fe+2Fe3+=3Fe2+,下列與此電,池總反應不符的原電池是( )
A.銅片、鐵片、FeCl3溶液組成的原電池
B.石墨、鐵片、Fe(NO3)3溶液組成的原電池
C.鐵片鋅片、Fe2(SO4)3溶液組成的原電池
D.銀片、鐵片、Fe(NO3)3溶液組成的原電池
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現代社會環境變化快、生活節奏快,很多人心理壓力過大,緊張焦慮,導致抑郁患者量增加。某研究小組按下列路線合成抗抑郁藥物嗎氯貝胺:
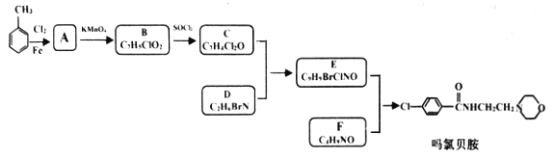
已知: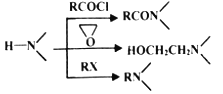
請回答:
(1)下列說法正確的是___________。
A.化合物A分子中有兩種氫原子 B.合成路線所涉反應均為取代反應
C.化合物D具有堿性 D.嗎氯貝胺能發生水解反應
(2)化合物F的結構簡式是______________________。
(3)寫出C+D→E的化學方程式____________________________________________。
(4)為探索新的合成路線,發現用化合物C與X(C6H14N2O)一步反應即可合成嗎氯貝胺。請設計以環氧乙烷(![]() )為原料合成X的合成路線_________________________________(用流程圖表示,無機試劑任選)。
)為原料合成X的合成路線_________________________________(用流程圖表示,無機試劑任選)。
(5)符合以下條件的化合物X(C6H14N2O)可能的同分異構體有___________種。其中只有一條側鏈的同分異構體的結構簡式為______________________(任寫一種)。
①分子中有一個六元環,且成環原子中最多含一個非碳原子。
②1H-NMR譜顯示分子中有5種氫原子;IR譜表明分子中有N-N鍵,無O-H鍵。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com