
 CO(g)+ H2(g)在一容積可變的密閉容器中進行。下列條件的改變對其反應速率幾乎無影響的是
CO(g)+ H2(g)在一容積可變的密閉容器中進行。下列條件的改變對其反應速率幾乎無影響的是| A.壓縮容器體積,增大體系壓強 |
| B.加入適當的催化劑 |
| C.保持壓強不變,充入惰性氣體使容器容積增大 |
| D.保持容器容積不變,充入惰性氣體使體系壓強增大 |
 直通貴州名校周測月考直通名校系列答案
直通貴州名校周測月考直通名校系列答案科目:高中化學 來源:不詳 題型:單選題
| A.滴加NaCl溶液 | B.加熱 |
| C.換用4mol/L硫酸 | D.換用鐵粉 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.常溫下“納米銅”比銅片的還原性強,反應時反應速率快 |
| B.“納米銅”顆粒更細小,化學反應時接觸面大,所以反應速率快 |
| C.“納米銅”與銅是同素異形體 |
| D.常溫下“納米銅”比銅片更易得電子,反應時反應速率快 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 CO(g)+H2(g)。該反應在一容積可變的密閉容器中進行時,改變下列條件會對反應速率產生影響的是
CO(g)+H2(g)。該反應在一容積可變的密閉容器中進行時,改變下列條件會對反應速率產生影響的是| A.①② | B.②③ | C.②④ | D.①④ |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.①③④ | B.①②④ | C.①②③④ | D.①②③⑤ |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 2SO3(g)ΔH<0,某研究小組研究了其他條件不變時,改變某一條件對上述反應的影響,下列分析正確的是
2SO3(g)ΔH<0,某研究小組研究了其他條件不變時,改變某一條件對上述反應的影響,下列分析正確的是
| A.圖Ⅰ研究的是t0時刻增大O2的物質的量濃度對反應速率的影響 |
| B.圖Ⅱ研究的是t0時刻通入氦氣增大體系壓強對反應速率的影響 |
| C.圖Ⅲ研究的是催化劑對化學平衡的影響,且甲的催化效率比乙高 |
| D.圖Ⅲ研究的是溫度對化學平衡的影響,且乙的溫度較高 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
| 實驗編號 | 實驗目的 | T/K | pH | c/10-3 mol·L-1 | |
| H2O2 | Fe2+ | ||||
| ① | 為以下實驗作參照 | 298 | 3 | 6.0 | 0.30 |
| ② | 探究溫度對降解反應速率的影響 | | | | |
| ③ | | 298 | 10 | 6.0 | 0.30 |
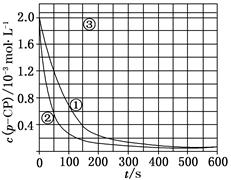
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 Na2S(s)+4H2O(g) ΔH=-225 kJ·mol-1,該反應的正反應速率隨時間的變化情況如圖所示,在t1時改變了某種條件,反應在t2時達平衡,改變的條件可能是( )
Na2S(s)+4H2O(g) ΔH=-225 kJ·mol-1,該反應的正反應速率隨時間的變化情況如圖所示,在t1時改變了某種條件,反應在t2時達平衡,改變的條件可能是( )
| A.升高溫度 | B.增大H2的濃度 |
| C.使用催化劑 | D.增大壓強 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
| 反應進程 (分鐘) | 1 | 2 | 5 | 15 | 20 |
| 4.0 mol/L 鹽酸 | 少量氣泡 | 較多氣泡 | 大量氣泡 | 反應劇烈 | 鋁片耗盡 |
| 2.0 mol/L 硫酸 | 無明顯現象 | 極少量 氣泡 | 少量氣泡 | ||
| 4.0 mol/L 硫酸 | 無明顯現象 | 少量氣泡 | 有比較連續的氣泡 | ||
| 實驗目的 | 實驗 編號 | 溫度 /℃ | 金屬鋁的 形態 | 鹽酸濃度 /mol·L-1 |
| 1.實驗①和②探究鹽酸濃度對該反應速率的影響; 2.實驗①和③探究溫度對該反應速率的影響; 3.實驗①和④探究金屬規格(鋁片、 鋁粉)對該反應速率的影響 | ① | 25 | 鋁片 | 4.0 |
| ② | | | | |
| ③ | | | | |
| ④ | | | |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com