
| A. | 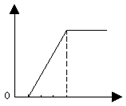 | B. | 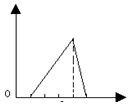 | C. | 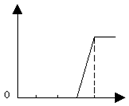 | D. | 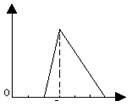 |
分析 含少量HCl的氯化鋁溶液,加入氫氧化鈉,先是和鹽酸之間發生中和反應生成氯化鈉和水,沒有沉淀,HCl+NaOH=NaCl+H2O,然后氫氧化鈉和氯化鋁之間反應逐漸產生沉淀直到沉淀量最大,AlCl3+3NaOH═Al(OH)3↓+3NaCl,后是氫氧化鋁溶解,Al(OH)3 +NaOH═NaAlO2+2H2O,由此分析解答.
解答 解:含少量HCl的氯化鋁溶液,加入氫氧化鈉,先是和鹽酸之間發生中和反應生成氯化鈉和水,沒有沉淀,HCl+NaOH=NaCl+H2O,然后氫氧化鈉和氯化鋁之間反應逐漸產生沉淀直到沉淀量最大,AlCl3+3NaOH═Al(OH)3↓+3NaCl,后是氫氧化鋁溶解,Al(OH)3 +NaOH═NaAlO2+2H2O,圖象為: ,故選B.
,故選B.
點評 本題以圖象顯示考查化學反應,難度中等,明確發生的化學反應是解答的關鍵,注意圖象前后兩部分的比例關系.


 計算高手系列答案
計算高手系列答案科目:高中化學 來源: 題型:選擇題
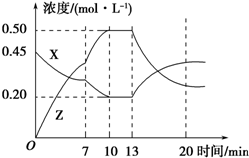
| A. | 用X表示0~10 min內該反應的平均速率為v(X)=0.045 mol•L-1•min-1 | |
| B. | 根據上圖可求得化學方程式中a:b=1:3 | |
| C. | 推測在第7 min時曲線變化的原因可能是升溫 | |
| D. | 推測在第13 min時曲線變化的原因可能是降溫 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用CH3COOH 溶液做導電性實驗,燈泡很暗,能證明 CH3COOH 是弱電解質 | |
| B. | 將Ca(OH)2的飽和溶液加熱,pH 和 Kw均增大 | |
| C. | 25℃時,1.0×10-3mol•L-1鹽酸的pH=3.0,1.0×10-8 mol•L-1鹽酸的pH=8.0 | |
| D. | 向pH相同的氨水和氫氧化鈉溶液中分別加入適量NH4Cl(s)后,兩溶液的pH均減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下分別測等體積、等濃度的醋酸和氨水pH,發現二者的pH 之和為14,說明常溫下醋酸和氨水的電離平衡常數相等 | |
| B. | 將CH3COONa溶液從25℃升溫至 40℃,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$增大 | |
| C. | 向硝酸中加入氨水至中性,溶液中$\frac{{c(N{H_4}^+)}}{{c(N{O_3}^-)}}$<1 | |
| D. | 向AgCl、AgBr 的飽和溶液中加入少量 AgNO3,溶液中$\frac{c(C{l}^{-})}{c(B{r}^{-})}$增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯化鉀溶液在電流作用下電離成K+和Cl- | |
| B. | 摩爾是表示物質所含微粒集體是多少的物理量 | |
| C. | 依據丁達爾效應可將分散系分為溶液、膠體與濁液 | |
| D. | 氧化還原反應的本質是有電子的轉移 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 目的 | 實驗 | 現象 |
| A | 檢驗CO2氣體中混有SO2 | 將氣體通入盛有足量的澄清石灰水中的洗氣瓶中 | 石灰水變渾濁 |
| B | 檢驗黑色固體Fe3O4中含有+3價鐵元素 | 將少量黑色固體加入盛有KSCN溶液的燒杯中 | 固體溶解,溶液呈血紅色 |
| C | 比較氯和碳的非金屬性強弱 | 將碳酸鈉溶液中滴入稀鹽酸 | 有氣泡產生 |
| D | 驗證氧化性:Fe3+>Cu2+ | 將一定量銅粉加到盛有一定體積的1.0mol•L-1Fe2(SO4)3溶液的試管中 | 銅粉溶解,溶液變藍色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com