
(10分)工業制硫酸生產流程如下圖:

(1)在氣體進入催化反應室前,需凈化的原因是:________________________________。
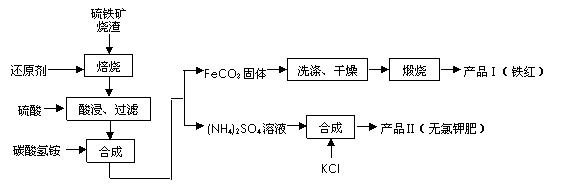
(2)在制氣過程中,我國往往以黃鐵礦為原料制SO2 ,其鐵礦燒渣(主要成分為Fe2O3、Fe3O4、FeO、SiO2等)是生產硫酸的工業廢渣,綜合利用對環境保護具有現實意義。利用硫鐵礦燒渣制備鐵紅等產品的實驗流程如下:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
已知幾種鹽的溶解度隨溫度變化的曲線如下圖所示:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
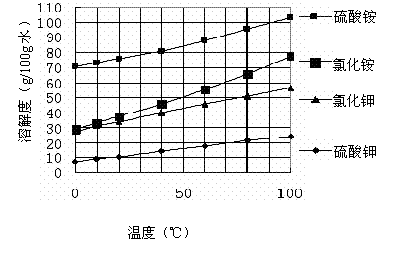
則:
①酸浸、過濾后濾液中的金屬陽離子是________________。
②煅燒FeCO3生成產品Ⅰ的化學反應方程式為_______________________________ _。
③產品Ⅱ的化學式為_______________
④檢驗產品II中是否含有氯化物雜質的實驗操作是:取少量產品Ⅱ于試管中配成溶液,
科目:高中化學 來源: 題型:
(10分) 硫酸的消費量是衡量一個國家化工生產水平的重要標志。
(1)V2O5是SO2與O2反應的催化劑,請寫出該反應的方程式:
_____________________________________________________________________。
(2)一定條件下,SO2與空氣反應10 min后,SO2和SO3物質的量濃度分別為1.2 mol/L和2.0 mol/L,則SO2起始物質的量濃度為_____________;生成SO3的化學反應速率為_________________。
(3)若改變外界條件,發生SO2與空氣反應生成SO3,使10 min內的用O2表示的反應速率為0.15mol/(L·min),則改變的條件可能是_______________。
A.壓縮體積,增大壓強 B.降低溫度
C.充入大量的氮氣 D.僅增加SO2的濃度
(4)工業制硫酸,用過量的氨水對SO2尾氣處理,請寫出相關的離子方程式
______________________________________________________。
查看答案和解析>>
科目:高中化學 來源:09~10年西南師大附中高一下期期末考試化學卷 題型:填空題
(10分) 硫酸的消費量是衡量一個國家化工生產水平的重要標志。
(1)V2O5是SO2與O2反應的催化劑,請寫出該反應的方程式:
_____________________________________________________________________。
(2)一定條件下,SO2與空氣反應10 min后,SO2和SO3物質的量濃度分別為1.2 mol/L和2.0 mol/L,則SO2起始物質的量濃度為_____________;生成SO3的化學反應速率為_________________。
(3)若改變外界條件,發生SO2與空氣反應生成SO3,使10 min內的用O2表示的反應速率為0.15mol/(L·min),則改變的條件可能是_______________。
| A.壓縮體積,增大壓強 | B.降低溫度 |
| C.充入大量的氮氣 | D.僅增加SO2的濃度 |
查看答案和解析>>
科目:高中化學 來源:2012-2013學年四川省宜賓市高三第一次診斷性測試化學試卷(解析版) 題型:填空題
(12分)工業制硫酸時,利用接觸氧化反應將SO2轉化為SO3是一個關鍵的步驟。
(1)在接觸室中2SO2(g)+O2(g)
 2SO3(g)達到平衡狀態的標志是______。
2SO3(g)達到平衡狀態的標志是______。
A.υ(O2)正=2υ(SO2)逆
B.容器中氣體的總質量不隨時間而變化
C.容器中氣體的顏色不隨時間而變化
D.容器中氣體的壓強不隨時間而變化
(2)下列關于反應2SO2(g)+O2(g)
 2SO3(g)
ΔH<0。下列圖像中不正確的是______ (填字母序號)。
2SO3(g)
ΔH<0。下列圖像中不正確的是______ (填字母序號)。

(3)某溫度下SO2(g)+ 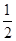 O2(g)
O2(g)
 SO3(g)
ΔH=-98KJ/mol
SO3(g)
ΔH=-98KJ/mol
①開始時在體積固定的密閉容器中加入4mol SO2 (g)和1mol O2 (g),達到平衡時 共放出196 KJ的熱量,該溫度下SO2的平衡轉化率為______
②已知固態單質硫的燃燒熱為296KJ/mol,則由S(s)生成2 molSO3(g)的ΔH為____________
(4)檢驗SO42-常用BaCl2溶液。常溫時,BaSO4的Ksp=1.08×10-10,現將等體積的 BaCl2溶液與2.0×10-3mol/L的H2SO4溶液混合。若要生成BaSO4沉淀,原BaCl2溶液的最小濃度為____________
查看答案和解析>>
科目:高中化學 來源:09-10年西南師大附中高一下期期末考試化學卷 題型:填空題
(10分) 硫酸的消費量是衡量一個國家化工生產水平的重要標志。
(1)V2O5是SO2與O2反應的催化劑,請寫出該反應的方程式:
_____________________________________________________________________。
(2)一定條件下,SO2與空氣反應10 min后,SO2和SO3物質的量濃度分別為1.2 mol/L和2.0 mol/L,則SO2起始物質的量濃度為_____________;生成SO3的化學反應速率為_________________。
(3)若改變外界條件,發生SO2與空氣反應生成SO3,使10 min內的用O2表示的反應速率為0.15mol/(L·min),則改變的條件可能是_______________。
A.壓縮體積,增大壓強 B.降低溫度
C.充入大量的氮氣 D.僅增加SO2的濃度
(4)工業制硫酸,用過量的氨水對SO2尾氣處理,請寫出相關的離子方程式
______________________________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com