
| A. | v(A)=0.5 mol/(L•s) | B. | v(B)=0.3 mol/(L•s) | C. | v(C)=0.8 mol/(L•s) | D. | v(D)=1.0 mol/(L•s) |
分析 不同物質表示的速率之比等于其化學計量數之比,故不同物質表示的速率與其化學計量數的比值越大,表示的速率越快,注意保持單位一致.
解答 解:不同物質表示的速率之比等于其化學計量數之比,故不同物質表示的速率與其化學計量數的比值越大,表示的速率越快,對應反應:2A+B?3C+4D,
A.$\frac{v(A)}{1}$=0.5 mol/(L•s);
B.$\frac{v(B)}{1}$=0.3 mol/(L•s);
C.$\frac{v(C)}{1}$=0.8mol/(L.s),
D.$\frac{v(D)}{1}$=1.0 mol/(L•s),
故D表示的反應速率最快,
故選D.
點評 本題考查化學反應速率快慢比較,難度不大,利用比值法可以迅速判斷,也可以轉化為同一物質表示的速率進行比較,注意單位保持一致.


 陽光課堂課時優化作業系列答案
陽光課堂課時優化作業系列答案科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 濃H2SO4的吸水性和酸性 | |
| B. | 濃H2SO4的脫水性和吸水性 | |
| C. | 濃H2SO4的強氧化性和吸水性 | |
| D. | 濃H2SO4的吸水性和稀H2SO4的通性(酸性) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在船舶的外殼裝上銅塊可防止其發生電化學腐蝕 | |
| B. | FeCl3溶液和Fe2(SO4)3溶液加熱蒸干、灼燒都得到Fe2O3 | |
| C. | MnO2、FeCl3和CuSO4都可加快H2O2的分解速率 | |
| D. | 用惰性電極分別電解CuCl2溶液和MgCl2溶液分別得到單質Cu和Mg |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 步驟 | 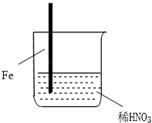 | 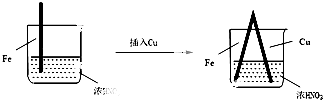 | |
| 現象 | Fe表面產生大量無色氣泡,液面上方變為紅棕色 | Fe表面產生少量紅棕色氣泡后,迅速停止 | Fe、Cu接觸后,其表面均產生紅棕色氣泡 |
| A. | Ⅰ中氣體由無色變紅棕色的化學方程式為:2NO+O2═2NO2 | |
| B. | Ⅱ中的現象說明Fe表面形成致密的氧化層,阻止Fe進一步反應 | |
| C. | 對比Ⅰ、Ⅱ中現象,說明稀HNO3的氧化性強于濃HNO3 | |
| D. | 針對Ⅲ中現象,在Fe、Cu之間連接電流計,可判斷Fe是否被氧化 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | … |
| … | C2H6 | C5H12 | C8H18 | … | … | … | … |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH4+、Ba2+、Cl-、NO3- | B. | K+、AlO2-、Cl-、SO42- | ||
| C. | Ca2+、Mg2+、NO3-、HCO3- | D. | Na+、Cl-、CO32-、S2- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 等體積硫酸鐵、硫酸銅、硫酸鉀溶液分別與足量的氯化鋇溶液反應,若生成的硫酸鋇沉淀的質量比為1:2:3,則三種硫酸鹽溶液的物質的量濃度比為1:2:3 | |
| B. | 150 mL 1 mol•L-1的氯化鉀溶液中的c(Cl-)與50 mL 1 mol•L-1的氯化鋁溶液中的c(Cl-)相等 | |
| C. | 20℃時,飽和KCl溶液的密度為1.174 g•cm-3,物質的量濃度為4.0 mol•L-1,則此溶液中KCl的質量分數為$\frac{4.0×74.5}{1.174×1000}$×100% | |
| D. | 20℃時,100 g水可溶解34.2 g KCl,此時KCl飽和溶液的質量分數為34.2% |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com