
某有機化合物D,其相對分子質量為166,取8.3g該物質完全燃燒得到CO2與H2O的物質的量之比是9:5。回答下列問題:
(1)D的分子式為: ;
(2)已知其分子結構中含有一個苯環,苯環的兩個鄰位有取代基。進一步實驗可知:
①D能與碳酸氫鈉溶液反應生成無色無味氣體。②8.3gD物質與足量金屬鈉反應可生成氫氣1.12L(標準狀況)。③D不能與FeCl3溶液發生顯色反應。④D不能發生消去反應。請寫出符合上述條件的D的所有同分異構體的結構簡式:
(3)已知D的一種同分異構體有以下轉化關系。取C在NaOH水溶液中反應后的混合液,加入足量硝酸酸化后,再加入硝酸銀溶液,出現白色沉淀。E分子中有兩個六元環結構。
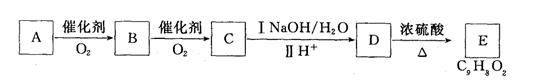
①A的結構簡式為 ;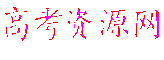
②上述轉化過程中涉及到的反應類型有(填選項) ;
A.氧化反應 B.加成反應 C.取代反應 D.聚合反應
③寫出由A→B的化學方程式: ;
寫出由D→E的化學方程式: 。
 教材全解字詞句篇系列答案
教材全解字詞句篇系列答案科目:高中化學 來源: 題型:閱讀理解
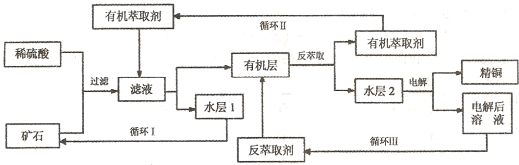
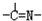 三種基團,無環狀結構,三種基團的數目關系為n3=
三種基團,無環狀結構,三種基團的數目關系為n3=

查看答案和解析>>
科目:高中化學 來源:山東省聊城市“四縣六校”2012-2013學年高一下學期期末聯考化學試題 題型:058
乙烯是來自石油的重要有機化工原料,其產量通常用來衡量一個國家的石油化工發展水平.結合以下路線回答:

已知:2CH3CHO+O2![]() 2CH3COOH
2CH3COOH
(1)反應Ⅱ的化學方程式是________.
(2)D為高分子化合物,可以用來制造多種包裝材料,其結構簡式是________.
(3)E是有香味的物質,在實驗室用下圖裝置制取.

①反應IV的化學方程式是________,該反應類型為________.
②該裝置圖中有一個明顯的錯誤是________.
(4)為了證明濃硫酸在反應IV中起到了催化劑和吸水劑的作用,某同學利用上圖改進后裝置進行了以下4個實驗.實驗開始先用酒精燈微熱3 min,再加熱使之微微沸騰3 min.實驗結束后充分振蕩小試管乙再測有機層的厚度,實驗記錄如下:

①實驗D的目的是與實驗C相對照,證明H+對酯化反應具有催化作用.實驗D中應加入鹽酸的體積和濃度分別是3 mL和________ mol·L-1 .
②分析實驗________(填實驗編號)的數據,可以推測出濃H2SO4的吸水性提高了乙酸乙酯的產率.
查看答案和解析>>
科目:高中化學 來源: 題型:
乙烯是來自石油的重要有機化工原料,其產量通常用來衡量一個國家的石油化工發展水平。結合以下路線回答:
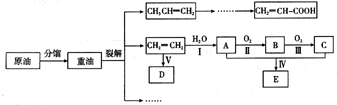
已知:![]()
(1)反應II的化學方程式是 。
(2)D為高分子化合物,可以用來制造多種包裝材料,其結構簡式是 。
(3)E是有香味的物質,在實驗室用下圖裝置制取。

①反應IV的化學方程式是 ,該反應類型為 。
②該裝置圖中有一個明顯的錯誤是 。
(4)為了證明濃硫酸在反應IV中起到了催化劑和吸水劑的作用,某同學利用上圖改進后裝置進行了以下4個實驗。實驗開始先用酒精燈微熱3min,再加熱使之微微沸騰3min。實驗結束后充分振蕩小試管乙再測有機層的厚度,實驗記錄如下:
| 實驗編號 | 試管甲中試劑 | 試管乙中試劑 | 有機層的厚度/cm |
| A | 2 mL乙醇、1 mL乙酸、 1mL18mol·L-1 濃硫酸 | 飽和Na2CO3溶液 | 3.0 |
| B | 2 mL乙醇、1 mL乙酸 | 0.1 | |
| C | 2 mL乙醇、1 mL乙酸、 3 mL 2mol·L-1 H2SO4 | 0.6 | |
| D | 2 mL乙醇、1 mL乙酸、鹽酸 | 0.6 |
①實驗D的目的是與實驗C相對照,證明H+對酯化反應具有催化作用。實驗D中應加入鹽酸的體積和濃度分別是3mL和 mol·L-1 。
②分析實驗 (填實驗編號)的數據,可以推測出濃H2SO4的吸水性提高了乙酸乙酯的產率。
查看答案和解析>>
科目:高中化學 來源:2015屆山東省聊城市四縣六校高一下學期期末聯考化學試卷(解析版) 題型:實驗題
乙烯是來自石油的重要有機化工原料,其產量通常用來衡量一個國家的石油化工發展水平。結合以下路線回答:

已知: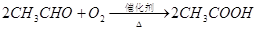
(1)反應II的化學方程式是 。
(2)D為高分子化合物,可以用來制造多種包裝材料,其結構簡式是 。
(3)E是有香味的物質,在實驗室用下圖裝置制取。
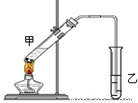
①反應IV的化學方程式是 ,該反應類型為 。
②該裝置圖中有一個明顯的錯誤是 。
(4)為了證明濃硫酸在反應IV中起到了催化劑和吸水劑的作用,某同學利用上圖改進后裝置進行了以下4個實驗。實驗開始先用酒精燈微熱3min,再加熱使之微微沸騰3min。實驗結束后充分振蕩小試管乙再測有機層的厚度,實驗記錄如下:
實驗編號 試管甲中試劑 試管乙中試劑 有機層的厚度/cm
A 2 mL乙醇、1 mL乙酸、
1mL18mol·L-1 濃硫酸 飽和Na2CO3溶液 3.0
B 2 mL乙醇、1 mL乙酸 0.1
C 2 mL乙醇、1 mL乙酸、
3 mL 2mol·L-1 H2SO4 0.6
D 2 mL乙醇、1 mL乙酸、鹽酸 0.6
①實驗D的目的是與實驗C相對照,證明H+對酯化反應具有催化作用。實驗D中應加入鹽酸的體積和濃度分別是3mL和 mol·L-1 。
②分析實驗 (填實驗編號)的數據,可以推測出濃H2SO4的吸水性提高了乙酸乙酯的產率。
查看答案和解析>>
科目:高中化學 來源:2015屆江西省撫州市高一下學期期末考試化學試卷(解析版) 題型:實驗題
乙烯是來自石油的重要有機化工原料,其產量通常用來衡量一個國家的石油化工發展水平。結合以下路線回答:

已知:
(1)反應II的化學方程式是 。
(2)D為高分子化合物,可以用來制造多種包裝材料,其結構簡式是 。
(3)E是有香味的物質,在實驗室用下圖裝置制取。

①反應IV的化學方程式是 ,該反應類型為 。
②該裝置圖中有一個明顯的錯誤是 。
(4)為了證明濃硫酸在反應IV中起到了催化劑和吸水劑的作用,某同學利用上圖改進后裝置進行了以下4個實驗。實驗開始先用酒精燈微熱3min,再加熱使之微微沸騰3min。實驗結束后充分振蕩小試管乙再測有機層的厚度,實驗記錄如下:
實驗編號 試管甲中試劑 試管乙中試劑 有機層的厚度/cm
A 2 mL乙醇、1 mL乙酸、
1mL18mol·L-1 濃硫酸 飽和Na2CO3溶液 3.0
B 2 mL乙醇、1 mL乙酸 0.1
C 2 mL乙醇、1 mL乙酸、
3 mL 2mol·L-1 H2SO4 0.6
D 2 mL乙醇、1 mL乙酸、鹽酸 0.6
①實驗D的目的是與實驗C相對照,證明H+對酯化反應具有催化作用。實驗D中應加入鹽酸的體積和濃度分別是3mL和 mol·L-1 。
②分析實驗 (填實驗編號)的數據,可以推測出濃H2SO4的吸水性提高了乙酸乙酯的產率。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com