
氧化鋁中含少量氧化鐵和二氧化硅雜質,試寫出除雜過程和有關的化學方程式。
(1)將樣品加稍過量的鹽酸中充分反應,過濾除去SiO2:Al2O3+6HCl=2AlCl3+3H2O;Fe2O3+6HCl=2FeCl3+3H2O。
(2)向濾液中加稍過量的氫氧化鈉溶液,充分反應后過濾,除去Fe(OH)3。
NaOH+HCl=NaCl+H2O;3NaOH+FeCl3=Fe(OH)3↓+3NaCl;4NaOH+AlCl3=Na[Al(OH)4]+3NaCl
(3)向上述濾液中通入過量二氧化碳,過濾,得Al(OH)3
CO2+NaOH=NaHCO3;Na[Al(OH)4]+CO2=Al(OH)3↓+NaHCO3。
(4)將所得Al(OH)3加熱得Al2O3。2 Al(OH)3![]() Al2O3+3H2O
Al2O3+3H2O
本題的特點是:兩性氧化物中含有堿性氧化物和酸性氧化物的雜質。應根據三類不同氧化物與酸、堿反應的情況加以分析。氧化鋁與強酸、強堿都反應,除雜時必然轉化為其它物質。應選擇適當的酸、堿將雜質一一除去,并使氧化鋁復生。


 各地期末復習特訓卷系列答案
各地期末復習特訓卷系列答案 小博士期末闖關100分系列答案
小博士期末闖關100分系列答案科目:高中化學 來源: 題型:閱讀理解

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 開始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
 [Fe2(OH)4]2++2H+
[Fe2(OH)4]2++2H+ [Fe2(OH)4]2++2H+
[Fe2(OH)4]2++2H+
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
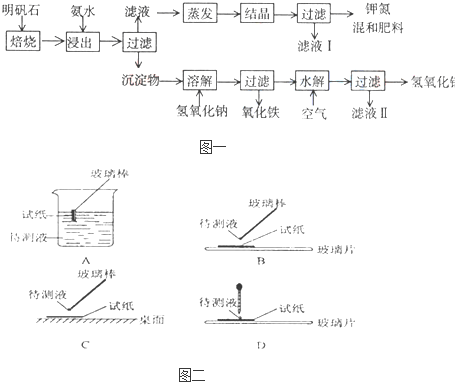
| (m-132n) |
| 42 |
| (m-132n) |
| 42 |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
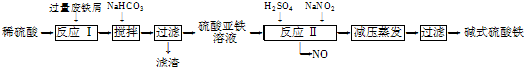
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 開始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
2+ 4 |
- 3 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com