
【題目】基于CaSO4為載氧體的天然氣燃燒是一種新型綠色的燃燒方式,CaSO4作為氧和熱量的有效載體,能夠髙效低能耗地實現CO2的分離和捕獲其原理如下圖所示:
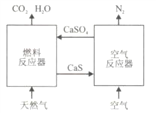
(1)已知在燃料反應器中發生如下反應:
i.CaSO4(g)+CH4(g)=4CaO(s)+CO2(g)+4SO2(g)+2H2O(g) ΔH1=akJ/mol
ii.CaSO4(s)+CH4(g)=CaS(s)+CO2(g)+2H2O(g) ΔH2=bkJ/mol
ⅲ. CaS(s)+3CaSO4(s)= 4CaO(s)+4SO2(g) ΔH3=ckJ/mol
①燃料反應器中主反應為_____________(填“i”“ ii”或“ⅲ”)。
②反應i和ii的平衡常數Kp與溫度的關系如圖1,則a_____________ 0(填“>”“ =” 或“<”);720℃時反應ⅲ的平衡常數Kp=_________________。
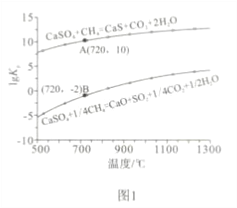

③下列措施可提高反應ii中甲烷平衡轉化率的是______________ 。
A.增加CaSO4固體的投入量 B.將水蒸氣冷凝
C.降溫 D.增大甲烷流量
(2)如圖2所示,該燃料反應器最佳溫度范圍為850℃-900℃之間,從化學反應原理的角度說明原因:
________________________。
(3)空氣反應器中發生的反應為
CaS(s) +2O2(g)=CaSO4(s) ΔH4=dkJ/mol
①根據熱化學原理推測該反應為 __________________(填“吸熱”或“放熱”) 反應。
(4)該原理總反應的熱化學方程式為_____________________________。
(5)25℃時,用Na2S沉淀Cu2+、Sn2+兩種金屬離子(M2+),所需S2-最低濃度的對數值lgc(S2-)與lgc(M2+)的關系如右圖所示,請回答:

25℃時向50mL的Sn2+、Cu2+濃度均為0.01 mol/L的混合溶液中逐滴加入Na2S溶液,當Na2S溶液加到150mL時開始生成SnS沉淀,則此時溶液中Cu2+濃度為___________mol/L。
【答案】 ii > 1.0×10-18 B 溫度過低,反應速率較慢;溫度較高,副反應增多 放熱 CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=(b+d)kJ/mol或ΔH=(a-c+d)kI/mol 2.5×10-13
【解析】(1)①:反應ii中生成的CaS在反應ⅲ中繼續反應,有利于反應ii的正向進行,反應的程度大,故ii反應是主要反應;②:反應i的lgK隨著溫度的升高增大,所以K也增大,平衡正向移動,所以正反應是吸熱反應,a>0;反應ⅲ= 反應i-反應ii,所以反應ⅲ的平衡常數Kp=Kpi/ Kp ii=(10-2)4÷1010=10-18;③:A、增加CaSO4固體的投入量對平衡無影響; B、將水蒸氣冷凝,生成物的濃度減小,平衡正向移動,CH4的轉化率增大;C、反應 ii的平衡常數隨溫度降低而降低,即降溫平衡逆向移動,CH4的轉化率減小;D、增大甲烷流量,平衡正向移動,但CH4的轉化率反而減小。故可提高反應ii中甲烷平衡轉化率的是B。
(2)溫度較低時,CaS的摩爾分數雖然較大,但反應速率太慢,溫度太高時,副產物CaO的含量較大,即副反應增多,故答案為:溫度過低,反應速率較慢;溫度較高,副反應增多。
(3) ①CaS(s) +2O2(g)=CaSO4(s)是一個熵減的自發反應,ΔS<0,根據吉布斯自由能ΔG=ΔH-TΔS<0,可知ΔH<0,所以該反應正反應一定是放熱反應。
(4) 對于CaSO4(s)+CH4(g)=CaS(s)+CO2(g)+2H2O(g)ΔH2=bkJ/mol和CaS(s)+2O2(g)=CaSO4(s) ΔH4=dkJ/mol,兩個熱化學方程式相加可得甲烷燃燒的熱化學方程式為:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=(b+d)kJ/mol,因為反應ⅲ= 反應i-反應ii,所以焓變關系有c=a-b,故有b=a-c,故ΔH=(b+d)kJ/mol=(a-c+d)kI/mol,答案為:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=(b+d)kJ/mol或ΔH=(a-c+d)kI/mol。
(5)兩條曲線均是溶解平衡曲線,lgc(Sn2+)+lgc(S2-)=-25,所以Ksp(SnS)=10-25, lgc(Cu2+)+lgc(S2-)=-35,所以Ksp(CuS)=10-35。向50mL的Sn2+、Cu2+濃度均為0.01 mol/L的混合溶液中逐滴加入150mL Na2S溶液時,Sn2+的濃度為0.01/4(mol/L),此時Sn2+開始沉淀,則c(S2-)= Ksp(SnS)÷c(Sn2+)=10-25÷0.01/4(mol/L)=4×10-23 mol/L,所以c(Cu2+)= Ksp(CuS)÷c(S2-)=10-35÷(4×10-23 )mol/L=2.5×10-13。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】生活中的有機物種類豐富,在衣食住行等多方面應用廣泛,其中乙醇和乙酸是比較常見的有機物。
(1)工業上用乙烯與水反應可制得乙醇,該反應的化學方程式為_______________(不用寫反應條件)。
(2)乙醇能夠發生氧化反應:乙醇在銅作催化劑的條件下可被氧氣氧化為乙醛,反應的化學方程式為_______。
(3)下列關于乙醇的說法正確的是______(選填字母)。
A.乙醇不能和酸性高錳酸鉀溶液發生氧化還原反應
B.乙醇只能被氧化成乙醛
C.黃酒中某些微生物使乙醇氧化為乙酸,于是酒就變酸了
(4)當乙酸分子中的O都是18O時,乙醇分子中的O都是16O時,二者在一定條件下反應,生成物中水的相對分子質量為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學實驗室需要0.5 mol·L-1硫酸溶液450 mL。根據溶液的配制情況回答下列問題:

(1)如圖所示的儀器中配制溶液肯定不需要的是______(填序號),配制上述溶液還需用到的玻璃儀器是________(填儀器名稱)。
(2)現用質量分數為98%、密度為1.84 g·cm-3的濃硫酸來配制450 mL、0.5 mol·L-1的稀硫酸。計算所需濃硫酸的體積為________ mL(保留1位小數),現有
①10 mL ②25 mL ③50 mL ④100 mL四種規格的量筒,你選用的量筒是________(填代號)。
(3)配制過程中需先在燒杯中將濃硫酸進行稀釋,稀釋時操作方法是__________________________________________________________。
(4)配制時,一般可分為以下幾個步驟:
①量取 ②計算 ③稀釋 ④搖勻 ⑤轉移 ⑥洗滌 ⑦定容 ⑧冷卻
其正確的操作順序為:②→①→③→________→ ________→________→________→④(填序號)。_________
(5)在配制過程中,其他操作都準確,下列操作中錯誤的是________(填代號,下同),能引起誤差偏高的有________。
①洗滌量取濃硫酸后的量筒,并將洗滌液轉移到容量瓶中
②未等稀釋后的H2SO4溶液冷卻至室溫就轉移到容量瓶中
③將濃硫酸直接倒入燒杯,再向燒杯中注入蒸餾水來稀釋濃硫酸
④定容時,加蒸餾水超過刻度線,又用膠頭滴管吸出
⑤轉移前,容量瓶中含有少量蒸餾水
⑥定容搖勻后,發現液面低于標線,又用膠頭滴管加蒸餾水至刻度線
⑦定容時,俯視刻度線
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在含有Fe3+、Fe2+、Cu2+的溶液中加入鐵粉,充分反應后,固體殘渣用鹽酸處理有氣體放出,則與鐵粉反應后的溶液中最多的離子是( )
A.Fe3+
B.Fe2+
C.Cu2+
D.H+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】ClO2(其中氧元素為-2價)是一種消毒殺菌效率高、二次污染小的水處理劑。實驗室中可通過以下反應制得ClO2:2KClO3+H2C2O4+H2SO4![]() 2ClO2↑+K2SO4+2CO2↑+2H2O。
2ClO2↑+K2SO4+2CO2↑+2H2O。
(1)該反應中氧化劑是__________。
(2)當收集到標況下氣體22.4L時,求參加反應的H2C2O4質量和物質的量__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“碳捕捉技術”是指通過一定的方法將工業生產中產生的CO2分離出來并利用。如可利用NaOH溶液來“捕捉”CO2,其基本過程如圖所示(部分條件及物質未標出)。
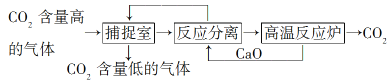
下列有關該方法的敘述中正確的是( )
①能耗小是該方法的一大優點
②整個過程中,有兩種物質可以循環利用
③“反應分離”環節中,分離物質的基本操作是蒸發、結晶
④該方法可減少碳排放,“捕捉”到的CO2還可用來制備甲醇等產品
A. ①③ B. ②④ C. ③④ D. ①④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【化學―選修5:有機化學基礎】
聚碳酸酯(PC)是一種強韌的熱塑性樹脂,廣泛用于玻璃裝配業、汽車工業、電子和電器工業。PC的一種合成路徑如下:
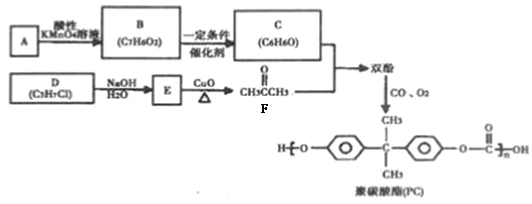
回答下列問題:
(1)烴A 的質譜圖如下,則A 的分子式為__________。
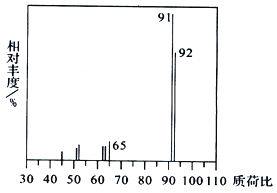
(2)D 的名稱為_________,D→E的反應類型為_______。
(3)雙酚的結構簡式為_______。
(4)B 和E 可以形成一種酯類物質F,寫出B + E→F反應的化學方程式:_______。
(5)F的同分異構體中,能同時滿足如下條件的共有______種(不考慮立體異構)。
① 分子中有兩個甲基;
② 能發生銀鏡反應;
③ 在酸性溶液中的水解產物遇FeC13 溶液顯紫色。
寫出其中核磁共振氫譜顯示5組峰,且峰面積比為62:2:11的種分子的結構簡式:_______。
(6)寫出由D分子合成甘油(丙三醇)的合成路線圖_______。(已知:![]() )
)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有機化學反應屬于加成反應的是
A.甲烷和氯氣混合光照顏色逐漸變淺B.乙烯通入溴的四氯化碳溶液使其褪色
C.苯和液溴混合物中加入鐵屑D.乙醇和金屬鈉反應產生氫氣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】能源“非石油化”是戰略目標,發展以CH4、CO2等為原料的“C1化學”成為當今化工生產的必然趨勢。通常天然氣中含有H2S等有毒氣體,下面為天然氣合成氨的工藝流程。
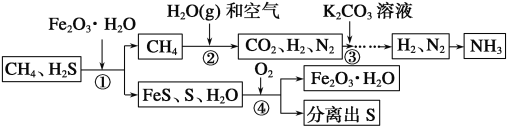
(1)合成氨的原料之一為氮氣,該流程中為合成氨提供氮氣的物質是__________。
(2)①處加入Fe2O3·H2O的目的是__________。
(3)②處CH4與H2O(g)反應生成CO2、H2,反應的化學方程式是_________________________。
(4)③處一般加入K2CO3溶液以吸收CO2,K2CO3溶液與CO2反應生成碳酸氫鉀(KHCO3),該反應的化學方程式是________________________。
(5)該流程中參與循環的物質是__________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com