
| 編號 | 操作 | 實驗現象 |
| ① | 分別在試管A、B中加入 5mL 5% H2O2溶液,各滴入1~2 滴1mol/L FeCl3溶液.待試管中均有適量氣泡出現時,將試管A放入盛有5℃左右冷水的燒杯中;將試管B放入盛有40℃左右熱水的燒杯中 | 試管A中不再產生氣泡 試管B中產生的氣泡量增大 |
| ② | 另取兩支試管分別加入 5mL 5%H2O2溶液和 5mL10%H2O2溶液 | 試管A、B中均未見氣泡產生 |
分析 (1)在FeCl3催化作用下,過氧化氫分解生成氧氣和水;
(2)實驗①中試管A、B中只有溫度不同,滴加FeCl3溶液雙氧水的分解速率增大,現象明顯;
(3)現象不明顯可以提高反應速率,結合影響化學反應速率的外界因素解答.
解答 解:(1)過氧化氫分解,FeCl3在此反應中作催化劑,起催化作用,能加快過氧化氫分解產生氧氣的速率,其反應的方程式為:2H2O2$\frac{\underline{\;FeCl_{3}\;}}{\;}$2H2O+O2↑,
故答案為:2H2O2$\frac{\underline{\;FeCl_{3}\;}}{\;}$2H2O+O2↑
(2)分別在試管A、B中加入 5mL 5% H2O2溶液,各滴入1~2 滴1mol/L FeCl3溶液.待試管中均有適量氣泡出現,說明過氧化氫分解能發生,試管A、B中均有適量氣泡出現時,將試管A放入盛有5℃左右冷水的燒杯中;將試管B放入盛有40℃左右熱水的燒杯中,兩支試管不同點是試管A的溫度比試管B的溫度低,說明研究的是溫度對反應速率的影響,而開始加滴加FeCl3溶液,目的加快H2O2分解,
故答案為:研究溫度對H2O2分解速率的影響;加快H2O2分解速率,使實驗現象易于觀察;
(3)影響化學反應速率的外界因素有濃度、溫度、氣體的壓強、催化劑、固體的表面積,另取兩支試管分別加入 5mL 5%H2O2溶液和 5mL10%H2O2溶液,試管A、B中均未見氣泡產生,為加快反應速率,可從溫度、或催化劑的影響角度考慮,
故答案為:將兩支試管同時放入盛有相同溫度熱水的燒杯中,或向兩支試管中同時滴入2滴1mol/L FeCl3溶液,觀察產生氣泡的速率.
點評 本題主要考查外界條件對反應速率的影響,側重于學生的實驗探究能力的考查,解答時須注意實驗的原理,難度中等.


科目:高中化學 來源: 題型:解答題
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | VIIA | O |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | (10) | (11) | (12) |
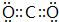
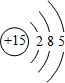 .
.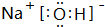 含有化學鍵為離子鍵、共價鍵
含有化學鍵為離子鍵、共價鍵查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑:Na<Mg<Al | B. | 酸性強弱:H2CO3<H2SiO3<HNO3 | ||
| C. | 熱穩定性:HF>HCl>HBr | D. | 非金屬性強弱:P>S>Cl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | R為第ⅣA族元素 | B. | R的氣態氫化物為H2R | ||
| C. | R能形成含氧酸H2RO4 | D. | R氣態氫化物水溶液呈堿性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 半徑:Al3+>Mg2+>Na+>F- | B. | 穩定性:HI<HBr<HCl<HF | ||
| C. | 酸性:HClO4<H2SO4<H3PO4 | D. | 堿性:Al(OH)3>Mg(OH)2>Ca(OH)2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 鐵鹽、亞鐵鹽在工農業生產、生活、污水處理等方面有極其廣泛的應用.
鐵鹽、亞鐵鹽在工農業生產、生活、污水處理等方面有極其廣泛的應用.
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 開始沉淀的pH | 2.3 | 7.5 | 3.4 |
| 完全沉淀的pH | 3.2 | 9.7 | 4.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鉀與鈉同一主族,鈉比鉀更容易從水中置換出氫 | |
| B. | 溴化鉀與碘化鉀溶液置于空氣中,溴化鉀更容易被氧化 | |
| C. | 過渡元素都是副族元素 | |
| D. | 同周期元素的原子,半徑越大,越容易失去電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ,取代反應
,取代反應 ,取代反應
,取代反應查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金剛石,晶體硅,碳化硅 | B. | CI4>CBr4>CCl4>CH4 | ||
| C. | MgO>CsCl>NaCl | D. | Na>Mg>Al |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com