
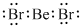 .
.| 共價鍵 | f-f | g-g | h-h | i-i |
| 鍵能(kJ/mol) | 157 | 242.7 | 193.7 | 152.7 |
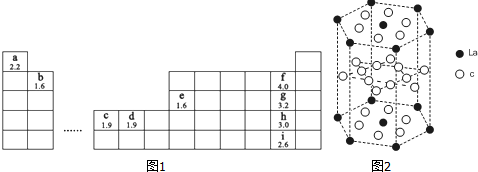
分析 由元素在周期表中位置,可知a為H,b為Be,c為Ni,d為Cu,e為Al,f為F,g為Cl、h為Br、i為I.
(1)b、h兩元素電負性之差小于1.7,二者形成化合物BeBr2屬于共價化合物,Be原子與Br原子之間形成1對共用電子對;
(2)計算AlCl3的分子Al原子的價層電子對數、孤電子對數,進而確定空間構型與雜化方式;
Al2Cl6中心原子Al形成4個σ鍵(其中1個為配位鍵),沒有孤電子對;
(3)可燃性氣體為氫氣,由于HCl濃溶液,配合物為H2CuCl4;
(4)F原子半徑較小,價電子較多,導致電子云密度增大,極大增加了兩原子間的排斥作用;
(5)c為Ni,原子核外由28個電子,根據能量最低原理書寫價電子排布式;晶胞采取平行六面體,是晶體的基本重復單元,晶胞通過無隙并置形成晶體;利用均攤法計算圖中六棱體中La原子、Ni原子數目,確定化學式.
解答 解:由元素在周期表中位置,可知a為H,b為Be,c為Ni,d為Cu,e為Al,f為F,g為Cl、h為Br、i為I.
(1)b、h兩元素電負性之差小于1.7,二者形成化合物BeBr2屬于共價化合物,Be原子與Br原子之間形成1對共用電子對.其電子式為: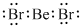 ,故答案為:
,故答案為: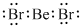 ;
;
(2)AlCl3的分子Al原子的價層電子對數=3+$\frac{3-1×3}{2}$=3,沒有孤電子對,故其空間構型為平面正三角形,Al原子采取sp2雜化,而Al2Cl6中心原子Al形成4個σ鍵(其中1個為配位鍵),沒有孤電子對,采取sp3雜化,故答案為:平面正三角形;sp2;sp3;
(3)可燃性氣體為氫氣,由于HCl濃溶液,配合物為H2CuCl4,反應方程式為:Cu+4HCl=H2CuCl4+H2↑,
故答案為:Cu+4HCl=H2CuCl4+H2↑;
(4)F原子半徑較小,價電子較多,導致電子云密度增大,極大增加了兩原子間的排斥作用,故鍵能較小,共價鍵易斷裂,
故答案為:F原子半徑較小,價電子較多,導致電子云密度增大,極大增加了兩原子間的排斥作用,故鍵能較小,共價鍵易斷裂;
(5)c為Ni,原子核外由28個電子,根據能量最低原理,可知價電子排布式為3d84s2;晶胞采取平行六面體,是晶體的基本重復單元,晶胞通過無隙并置形成晶體,畫出該晶體的一個晶胞如圖: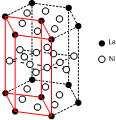 ;圖2中六棱體中La原子數目=12×$\frac{1}{6}$+2×$\frac{1}{2}$=3,六棱體中Ni原子數目=6+12×$\frac{1}{2}$+6×$\frac{1}{2}$=15,化學式為LaNi5,
;圖2中六棱體中La原子數目=12×$\frac{1}{6}$+2×$\frac{1}{2}$=3,六棱體中Ni原子數目=6+12×$\frac{1}{2}$+6×$\frac{1}{2}$=15,化學式為LaNi5,
故答案為:Ni;3d84s2; ;LaNi5.
;LaNi5.
點評 本題是對物質結構的考查,涉及核外電子排布、雜化方式、空間構型、配合物、晶胞結構與計算等,是對學生綜合能力的考查,難度較大.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:填空題
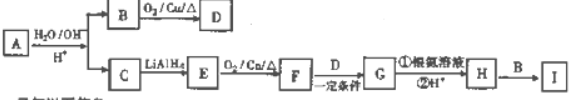
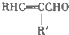 +H2O
+H2O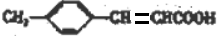 +CH3CH2OH$→_{△}^{濃硫酸}$
+CH3CH2OH$→_{△}^{濃硫酸}$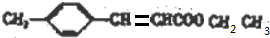 +H2O,反應類型為取代反應(酯化反應).
+H2O,反應類型為取代反應(酯化反應).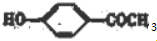 (寫結構簡式).
(寫結構簡式).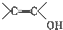 )結構.
)結構.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
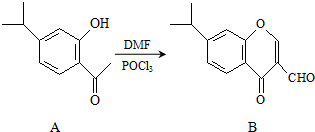 有機物A、B均為合成某種抗支氣管哮喘藥物的中間體,A在一定條件下可轉化為B(如圖所示),下列說法正確的是( )
有機物A、B均為合成某種抗支氣管哮喘藥物的中間體,A在一定條件下可轉化為B(如圖所示),下列說法正確的是( )| A. | 分子A中所有碳原子均位于同一平面 | |
| B. | 用FeCl3溶液可檢驗物質B中是否混有A | |
| C. | 物質B既能發生銀鏡反應,又能發生水解反應 | |
| D. | 1mol B最多可與5mol H2發生加成反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 開始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 催化劑的使用,可以降低反應的溫度,起到節能的效果 | |
| B. | 陶瓷刀大多是用一種納米材料“氧化鋯”為原料加工而成,具有硬度高、導熱性好、抗腐蝕等優點 | |
| C. | 石墨烯是一種由碳原子構成的單層片狀結構的新材料,因此具有巨大的表面積,通過穿透式電子顯微鏡可用于直接觀測單原子的吸附和釋放過程 | |
| D. | 推進脫硫、脫硝、除塵等設施改造,能大量減排SO2、NO2、PM2.5,使天空重現“蔚藍” |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 苯、乙醇和乙酸都能發生取代反應 | |
| B. | 葡萄糖注射液不能產生丁達爾效應現象,不屬于膠體 | |
| C. | 淀粉、油脂、蛋白質都能水解,但水解產物不同 | |
| D. | 白酒中混有少量塑化劑,少量飲用對人體無害,可通過過濾方法除去 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 溶液一定呈酸性 | B. | 溶液中一定存在:Y2-+H2O?OH-+HY- | ||
| C. | 溶液加水稀釋,離子濃度都減小 | D. | 溶液中:c(Na+)≥c(Y2-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 導致易拉罐變癟的離子反應是CO2+OH-=HCO3- | |
| B. | 導致易拉罐又鼓起來的反應是Al3++3HCO3-=Al(OH)3+3CO2↑ | |
| C. | 上述過程中共發生了三個化學反應,且反應結束后的溶液呈堿性 | |
| D. | 若將CO2換為NH3,濃NaOH溶液換為水,易拉罐也會出現先癟后鼓的現象 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | I A族和ⅦA族元素間可形成共價化合物或離子化合物 | |
| B. | 因H2SO3的酸性比H2CO3強,所以S的非金屬性比C強 | |
| C. | H2O2、CH3CH3、Cl-、K+中的電子數和質子數均分別相等 | |
| D. | Na+、Al3+、O2-、F-的半徑逐漸減小 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com