
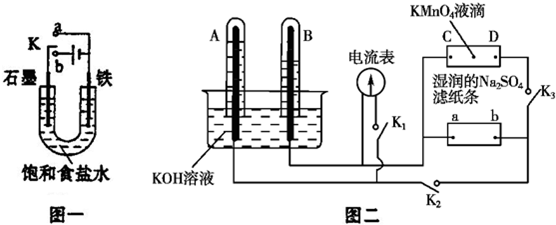
分析 Ⅰ.(1)若開始時開關K與a連接,該裝置構成原電池,發生電化學腐蝕中的吸氧腐蝕,正極上氧氣發生還原反應;
(2)若開始時開關K與b連接時,兩極均有氣體產生,則Fe作陰極,石墨作陽極,陽極上氯離子放電、陰極上氫離子放電;
Ⅱ.電解KOH溶液時,陽極上生成氧氣、陰極上生成氫氣,且氧氣和氫氣體積之比為1:2,根據圖知,A中氣體是氧氣、B中氣體是氫氣,則A中電極為陽極、B中電極為陰極;
(1)連接陽極的電極是正極、連接陰極的電極是負極;
(2)高錳酸鉀溶液中高錳酸根離子呈紅色,電解過程中,陽離子向陰極移動、陰離子向陽極移動;
(3)若A、B中均有氣體包圍電極,此時切斷K2、K3,閉合K1,電流表的指針偏轉,說明構成原電池,有氫氣的電極是負極、有氧氣的電極是正極,正極上氧氣得電子和水反應生成氫氧根離子.
解答 解:Ⅰ.(1)開關K與a連接,為原電池,NaCl溶液為中性,發生吸氧腐蝕,正極上氧氣得電子發生還原反應,電極反應式為O2+4e-+2H2O=4OH-,故答案為:吸氧;
(2)K與b連接,為電解池,若開始時開關K與b連接時,兩極均有氣體產生,則Fe作陰極,石墨作陽極,氯離子、氫離子放電,則N為電源負極,電解的總離子反應為2Cl-+2H2O$\frac{\underline{\;通電\;}}{\;}$2OH-+H2↑+Cl2↑,
故答案為:2Cl-+2H2O$\frac{\underline{\;通電\;}}{\;}$2OH-+H2↑+Cl2↑;
Ⅱ、電解KOH溶液時,陽極上生成氧氣、陰極上生成氫氣,且氧氣和氫氣體積之比為1:2,根據圖知,A中氣體是氧氣、B中氣體是氫氣,則A中電極為陽極、B中電極為陰極;
(1)連接陽極的電極是正極、連接陰極的電極是負極,a連接陰極,則a是負極,
故答案為:負;
(2)高錳酸鉀溶液中高錳酸根離子呈紅色,電解過程中,陽離子向陰極移動、陰離子向陽極移動,電解時,硫酸鈉溶液和鉑電極構成電解池,C是陰極、D是陽極,所以高錳酸根離子向陽極D電極移動,則看到的現象是紫色向D方向移動,兩個電極有氣體生成,
故答案為:紫色向D方向移動,兩極有氣體產生;
(3)若A、B中均有氣體包圍電極,此時切斷K2、K3,閉合K1,電流表的指針偏轉,說明構成原電池,有氫氣的電極是負極、有氧氣的電極是正極,正極上氧氣得電子和水反應生成氫氧根離子,電極反應式為O2+2H2O+4e-=4 OH-,
故答案為:O2+2H2O+4e-=4 OH-.
點評 本題考查了原電池和電解池原理,明確離子放電順序,根據各個電極上發生的反應來分析解答,把握電解質溶液的酸堿性確定生成的離子或物質,為易錯點,正確判斷正負極、陰陽極是解本題關鍵,知道各個電極上發生的反應,難點是電極反應式的書寫,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | O2、I2、Hg | B. | CO2、NaCl、KCl、Si | C. | HF、HCl、HBr | D. | 鎂鋁合金、Mg、Al |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題


查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 僅用AgNO3溶液便可鑒別亞硝酸鈉和食鹽 | |
| B. | 重結晶時,溶液冷卻速度越慢得到的晶體顆粒越大 | |
| C. | 乙酸與乙醇的混合液可用分液漏斗進行分離 | |
| D. | 醇都能發生取代反應,也都能發生消去和氧化反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
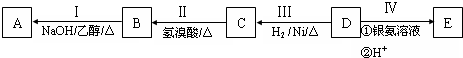
 ;
; 和
和 ;
;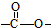 結構的有12種;E的另一種同分異構體能發生銀鏡反應,能與足量金屬鈉生成氫氣,不能發生消去反應,其結構簡式為
結構的有12種;E的另一種同分異構體能發生銀鏡反應,能與足量金屬鈉生成氫氣,不能發生消去反應,其結構簡式為 .
.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
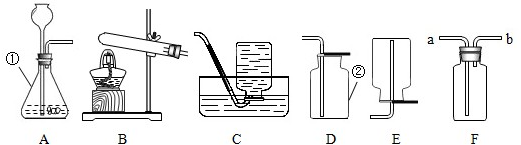
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分液時,分液漏斗下層液體從下口放出,上層液體從上口倒出 | |
| B. | 過濾時,引流的玻璃棒下端觸在三層濾紙處 | |
| C. | 蒸餾中,冷卻水應從冷凝管的下口通入,上口流出 | |
| D. | 用pH試紙測溶液的酸性時,應先將試紙用蒸餾水潤濕 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com