
| 元素 | V | W | X | Y | Z |
| 原子半徑(×0.1nm) | 0.37 | 0.77 | 0.75 | 0.74 | 1.85 |
| 電負性 | 2.1 | 2.5 | 3.0 | 3.5 | 1.66 |
| 常見化合價 | +1 | +4,-4 | +5,+3,-3 | -2 | +6,+3 |
2 1 |
2 1 |


 學期復習一本通學習總動員期末加暑假延邊人民出版社系列答案
學期復習一本通學習總動員期末加暑假延邊人民出版社系列答案 芒果教輔暑假天地重慶出版社系列答案
芒果教輔暑假天地重慶出版社系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
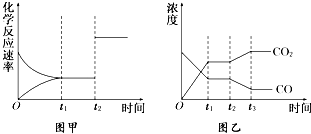 已知化學反應①:Fe(s)+CO2(g)?FeO(s)+CO(g),其平衡常數為K1;
已知化學反應①:Fe(s)+CO2(g)?FeO(s)+CO(g),其平衡常數為K1;| 溫度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
查看答案和解析>>
科目:高中化學 來源: 題型:
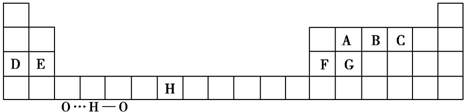
查看答案和解析>>
科目:高中化學 來源: 題型:
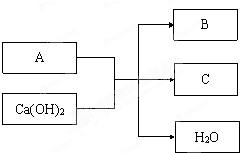
查看答案和解析>>
科目:高中化學 來源: 題型:
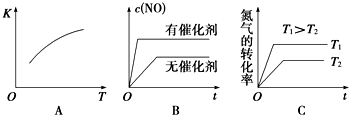
 工業上合成合成氨的熱化學方程式如下:
工業上合成合成氨的熱化學方程式如下:查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
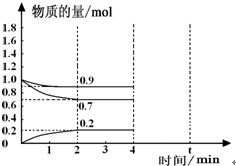
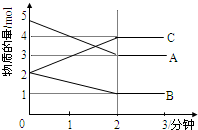 某可逆反應從0-2分鐘進行過程中,在不同反應時間各物質的量的變化情況如圖所示.則該反應的反應物是
某可逆反應從0-2分鐘進行過程中,在不同反應時間各物質的量的變化情況如圖所示.則該反應的反應物是查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com