

| A. | 電解過程中,a電極表面先有紅色物質析出,后有氣泡產生 | |
| B. | b電極上發生的反應方程式為:2H2O+2e-═2OH-+H2↑ | |
| C. | 從P到Q點時收集到的混合氣體的平均摩爾質量為12 g/mol | |
| D. | 從開始到P點收集到的氣體是O2 |
分析 由圖可知,電流由正極流向負極,則b為陽極,a為陰極,惰性電極電解一定量的硫酸銅溶液,發生2CuSO4+2H2O$\frac{\underline{\;通電\;}}{\;}$2Cu+O2↑+2H2SO4,結合圖2可知,通過0.2mol電子時電解硫酸銅,然后電解硫酸溶液,發生2H2O$\frac{\underline{\;通電\;}}{\;}$2H2↑+O2↑,P到Q點時收集到的混合氣體為氫氣和氧氣,以此來解答.
解答 解:由圖可知,電流由正極流向負極,則b為陽極,a為陰極,惰性電極電解一定量的硫酸銅溶液,發生2CuSO4+2H2O$\frac{\underline{\;通電\;}}{\;}$2Cu+O2↑+2H2SO4,結合圖2可知,通過0.2mol電子時電解硫酸銅,然后電解硫酸溶液,發生2H2O$\frac{\underline{\;通電\;}}{\;}$2H2↑+O2↑,
A.a為陰極,先發生Cu2++2e-═Cu,后發生2H++2e-═H2↑,a電極表面先有紅色物質析出,后有氣泡產生,故A正確;
B.b為陽極,溶液中的氫氧根離子放電,則b電極上發生的反應方程式為:4OH--4e-═H2O+O2↑,故B錯誤;
C.PQ段3.36L氣體中,由電解水反應可知0.2mol電子通過時生成0.1mol H2、0.05mol O2,故混合氣體的平均摩爾質量為$\frac{0.05×32+0.1×2}{0.1+0.05}$=12g•mol-1,故C正確;
D.由上述分析可知,曲線0~P段表示O2的體積變化,曲線P~Q段表示H2和O2混合氣體的體積變化,故D正確.
故選:B.
點評 本題考查電解原理,明確圖象這電子轉移與生成氣體的關系及離子的放電順序是解答本題的關鍵,熟悉電解原理即可解答,題目難度不大.


 世紀百通主體課堂小學課時同步達標系列答案
世紀百通主體課堂小學課時同步達標系列答案 世紀百通優練測系列答案
世紀百通優練測系列答案 百分學生作業本題練王系列答案
百分學生作業本題練王系列答案科目:高中化學 來源: 題型:選擇題
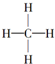 | 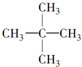 | 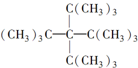 | … |
| 1 | 2 | 3 | … |
| A. | C36H74 | B. | C36H72 | C. | C53H106 | D. | C53H108 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 提出原子結構模型的科學家按時間先后依次是:道爾頓、湯姆生、盧瑟福、玻爾 | |
| B. | 已知PM2.5是指大氣中直徑≤2.5×10-6m的顆粒物,則受PM2.5污染的大氣不一定能產生丁達爾現象 | |
| C. | 借助儀器來分析化學物質的組成是常用的手段,原子吸收光譜常用來確定物質中含有哪些非金屬元素 | |
| D. | 并不是所有金屬元素都可以用焰色反應來確定其存在 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 硒化氫(H2Se)是有色、有毒的氣體,比H2S穩定 | |
| B. | Na2O2中陽離子與陰離子的個數比為1:1 | |
| C. | Ba(OH)2•8H2O晶體與氯化銨晶體反應不需要加熱就能發生,說明該反應是放熱反應 | |
| D. | 由H2→2H的過程需要吸收能量 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
 .
. .其中心原子的雜化類型為sp3.
.其中心原子的雜化類型為sp3. .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{N}{V}$ mol•L-1 | B. | $\frac{2N}{3V}$ mol•L-1 | C. | $\frac{N}{2V}$ mol•L-1 | D. | $\frac{3N}{2V}$ mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
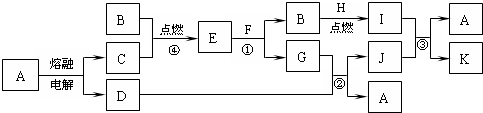
 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入AgNO3溶液,生成白色沉淀,加稀鹽酸沉淀不溶解,可確定有Cl-存在 | |
| B. | 加入幾滴KSCN溶液,溶液變成紅色,可確定有Fe3+存在 | |
| C. | 加入Ba(NO3)2溶液,生成白色沉淀,加稀鹽酸沉淀不消失,可確定有SO42-存在 | |
| D. | 加入鹽酸,生成的氣體能使澄清石灰水變渾濁,可確定有CO32-存在 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com