
【題目】求25℃時以下溶液的pH
(1)pH=3的鹽酸與pH=5的硫酸等體積混合后,pH=
(2)pH=10和pH=12的兩種NaOH溶液等體積混合后,pH=
(3)pH=9的NaOH溶液稀釋到原來的10倍后,pH= , 再稀釋到原來的1000倍后,pH .
(4)pH=12的NaOH和pH=4的HCl等體積混合后,pH= .
【答案】
(1)3.3
(2)11.7
(3)8;≈7
(4)11.7
【解析】解:(1)設兩種酸的體積都是1L,pH=3的鹽酸與pH=5的硫酸等體積混合后,混合溶液中氫離子濃度= ![]() =5.05×10﹣4 mol/L,則混合溶液的pH=﹣lg5.05×10﹣4=3.3, 所以答案是:3.3;(2)設兩種堿的體積都是1L,pH=10和pH=12的兩種NaOH溶液等體積混合后,混合溶液中氫氧根離子濃度=
=5.05×10﹣4 mol/L,則混合溶液的pH=﹣lg5.05×10﹣4=3.3, 所以答案是:3.3;(2)設兩種堿的體積都是1L,pH=10和pH=12的兩種NaOH溶液等體積混合后,混合溶液中氫氧根離子濃度= ![]() mol/L=5.05×10﹣3 mol/L,則混合溶液中氫離子濃度=
mol/L=5.05×10﹣3 mol/L,則混合溶液中氫離子濃度= ![]() mol/L=2×10﹣12mol/L,pH=11.7,
mol/L=2×10﹣12mol/L,pH=11.7,
所以答案是:11.7;(3)強堿溶液稀釋10倍是溶液的pH減小1,所以pH=9的NaOH溶液稀釋到原來的10倍后,pH=8,再稀釋到原來的1000倍后,溶液接近中性,則pH≈7,所以答案是:8;≈7;(4)pH=12的NaOH溶液中氫氧根濃度為0.01mol/L,pH=4的HCl中氫離子濃度為10﹣4mol/L,等體積混合后,堿過量,混合后溶液中氫氧根的濃度c(OH﹣)= ![]() =4.95×10﹣3mol/L,故氫離子濃度c(H+)=
=4.95×10﹣3mol/L,故氫離子濃度c(H+)= ![]() ≈2×10﹣11mol/L,故pH=11.7,所以答案是:11.7.
≈2×10﹣11mol/L,故pH=11.7,所以答案是:11.7.


科目:高中化學 來源: 題型:
【題目】具有顯著抗癌活性的10﹣羥基喜樹堿的結構如圖所示,下列關于10﹣羥基喜樹堿的說法正確的是( ) 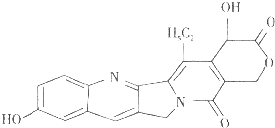
A.分子式為C20H17N2O5
B.該物質可發生消去反應
C.1mol該物質可與9molH2發生加成反應
D.1mol該物質可分別消耗Na、NaOH,Na2CO3的物質的量之比為2:2:1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將碘水中的碘萃取出來的實驗中,下列說法錯誤的是 ( )
A. 分液漏斗使用前要檢驗它是否漏水
B. 萃取劑要求不溶于水,且比水更容易使碘溶解
C. 注入碘水和萃取劑,倒轉分液漏斗反復用力振蕩后立即分液
D. 若用苯作萃取劑,則分層后上層液體呈紫紅色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究性學習小組對過量炭粉與氧化鐵反應的氣體產物成分進行研究.
(1)提出假設 ①該反應的氣體產物是CO2 .
②該反應的氣體產物是CO.
③該反應的氣體產物是 .
(2)設計方案如圖所示,將一定量的氧化鐵在隔絕空氣的條件下與過量炭粉完全反應,測定參加反應的碳元素與氧元素的質量比.
查閱資料
氮氣不與碳、氧化鐵發生反應.實驗室可以用氯化銨飽和溶液和亞硝酸鈉(NaNO2)飽和溶液混合加熱反應制得氮氣.請寫出該反應的離子方程式: .
(3)實驗步驟①按圖連接裝置,并檢查裝置的氣密性,稱取3.20g氧化鐵、2.00g碳粉混合均勻,放入48.48g的硬質玻璃管中;
②加熱前,先通一段時間純凈干燥的氮氣;
③停止通入N2后,夾緊彈簧夾,加熱一段時間,澄清石灰水(足量)變渾濁;
④待反應結束,再緩緩通入一段時間的氮氣.冷卻至室溫,稱得硬質玻璃管和固體總質量為52.24g;
⑤過濾出石灰水中的沉淀,洗滌、烘干后稱得質量為2.00g.
步驟②、④中都分別通入N2 , 其作用分別為 .
(4)數據處理試根據實驗數據分析,寫出該實驗中氧化鐵與碳發生反應的化學方程式: .
(5)實驗優化 學習小組有同學認為應對實驗裝置進一步完善.①甲同學認為:應將澄清石灰水換成Ba(OH)2溶液,其理由是 .
②從環境保護的角度,請你再提出一個優化方案將此實驗裝置進一步完善: .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列判斷正確的是 ( )
A. 酸性氧化物一定是非金屬氧化物 B. 堿性氧化物一定是金屬氧化物
C. SO2 溶于水能導電所以SO2 是電解質 D. Na2O是非電解質
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】不能用膠體的知識解釋的現象是( )
A. 向FeCl3溶液中加入NaOH溶液,出現紅褐色沉淀
B. 石膏點豆腐
C. 一支鋼筆使用兩種不同牌號的墨水,易出現堵塞
D. 江河入海處,易形成沙洲
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物A的相對分子質量184.5,其結構如圖1所示,(﹣R﹣代表某種烷基),A在一定條件下還有如圖2所示的反應關系,D不能發生銀鏡反應.
(1)C中含有的官能團為 , E→F的反應類型為;
(2)寫出A的結構簡式;
(3)寫出C→E的化學方程式;
(4)H的同分異構體很多,其中屬于酯類,含苯環,且水解產物中含有乙酸的同分異構體有種
(5)G顯酸性,M(B),M(G)分別表示B、G的相對分子質量,試求:M(G)﹣M(B)= .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在25℃時,密閉容器中X,Y,Z三種氣體的起始濃度和平衡濃度如表,下列說法錯誤的是( )
物質 | X | Y | Z |
初始濃度/molL﹣1 | 0.1 | 0.2 | 0 |
平衡濃度/molL﹣1 | 0.05 | 0.05 | 0.1 |
A.反應達到平衡時,X的轉化率為50%
B.反應可表示為X+3Y2Z,平衡常數為1600
C.其他條件不變時,增大壓強可使平衡常數增大
D.改變溫度可以改變該反應的平衡常數
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com